Tác giả: Kerasia‐Maria Plachouri MD, PhD, Sophia Georgiou MD, PhD
Biên dịch: Bác sĩ Yến Chi
Để tải bài viết Mesotherapy: Vấn đề an toàn và xử trí biến chứng, xin vui lòng click vào link ở đây.
Tóm lược
Tổng quát
Mesotherapy là một thủ thuật bao gồm việc tiêm các hoạt chất vào trong trung bì và mô dưới da để trị liệu nhiều bệnh lí và các nhu cầu thẩm mỹ. Mặc dù được coi là một phương pháp tương đối an toàn, một loạt các tác dụng phụ có thể xảy ra do do việc áp dụng rộng rãi và thiếu một quy trình tiêu chuẩn .
Mục tiêu
Mục tiêu của bài viết là tóm tắt tất cả các biến chứng liên quan đến mesotherapy được công bố cho đến nay, từ đó có sự quản lí chúng một cách đúng đắn
Phương pháp
Các bài viết có nguồn từ các dữ liệu, PubMed, EMBASE và SCOPUS, và được xuất bản từ năm 1992 đến 2018, được phân tích cho đánh giá này. Nghiên cứu được thực hiện theo guideline PRISMA.
Kết quả
Trong tài liệu này, có một số báo cáo về loạt ca lâm sàng và các trường hợp riêng biệt mô tả các tác dụng phụ khác nhau với mức độ nghiêm trọng khác nhau. Việc quản lí các biến chứng này – trong hầu hết các trường hợp – được cá nhân hóa.
Kết luận
Cần các nghiên cứu tổng hợp lớn hơn để đánh giá đầy đủ tính an toàn của liệu pháp mesotherapy và để xác định thông số điều trị được tiêu chuẩn hóa cũng như để giảm thiểu nguy cơ xảy ra các phản ứng có hại.
Giới thiệu
Mesotherapy là phương pháp điều trị hiện đại với nhiều chỉ định thẩm mỹ và không thẩm mỹ, được giới thiệu lần đầu tiên vào năm 1952 bởi bác sĩ người Pháp Pistor. Mục đích của thủ thuật này là vận chuyển các hoạt chất trực tiếp qua lớp biểu bì vào trong lớp trung bì hoặc các lớp da sâu hơn, để kích hoạt các nguyên bào sợi và tổng hợp collagen, cũng như đảo ngược quá trình thoái hóa của elastin và sự mất nước liên tục qua thượng bì, xảy ra trong quá trình lão hóa.Việc sử dụng các hoạt chất này bằng cách thoa ngoài không thể có kết quả tương tự, do sự suy giảm khả năng thâm nhập của chúng qua hàng ràng lipid và lớp sừng, hoặc do sự phân hủy hóa học của chúng trên bề mặt thượng bì. Mesotherapy đã trở nên vô cùng phổ biến trong những năm qua, bởi vì thực tế là nó giúp vận chuyển trực tiếp thuốc một vào các vùng mong muốn một cách kinh tế hơn và chỉ cần đào tạo tối thiểu cho các bác sĩ. Sự phát triển của các quy trình điều trị mesotherapy cho nhiều chỉ định làm cho việc đánh giá an toàn tích lũy trở nên khó khăn và không có nghiên cứu đoàn hệ nào lớn hơn để đánh giá rủi ro của mesotherapy được thực hiện cho tới thời điểm này. Báo cáo này nhằm trình bày tất cả các biến chứng liên quan mesotherapy được báo cáo trong tài liệu cho đến nay và cung cấp một cái nhìn sâu sắc về việc quản lí chúng.
2. Tài liệu và phương pháp
Nghiên cứu này được thực hiện dựa theo các guideline của PRISMA (Preferred Reporting Items for Systematic Reviews) cho các đánh giá có tính hệ thống. Dữ liệu của MEDLINE (PubMed), EMBASE, và SCOPUS đã được sàng lọc bằng cách sử dụng các thuật ngữ Mesh sau: “mesotherapy”. “microneedling”, “subcutaneous injection”, “side effect”, “complication” và “adverse reaction”. Các tư liệu khác cũng được xác định từ danh sách tài liệu tham khảo của các tài liệu và trích dẫn được truy xuất ở trên, được xác nhận bởi Web of Science. Nghiên cứu của chúng tôi bao gồm các bài báo bằng tiếng Anh, tiếng Tây Ban Nha, tiếng Đức và tiếng Pháp được xuất bản từ năm 1992 đến năm 2018. Quá trình lựa chọn bao gồm sàng lọc tiêu đề và tóm tắt đầu tiên, sau đó đánh giá các bài báo toàn văn.
3. Kết quả
Biến chứng nhiễm trùng
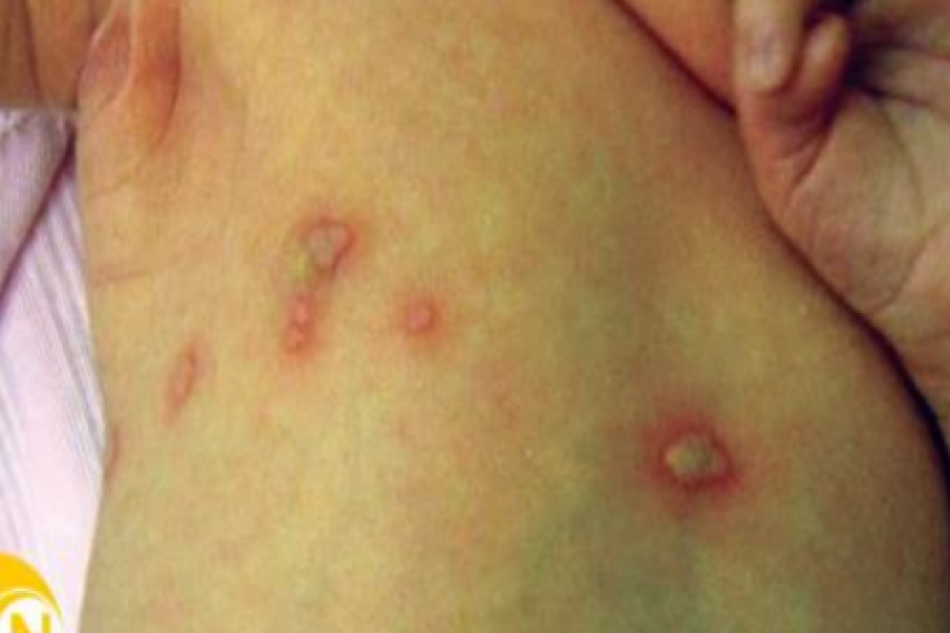
Trong số các phản ứng bất lợi chính trong quá trình thực hiện mesotherapy là các phản ứng liên quan tới vấn đề vô trùng và nguy cơ nhiễm trùng. Orjuela và các công sự đã trình bày một loạt các ca lâm sàng của 6 bệnh nhân xuất hiện tổn thương lao da do Mycobacterium tuberculosis sau tiêm hỗn hợp mesotherapy không xác định cho điều trị “sần vỏ cam”. Bất chấp hiệu quả của việc điều trị kháng sinh chuẩn, cuối cùng không phải lúc nào cũng tránh được sẹo vĩnh viễn. Tự lành vết thương sau vài tháng cũng được ghi nhận ở một trong số những bệnh nhân từ chối điều trị bằng kháng sinh. Trong khi nhiễm M.tuberculosis hiếm khi được mô tả trong y văn, có một lượng lớn các báo cáo về nhiễm trùng tại vị trí tiêm với mycobacteria không điển hình cơ hội, ngay cả ở các dạng bùng phát liên quan tới vị trí điều trị đặc hiệu. Hầu hết các mycobacteria riêng biệt trong các ca lâm sàng được báo cáo bao gồm M.abscessus, M.chelonae và M.fortuitum trong khi các bài báo cáo ít phổ biến hơn bao gồm các loài không quá phổ biến như M.cosmeticum hoặc M.immunogenum cũng như M.bovis trong một số trường hợp hiếm gặp. Việc điều trị nhiễm trùng mycobacteria có thể rất khó khăn do khả năng đa kháng thuốc của nó. Phương pháp điều trị nên được cá nhân hóa sau khi làm kháng sinh đồ và nên bao gồm ít nhất 2 kháng sinh để giảm nguy cơ kháng thuốc. Trong các trường hợp khó, phác đồ kết hợp 3 kháng sinh cũng đã được ghi nhận . Hầu hết các vi khuẩn mycobacteria nhạy cảm với các kháng sinh như clarithromycin, erythromycin, amikacin, doxycycline, ciprofloxacin, tobramycin, tigecycline và cefoxitin. Trong phần lớn các trường hợp, thời gian điều trị có thể dao động từ 2 tới 6 tháng, phụ thuộc vào khả năng miễn dịch của bệnh nhân và mức độ trầm trọng của nhiễm trùng. Nhiều trường hợp, vẫn còn các tổn thương mặc dù đã điều trị kháng sinh kéo dài. Một cách tiếp cận khác với các ca nhiễm mycobacteria kháng thuốc là phẫu thuật cắt bỏ các tổn thương đơn độc có hoặc không có liệu pháp kháng sinh kèm theo. Nên lưu ý rằng, ngay cả trong các trường hợp điều trị nhiễm trùng thành công, vẫn còn tồn tại các tổn thương sẹo vĩnh viễn.
Ngoài mycobacteria, các vi sinh vật khác là tác nhân gây nhiễm trùng liên quan đến mesotherapy cũng được ghi nhận. Rodriguez – Gutierez và công sự mô tả một ca nhiễm trùng Nocardia brasiliensis khởi phát 1 tuần sau điều trị mesotherapy với silica, axit triiodoacetic và dầu atiso ở bụng của một phụ nữ 30 tuổi. Sau khi điều trị 3 tháng với 800/160mg trimethoprim/ sulfmethoxazole mỗi 12 tiếng và 100mg dapsone mỗi ngày, bệnh nhân thuyên giảm hoàn toàn. Nấm sâu Sporotrichosis liên quan mesotherapy cũng được mô tả bởi Gama và cộng sự trong một báo cáo của 2 bệnh nhân:ở những ca này, lựa chọn điều trị là 300mg kali iodua, 3 lần/ngày, trong 8 tháng và 10mg itraconazole, mỗi ngày trong 6 tháng, tương ứng, cho tới khi điều trị khỏi hoàn toàn các tổn thương. Để giảm thiểu nguy cơ nhiễm trùng, điều quan trọng là các thủ thuật xâm lấn nhỏ như vậy phải được thực hiện bởi các bác sĩ được cấp phép, những người tuân thủ các quy định vô trùng, vì lớp thượng bì có thể được coi như một chất mang tạm thời cho một số vi khuẩn mycobacteria không điển hình như M.fortuitum. Điều kiện vệ sinh phù hợp trong các phòng khám điều trị và việc sử dụng các dụng cụ vô trùng như bông cotton hoặc kem bôi tê, cũng nên được đảm bảo. Vì các báo cáo về các sản phẩm vi lượng đồng cân bị nhiễm bẩn với các quy trình sản xuất, xử lý và đóng gói nghi vấn cũng đã được báo cáo, nên khuyến khích sử dụng các sản phẩm tiêm đã được kiểm duyệt chính thức theo các guideline đảm bảo vô trùng chuẩn.
Biến chứng không nhiễm trùng
Khi nói đến các biến chứng không nhiễm trùng, một số loại phản ứng bất lợi đã được mô tả, hầu hết là các báo cáo đơn độc của từng bệnh nhân.
Các phản ứng dị vật dạng u hạt đã được báo cáo xảy ra sau khi tiêm mesotherapy các hoạt chất như phosphatidylcholine, deoxycholate, buflomedil, silica hoặc carnitine cũng như một lượng lớn các hoạt chất khác, trong một số trường hợp thậm chí là cả các hoạt chất gốc dầu, được sử dụng rộng rãi cho mục đích tiêu mỡ. Xử lý các trường hợp này có thể bao gồm việc sử dụng steroid tiêm trong tổn thương như triamcinolone acetonide một vài liệu trình. Các cách tiếp cận với việc sử dụng corticosteroid toàn thân cũng đã được mô tả, tuy nhiên, không có lợi ích đáng kể, trong khi việc sử dụng 100mg dapsone mỗi ngày trong vài tuần đã được Gokdemir và cộng sự báo cáo là dẫn đến cải thiện đáng kể các tổn thương u hạt. Ramos-e-Silva và cộng sự mô tả một trường hợp oleoma, một loại phản ứng u hạt nặng sau tiêm mesotherapy gốc dầu điều trị sần vỏ cam. Các tổn thương còn lại không đáp ứng với steroid hệ thống nhưng dường như đáp ứng với điều trị bằng colchicine 0.5 mg/ngày trong hơn 3 tháng, tuy nhiên, để lại sẹo lõm. Một trường hợp u hạt vòng liên quan mesotherapy cũng được báo cáo bởi Strahan và cộng sự, tuy nhiên không có thông tin về điều trị thành công được cung cấp trong báo cáo này.
Ngoài sự hình thành u hạt, một tác dụng phụ khác thường thấy là phản ứng viêm nổi bật do tiêm hoạt chất mesotherapy dẫn đến hình thành các vi áp-xe trong trung bì, vách ngăn hoặc thuỳ mỡ, hoặc thậm chí trong các trường hợp nặng, hoại tử mỡ lan rộng cùng với các nốt vôi hóa nhỏ và hình thành u nang dưới da, đồng thời hình thành loét. Điều này đặc biệt quan sát thấy với các loại cocktail mesotherapy chứa phosphatidylcholine, trong điều trị sần vỏ cam. Các trường hợp viêm kẽ mô mỡ dưới da đã khẳng định bằng mô bệnh học liên quan mesotherapy cũng được ghi nhận trong y văn. Về xử trí, dapsone đã được sử dụng thành công trong những trường hợp độc lập. Tan cùng cộng sự đã báo cáo kết quả lâm sàng hoàn chỉnh với 100mg dapsone mỗi ngày, trong khoảng thời gian 3 tháng. Davis cùng cộng sự cũng báo cáo cải thiện viêm mô hạt không đáp ứng steroid theo cùng một phác đồ. Lee và cộng sử mô tả một một trường hợp viêm mô mỡ dưới da đã xác định bẳng mô bệnh học do tiêm dưới da 5% dextrose kết hợp lidocain làm trầm trọng thêm mức độ hoại tử của mô mỡ và dịch hóa kèm sự hình thành vết loét. Một phác đồ với minocycline (100mg/ngày trong 2 tuần) và prednisolone (20mg/ngày trong 2 tuần) ghi nhận thất bại điều trị, do đó các tác giả điều trị bảo tồn tại chỗ bằng băng vết thương và bôi mupirocin. Các phác đồ khác cho vết loét da liên quan mesotherapy bao gồm việc sử dụng 100mg doxycyclin mỗi ngày, kết hợp điều trị tại chỗ bằng axit fusiduc 2% hoặc hydrocortisone acetat 1% , được ghi nhận bỏi Al – Khenaizan. Một trong các ứng dụng của mesotherapy là điều trị rụng tóc androgen. Tuy nhiên, rụng tóc sẹo hay không sẹo đều có thể xảy ra do kết quả của việc điều trị, chủ yếu là do hoại tử mỡ do mesotherapy và hình thành ổ apxe. Một trường hợp như thế đã được ghi nhận bởi Kadry và cộng sự, điều trị bảo tồn dường như không có tác dụng, vì vậy phẫu thuật cắt bỏ mô viêm là giải pháp được lựa chọn. El-Komy và cộng sự mô tả 3 ca bệnh, trong đó đặc điểm mô học nổi bật không phải là viêm mô mỡ mà là sự hình thành sẹo viêm với thâm nhiễm tế bào lympho quanh mạch và quanh nang lông và tăng sản tuyến bã nhờn cũng như sự phì đại của sợi collagen quanh nang lông. Loại cocktail mesotherapy được sử dụng trong 2 trong 3 ca bao gồm dutasteride 0.005 % (Mesologica®), yếu tố tăng trưởng giống insulin -1 (IGF‐1), yếu tố tăng trưởng nguyên bào sợi cơ bản (bfGf), yếu tố tăng trưởng nội mạch (VEGF), copper tripeptide‐1, multi‐vitamins, amino acids, and khoáng chất (Mesologica MRS Hair®). Việc xử trí các phản ứng bất lợi này bao gồm kê đơn minoxidil bôi hoặc áp dụng phương pháp tiêm nước muối trong tổn thương 2 lần một ngày ở các vùng bị ảnh hưởng, kết hợp với dung dịch melatoin tại chỗ. Các trường hợp rụng tóc không sẹo, một tác dụng phụ cấp tính của mesotherapy cũng đã được mô tả. Các đặc điểm mô bệnh học chính ở đây không có mặt các nang anagen tận cùng và số lượng đơn vị nang telogen và catagen tăng lên được ghi nhận trong các trường hợp rụng tóc anagen. Rõ ràng, việc quản lí điều trị, trong trường hợp nay bao gồm cả phương pháp chờ và xem xét, tuy nhiên sinh thiết là cần thiết để có thể phân biệt với một bệnh nhân như vậy với một bệnh nhân rụng tóc có sẹo và từ đó cần điều trị kháng viêm phù hợp.
Một số biến chứng da liễu khác ở dạng phản ứng không dung nạp đã được báo cáo trong một số ca riêng lẻ, là kết quả của các điều trị mesotherapy. Khi nói đến mày đay cấp tính sau mesotherapy, cách tiếp cận được đề xuất là ngừng điều trị và sử dụng kháng histamin. Trong số ít các trường hợp được mô tả trong y văn, sẩn mày đay ban đầu chỉ giới hạn ở vùng điều trị. Các phản ứng không dung nạp khác đã được báo cáo bao gồm ban do thuốc dạng lichen, từ đó cần ngừng điều trị và sử dụng steroid toàn thân. Điều thú vị là, liệu pháp mesotherapy thường bị coi là yếu tố khởi phát dẫn tới sự trầm trọng của các bệnh da liễu sẵn có qua hiện tượng Koebner. Rosina và các cộng sự đã mô tả một trường hợp nữ bệnh nhân 67 tuổi, người đã hình thành vảy nến thể mảng lan tỏa sau điều trị mesotherapy với hỗn hợp aminophyllin, xantinol nicotinate và lidocain. Một liệu trình bắt đầu với cyclosporine A, liều khởi đầu 4mg/kg/ngày và sau đó giảm dần trong 14 tuần. Trong một trường hợp tương tự, mày đay sắc tố tại chỗ ở bệnh nhân rối loạn tế bào mast ẩn được báo cáo bởi Bessis và cộng sự. Ở đây, phương pháp điều trị được lựa chọn là bôi kem corticosteroid độ mạnh trung bình trong vài tuần, để cải thiện một phần các tổn thương. Một trường hợp hiếm của sự khởi phát của tổn thương dạng hồng ban nút sau mesotherapy ở bệnh nhân bị bệnh Behcet được mô tả trong y văn. Các tổn thương cho thấy chỉ đáp ứng một phần với phác đồ khởi đầu với colchicin, prednisolone (32mg/ngày và sau đó giảm dần), và azathioprine (2.5 mg/kg/ngày). Mặc dù trường hợp này không được mô tả giống một dấu hiệu Koebner, mà là test pathergy dương tính – một phản ứng tăng hoạt tính được thấy trong bệnh Behcet là một phản ứng với chấn thương ở da – nó vẫn là một dấu hiệu mà mesotherapy có thể kích hoạt sự bùng phát của các bệnh lí da liễu và tình trạng toàn thân mà một số cơ chế bệnh sinh không phải lúc nào cũng được hiểu đầy đủ. Như vậy, một trường hợp lupus ban đỏ hệ thống nặng được báo cáo ở một bệnh nhân 31 tuổi sau tiêm meso với acetyl – L – carnitine, một hoạt chất được biết tới với tác dụng điều hòa miễn dịch, thường được sử dụng cho mục đích giảm béo. Trong trường hợp đáng chú ý này được Colon-Soto và cộng sự mô tả, một phác đồ ức chế miễn dịch tích cực với methylprednisolone cách quãng, prednisone uống hàng ngày, cũng như một liệu pháp cách quãng với cyclophosphamide tiêm tĩnh mạch, là cần thiết để kiểm soát bệnh.
Các biến chứng cơ học ít gặp hơn do sự dịch chuyển của hoạt chất được tiêm trong quá trình trị liệu mesotherapy. Calonge và cộng sự mô tả mộ trường hợp của một phụ nữ 43 tuổi bị phù dưới da nặng ở hạ sườn phải và thành bụng trước cho đến nếp lằn vú, sau tiêm dưới da khí CO2 ở cả hai đùi vài ngày trước đó. Khí được hấp thu trong vòng 10 ngày và ngoài việc dùng kháng sinh không cần một can thiệp cụ thể nào khác. Việc vô tình tiêm hoạt chất vào tiểu động mạch có thể dẫn đến tắc mạch với viêm da dạng mạng lưới và hoại tử da, một tình trạng được biết đến là tắc mạch do thuộc hay hội chứng Nicolau. Việc xử trí các trường hợp như vậy thì ngoài điều trị tại chỗ bằng băng vết loét còn phải sử dụng các chất chống đông máu toàn thân và sử dụng các thuốc giãn mạch toàn thân. Zaragoza và cộng sự báo cáo một ca bệnh 53 tuổi hội chứng Nicolau liên quan mesotherapy được điều trị thành công, bằng enoxaparin liều 175 UI/kg mỗi ngày, kết hợp với amlodipine đường uống trong thời gian 4 tháng.
Một loại khác của các phản ứng bất lợi của mesotherapy bao gồm ảnh hưởng của các hoạt chất được tiêm khi hấp thu toàn thân. Một ca lâm sàng ngộ độc caffein hiếm gặp ở một bệnh nhân 51 tuổi, người được tiêm dưới da một loại cocktail có chứa caffein, được ghi nhận bởi Vulkevic và cộng sự. Phương pháp xử trí được lựa chọn là điều trị hỗ trợ và triệu chứng. Một trường hợp hiếm gặp giả nhiễm độc giáp liên quan mesotherapy cũng được mô tả trong y văn. Ở trường hợp này bệnh nhân biểu hiện một nhiễm độc giáp cơ năng sau tiêm một loại cocktail mesotherapy chứa axit triiodothyroacetíc, cũng như hợp chất hoạt mạch, giúp axit triiodothyroacetic hấp thu tốt hơn. Chức năng tuyến giáp đã được bình thường hóa sau khi ngừng trị liệu mesotherapy và không cần các phương pháp cụ thể nào khác. Một tác dụng vận mạch có thể có sau tiêm meso cũng được mô tả bởi Kim và cộng sự, họ báo cáo trường hợp viêm ruột do thiếu máu cục bộ sau khi tiêm meso kết hợp thuốc giảm béo. Loại cocktail có chứa aminophyllie, epinephrine và lidocain và thuốc uống bao gồm fluoxetine, ephedrine hydrochloride, anhydrous caffeine và bột trà xanh. Các tác giả cho rằng viêm ruột do thiếu máu cục bộ xảy ra do tác dụng co mạch trực tiếp và gián tiếp của các hoạt chất đã sử dụng, và việc xử trí ở đây bao gồm liệu pháp hỗ trợ với truyền dịch, điện giải và kháng sinh. Tor và cộng sự đã mô tả trường hợp nữ bệnh nhân 40 tuổi, người biểu hiện một trạng thái mê sảng và loạn thần biệt lập, khoảng 12h sau một liệu trình mesotherapy với các hoạt chất không rõ. Các tác giả của công trình đưa ra giả thuyết rằng việc các hoạt chất đã tiêm có thể tác động tới nhu mô não sau khi vượt qua hàng rào máu não. Tuy nhiên, việc thiếu thông tin về hỗn hợp đã sử dụng cũng như thiếu các dữ liệu liên quan, gây khó khăn trong thiết lập một mối quan hệ nhân quả nhất định giữa mesotherapy và trạng thái biệt lập này.
Các biến chứng ít nghiêm trọng hơn của mesotherapy bao gồm đau liên quan đến thủ thuật, bầm tím và phù nề do viêm khởi phát bởi các hoạt chất được tiêm. Chúng có xu hướng tương đối khu trú và tạm thời và xử lí chúng bao gồm việc bôi tê tại chỗ cũng như khoảng thời gian dài hơn giữa các lần thăm khám. Các triệu chứng nhẹ đau đầu tự giới hạn và ngứa cũng đã được mô tả trong trị liệu mesotherapy ở da đầu. Mặc dù có thể có chảy máu nhẹ hoặc tụ máu dễ tái hấp thu do tiêm, sự hình thành khối máu tụ lớn hơn cũng đã được mô tả trong những trường hợp cực kì hiếm gặp.
Cuối cùng, một biến chứng có khả năng đe dọa tính mạng đã được báo cáo gần đây bởi Arenbergevora và cộng sự mô tả sự phát triển của ung thư sắc tố dạng nốt trên một bớt bẩm sinh ở da đầu của một bệnh nhân 49 tuổi sau điều trị rụng tóc Telogen nhẹ, với một hỗn hợp mesotherapy chứa IGF-1, betaFGF, VEGF, copper tripeptide- 1, cũng như chiết xuất tế bào gốc trung mô. Mặc dù các tác giả không loại trừ khả năng xảy ra một tình huống ngẫu nhiên, nhưng sự gia tăng tiềm năng phát triển ung thư hắc tố do tác động của tất cả các yếu tố tăng trưởng được tiêm chắc chắn cần được xem xét. Cần tiến hành thêm các nghiên cứu về tính an toàn của các hoạt chất đó trên khía cạnh phát triển ung thư để có kết luận rõ ràng. Hơn nữa, nên thăm khám cẩn thận khu vực được điều trị, thận trọng với các bớt sắc tố.
Kết luận
Mesotherapy đang trở thành một thủ thuật ngày càng phổ biến, hiện nay được áp dụng rộng rãi không chỉ bởi các bác sĩ mà còn bởi các cá nhân không chuyên về y tế trong các cơ sở thẩm mỹ. Hầu hết bệnh nhân và trong một số trường hợp, ngay cả bác sĩ, có xu hướng đánh giá thấp tác dụng phụ tiềm ẩn có thể xảy ra bởi các phương pháp này. Để giảm thiểu nguy cơ của các phản ứng có hại, cần phải đảm bảo tiêu chuẩn hóa quy trình này cho từng chỉ định. Phải đảm bảo đào tạo chuyên môn, kiến thức khoa học nền đầy đủ cũng như tuân thủ các tiêu chuẩn vệ sinh cơ bản để tối ưu hóa điều trị. Hơn nữa, điều quan trọng hơn là phải bao gồm cả sự đồng thuận trước khi bắt đầu điều trị, không chỉ để bảo vệ bác sĩ khỏi các biến chứng có tính pháp lí có thể xảy ra, mà còn để giáo dục bệnh nhân hiểu rõ hơn về lợi ích và rủi ro của quy trình này nói chung.
Tài liệu tham khảo
- Kim JT, Choi A, Jeong JH, et al. Safety evaluation and consideration of 4 pin multi‐needle for mesotherapy. Technol Health Care. 2018;26:291‐306.
- Markiewicz A, Zasada M, Erkiert‐Polguj A, Wieckowska‐Szakiel M, Budzisz E. An evaluation of the antiaging properties of strawberry hydrolysate treatment enriched with L‐ascorbic acid applied with microneedle mesotherapy. J Cosmet Dermatol. 2019;18:129‐135.
- Wermeling DP, Banks SL, Hudson DA, et al. Microneedles permit transdermal delivery of a skin‐impermeant medication to humans. Proc Natl Acad Sci. 2008;105:2058‐2063.
- Almohanna HM, Perper M, Tosti A. Safety concerns when using novel medications to treat alopecia. Expert Opin Drug Saf. 2018;17:1115‐ 1128.
- Arenbergerova M, Arenberger P, Gkalpakiotis S, Dahmen RA, Sticova E, Fialova A. Scalp melanoma after antihair loss mesotherapy. J Eur Acad Dermatol Venereol. 2018;32(5):e187‐e188.
- Orjuela D, Puerto G, Mejía G, et al. Cutaneous tuberculosis after mesotherapy: report of six cases. Biomedica. 2010;30:321‐326.7.
- Centers for Disease Control and Prevention (CDC). Outbreak of mesotherapy‐associated skin reactions–district of Columbia area, january‐february 2005. MMWR Morb Mortal Wkly Rep. 2005;54(44):1127‐1130.
- Galmés‐Truyols A, Giménez‐Duran J, Bosch‐ Isabel C, et al. An outbreak of cutaneous infection due to Mycobacterium abscessus associated to mesotherapy. Enferm Infecc Microbiol Clin. 2011;29:510‐514.
- Wongkitisophon P, Rattanakaemakorn P, Tanrattanakorn S, Vachiramon V. Cutaneous Mycobacterium abscessus infection associated with mesotherapy injection. Case Rep Dermatol. 2011;3:37‐41.
- Da Mata JO, Hernández‐Pérez R, Corrales H, Cardoso‐Leao S, de Waard JH. Follow‐up on an outbreak in Venezuela of soft‐tissue infection due to Mycobacterium abscessus associated with mesotherapy. Enferm Infecc Microbiol Clin. 2010;28:596‐601.
- Couderc C, Carbonne A, Thiolet JM, et al. Non‐tuberculous mycobacterial infections related to esthetic care in France, 2001–2010. Med Mal Infect. 2011;41:379‐383.
- Correa NE, Cataño JC, Mejía GI, et al. Outbreak of mesotherapy‐associated cutaneous infections caused by Mycobacterium chelonae in Colombia. Jpn J Infect Dis. 2010;63:143‐145.
- Regnier S, Cambau E, Meningaud JP, et al. Clinical management of rapidly growing mycobacterial cutaneous infections in patients after mesotherapy. Clin Infect Dis. 2009;49:1358‐ 1364.
- Quiñones C, Ramalle‐Gómara E, Perucha M, et al. An outbreak of Mycobacterium fortuitum cutaneous infection associated with mesotherapy. J Eur Acad Dermatol Venereol. 2010;24:604‐606.
- Nagore E, Ramos P, Botella‐Estrada R, Ramos‐Níguez JA, Sanmartín O, Castejón P. Cutaneous infection with Mycobacterium fortuitum after localized microinjections (mesotherapy) treated successfully with a triple drug regimen. Acta Derm Venereol. 2001;81:291‐293.
- Difonzo EM, Campanile GL, Vanzi L, Lotti L. Mesotherapy and cutaneous Mycobacterium fortuitum infection. Int J Dermatol. 2009;48:645‐647.
- Del‐Castillo M, Palmero D, Lopez B, et al. Mesotherapy‐associated outbreak caused by Mycobacterium immunogenum. Emerg Infect Dis. 2009;15:357‐359.
- Marco‐Bonnet J, Beylot‐Barry M, Texier‐ Maugein J, et al. Mycobacterial bovis BCG cutaneous infections following mesotherapy: 2 cases. Ann Dermatol Venereol. 2002;129:728‐ 731.
- Rodríguez‐Gutiérrez G, Toussaint S, Hernández‐Castro R, Sánchez‐ León Mdel C, Arenas R Nocardia brasiliensis infection: an emergent suppurative granuloma after mesotherapy. Int J Dermatol. 2014;53:888‐890.
- González F, Hernández C, Henao L, et al. Infección cutánea por Micobacterias y Nocardia asociada a mesoterpia. Vitae. 2004;20:1‐7.
- Gamo R, Aguilar A, Cuétara M, et al. Sporotrichosis following mesotherapy for arthrosis. Acta Derm Venereol. 2007;87:430‐431.
- Kutlubay Z, Gokalp H, Ince U, Engin B. Cutaneous foreign body granulomas associated with lipolytic cocktail: who is the enemy, mesotherapy or drugs injected? J Cosmet Laser Ther. 2017;19:310‐312.
- Alfaro‐Rubio A, Martorell‐Calatayud A, Pelufo C, Terradez L, Hueso‐Gabriel L, GarciaMelgares ML. Mesotherapy granulomas with L‐carnitine. American Academy of Dermatology 71st Annual Meeting. Florida, USA. 1‐5 March 2013. PP‐6919 (Poster).
- Gokdemir G, Küçükünal A, Sakız D. Cutaneous granulomatous reaction from mesotherapy. Dermatol Surg. 2009;35:291‐293.
- Ramos‐e‐Silva M, Pereira AL, Ramos‐e‐Silva S, Piñeiro‐Maceira J. Oleoma: rare complication of mesotherapy for cellulite. Int J Dermatol. 2012;51:162‐167.
- Strahan JE, Cohen JL, Chorny JA. Granuloma annulare as a complication of mesotherapy: a case report. Dermatol Surg. 2008;34:836‐838.
- Park EJ, Kim HS, Kim M, Oh HJ. Histological changes after treatment for localized fat deposits with phosphatidylcholine and sodium deoxycholate. J Cosmet Dermatol. 2013;12:240‐ 243.
- Polat M, Üstün H. A case of mesotherapy‐ induced panniculitis. Cutan Ocul Toxicol. 2016;35:163‐164.
- Tan J, Rao B. Mesotherapy‐induced panniculitis treated with dapsone: case report and review of reported adverse effects of mesotherapy. J Cutan Med Surg. 2006;10:92‐95.
- Davis MD, Wright TI, Shehan JM. A complication of mesotherapy: noninfectious granulomatous panniculitis. Arch Dermatol. 2008;144:808‐809.
- Lee DP, Chang SE. Subcutaneous nodules showing fat necrosis owing to mesotherapy. Dermatol Surg. 2005;31:250‐251.
- Kadry R, Hamadah I, Al‐Issa A, Field L, Alrabiah F. Multifocal scalp abscess with subcutaneous fat necrosis and scarring alopecia as a complication of scalp mesotherapy. J Drugs Dermatol. 2008;7:72‐73.
- El‐Komy M, Hassan A, Tawdy A, Solimon M, Hady MA. Hair loss at injection sites of mesotherapy for alopecia. J Cosmet Dermatol. 2017;16:e28‐e30.
- Duque‐Estrada B, Vincenzi C, Misciali C, Tosti A. Alopecia second‐ ary to mesotherapy. J Am Acad Dermatol. 2009;61:707‐709.
- Schmutz JL, Barbaud A, Trechot P. Alopecia and mesotherapy. Ann Dermatol Venereol. 2010;137:338.
- Rallis E, Kintzoglou S, Moussatou V, Riga P. Mesotherapy‐induced urticaria. Dermatol Surg. 2010;36:1355‐1356.
- Urbani CE. Urticarial reaction to ethylenediamine in aminophylline following mesotherapy. Contact Dermatitis. 1994;31:198‐ 199.
- Vaillant L, de Muret A, Muller C, Machet L, Lorette G. Lichenoid drug eruption after mesotherapy. Ann Dermatol Venereol. 1992;119:936‐937.
- Grojean MF, Vaillant L. Lichenoid eruption caused by mesotherapy. Ann Med Interne. 1995;146:365‐366.
- Babacan T, Onat AM, Pehlivan Y, Comez G, Tutar E. A case of the Behcet’s disease diagnosed by the panniculits after mesotherapy. Rheumatol Int. 2010;30:1657‐1659.
- Rosina P, Chieregato C, Miccolis D, D’Onghia FS. Psoriasis and side‐effects of mesotherapy. Int J Dermatol. 2001;40:581‐583.
- Bessis D, Guilhou JJ, Guillot B. Localized urticaria pigmentosa triggered by mesotherapy. Dermatology. 2004;209:343‐344.
- Colón‐Soto M, Peredo RA, Vilá LM. Systemic lupus erythematosus after mesotherapy with acetyl‐L‐carnitine. J Clin Rheumatol. 2006;12:261‐262.
- Calonge WM, Lesbros‐Pantoflickova D, Hodina M, Elias B. Massive subcutaneous emphysema after carbon dioxide mesotherapy. Aesthetic Plast Surg. 2013;37:194‐197.
- Zaragoza J, Delaplace M, Benamara M, Estève E. A rare side effect of mesotherapy: Nicolau syndrome. Ann Dermatol Venereol. 2013;140:713‐717.
- Vukcević NP, Babić G, Segrt Z, Ercegović GV, Janković S, Aćimović L. Severe acute caffeine poisoning due to intradermal injections: mesotherapy hazard. Vojnosanit Pregl. 2012;69:707‐713. Erratum. In: Vojnosanit Pregl. 2012;69:929.
- Danilovic DL, Bloise W, Knobel M, Marui S. Factitious thyrotoxicosis induced by mesotherapy: a case report. Thyroid. 2008;18:655‐657.
- Kim JB, Moon W, Park SJ, et al. Ischemic colitis after mesotherapy combined with anti‐obesity medications. World J Gastroenterol. 2010;16:1537‐1540.
- Tor PC, Lee TS. Delirium with psychotic features possibly associated with mesotherapy. Psychosomatics. 2008;49:273‐274.
- Moftah N, Moftah N, Abd‐Elaziz G, et al. Mesotherapy using dutasteride‐containing preparation in treatment of female pattern hair loss: photographic, morphometric and ultrustructural evaluation. J Eur Acad Dermatol Venereol. 2013;27:686‐693.
- Brandão C, Fernandes N, Mesquita N, et al. Abdominal haematoma–a mesotherapy complication. Acta Derm Venereol. 2005;85:446.
- Mammucari M, Lazzari M, Maggiori E, et al. Role of the informed consent, from mesotherapy to opioid therapy. Eur Rev Med Pharmacol Sci. 2014;18:566‐574.
Xem thêm:
Trichloroacetic Acid Peels vùng cổ, ngực, cánh tay và bàn tay