Để tải bài viết Các hoạt chất thoa để phục hồi sức khỏe làn da PDF mời các bạn click vào link ở đây.
TOPICAL AGENTS FOR SKIN HEALTH RESTORATION
Các tác giả: Monika G. Kiripolsky, MD, FAAD
Biên dịch: Bs Nguyễn Đức Chánh
GIỚI THIỆU CÁC CHẤT HOẠT THOA
Các bác sĩ da liễu và những người khác tự coi mình là chuyên gia trong lĩnh vực chăm sóc da có thể không giới thiệu cho bệnh nhân những sản phẩm bôi ngoài cần thiết nhất, đã được khoa học chứng minh và có lợi. Một số lý do làm cơ sở cho vấn đề này. Do không có hướng dẫn điều trị duy trì và phục hồi sức khỏe làn da được chuẩn hóa, các bác sĩ được phép quảng cáo các sản phẩm bôi ngoài da dựa trên quan điểm khác nhau của họ và ảnh hưởng của hoạt động tiếp thị trong ngành công nghiệp. Các học viên cũng được hướng dẫn bởi sự thoải mái của bệnh nhân và những mong muốn không dính đáng của họ. Do đó, các bác sĩ lâm sàng không khuyến nghị các sản phẩm có thể gây kích ứng và khiến bệnh nhân khó chịu sau đó (ví dụ: retinoids, chất làm se da).
Khi đánh giá giá trị của một chất bôi ngoài da, các bác sĩ phải phân biệt giữa những công bố đã được khoa học chứng minh và những công bố chỉ mang tính lý thuyết Hơn nữa, nếu thuốc bôi không mang lại hiệu quả có lợi trong một khoảng thời gian tương đối “hạn chế” (ví dụ: 2 đến 3 tháng tương ứng với khoảng hai chu kỳ trưởng thành tế bào sừng đầy đủ), nên ngừng sử dụng. Khung 3.1 giới thiệu tổng quan về cách đánh giá hiệu quả các tác nhân tại chỗ.
Các hướng dẫn phân loại thuốc bôi dựa trên giá trị điều trị của chúng có thể hỗ trợ rất nhiều cho các bác sĩ trong việc đưa ra quyết định dựa trên bằng chứng về các sản phẩm bôi ngoài da. Các thành phần hoạt tính trong các công thức sản phẩm nên được phân loại thành một trong ba loại: thiết yếu, hỗ trợ hoặc nghi vấn (Bảng 3.1). Các tác nhân thiết yếu là trị liệu và chúng chủ yếu hoạt động trong tế bào. Sự đóng góp của chúng trong việc phục hồi sức khỏe làn da tổng thể là không thể phủ nhận và được chứng minh một cách khoa học. Mặt khác, các chất hỗ trợ chỉ có tác dụng điều trị nhẹ. Chúng thường có cơ chế hoạt động ngoại bào và do đó nên được sử dụng kết hợp với các tác nhân thiết yếu. Các tác nhân đang nghi ngờ đã không cho thấy bất kỳ lợi ích nào được khoa học chứng minh. Chúng chỉ nên được sử dụng sau khi đã sử dụng các thuốc hỗ trợ và cần thiết. Lưu ý, khoảng 80% tất cả các loại mỹ phẩm hiện có trên thị trường sử dụng các thành phần hoạt tính được xếp vào danh mục nghi vấn. Cho dù được phân
| Khung 3.1 |
| Đánh giá hoạt chất thoa |
| Khi đánh giá giá trị của thuốc thoa, bác sĩ phải phân biệt giữa những công bố đã được khoa học chứng minh và những công bố chỉ mang lại lợi ích về mặt lý thuyết |
| Bảng 31 Phân loại các tác nhân bôi ngoài da | |
| Phân loại tác nhân | Đặc tính |
| Thiết yếu | Tăng cường tẩy tế bào chết biểu bì tự nhiên |
| Đảm bảo chức năng hàng rào thích hợp bằng cách khôi phục sự cân bằng của nước, lipid và protein | |
| Ổn định sản xuất melanin bởi các tế bào hắc tố | |
| Đảm bảo sự phân bố đều của melanin đến các tế bào sừng xung quanh | |
| Tăng cường sức sống cho da qua việc kích thích liên tục quá trình sửa chữa/ sản xuất collagen và elastin | |
| Đảm bảo đủ độ ẩm thông qua sản xuất glycosaminoglycan | |
| Giảm thiểu tình trạng viêm mãn tính (ví dụ: thông qua việc giảm bã nhờn) và tạo ra các gốc tự do | |
| Sửa chữa DNA bị hư hỏng | |
| Hỗ trợ | Điều trị nhẹ và nên được sử dụng kết hợp với các chất thiết yếu |
| Nghi vấn | Chưa cho thấy bất kỳ lợi ích điều trị được chứng minh khoa học nào |
| Giá trị trong việc điều hòa da còn nhiều nghi vấn | |
loại là cần thiết, hỗ trợ hay nghi vấn, mỗi công thức bôi ngoài da có thể được phân loại thêm theo cơ chế hoạt động của các thành phần hoạt tính của nó.
Ví dụ về những thay đổi cần thiết và hỗ trợ được trình bày trong Bảng 3.2. Các tác nhân có thể nghi vấn, là tùy chọn, bao gồm các chất sau: vàng, bạch kim, trứng cá muối, tơ tằm, axit ursolic, Planifolia PFA và chiết xuất Imperiale Orchidee. Có vẻ như vô tận các tác nhân đáng nghi vấn đang được sử dụng trong các sản phẩm chăm sóc da hiện có trên thị trường. Một danh sách đầy đủ các tác nhân này sẽ không chỉ không phù hợp với giới hạn của cuốn sách này mà còn không liên quan vì chúng không cho thấy lợi ích khoa học trong các quy trình phục hồi hoặc duy trì sức khỏe làn da.
| Bảng 3.2 Ví dụ về các tác nhân hỗ trợ và cần thiết | |
| Tác nhân cần thiết | Tác nhân hỗ trợ |
| Các dẫn xuất vitamin A (tretinoin và retinol) | Alpha-hydroxy acids (glycolic, lactic, and malic acids) |
| Hydroquinone | Beta-hydroxy acids (salicylic acid) |
| Antioxidants (a-lipoic acid, glutathione, ubiquinone, idebenone, vitamin C, vitamin E, vitamin B3) | Chất ổn định sắc tố nonhydroquinone (axit kojic, azelaic acid, arbutin, resorcinol) |
| Các chất sửa chữa DNA (oxo-guanine glycosylase, tia cực tím endonuclease, photolyase, và các tiền chất DNA tự nhiên bao gồm Unirepair T-43) | Thuốc đặc trị (5-fluorouracil, imiquimod, benzoyl peroxide, kháng sinh kháng nấm thoa) |
| Các chất kháng viêm | |
| Growth factors (yếu tố tăng trưởng) | |
LỰA CHỌN HOẠT CHẤT THOA
Các bác sĩ và các chuyên gia chăm sóc da khác thường khuyên dùng các loại thuốc bôi ngoài da có thành phần hoạt tính chậm nhưng mang lại cảm giác thoải mái và hài lòng nhanh chóng cho bệnh nhân. Với chế độ khắt khe, các học viên không muốn đối phó với các phản ứng bất lợi từ các chất bôi ngoài, ngay cả khi những phản ứng dự kiến này là cần thiết để đạt được sự Phục hồi Sức khỏe Da. Hơn nữa, các bác sĩ da liễu thường được các công ty chăm sóc da tuyển dụng để quảng bá sản phẩm của họ. Do đó thuật ngữ bác sĩ da liễu đã thử nghiệm. Mỗi năm, nhiều nghiên cứu vô nghĩa được thực hiện theo kiểu này, với các bác sĩ nghiên cứu chính được các công ty dược trả tiền hậu hĩnh cho những công việc này.
Bệnh nhân có xu hướng tìm kiếm một chương trình chăm sóc da dựa trên các khuyến nghị từ bác sĩ da liễu và chuyên gia thẩm mỹ của họ. Hoạt động tiếp thị và quảng cáo của công ty dược phẩm cũng có ảnh hưởng. Cách tiếp cận này có sự thiên vị và thường hướng đến các sản phẩm tạo ra sự hài lòng tức thì nhất cho bệnh nhân và lợi nhuận cho các công ty dược phẩm.
Tốt nhất, trước khi bắt đầu bất kỳ chương trình chăm sóc da nào, bệnh nhân nên tự nghiên cứu và phân tích các thành phần thuốc. Điều này có thể đảm bảo rằng chỉ những sản phẩm được chứng minh là có lợi, điều trị và phù hợp cụ thể với loại da và nhu cầu của bệnh nhân. Nhưng với quá nhiều thông tin không rõ ràng và sai lệch, nhiệm vụ này có thể là khó khăn. Để hỗ trợ bệnh nhân lựa chọn và có thể khuyến họ không sử dụng các sản phẩm chưa được chứng minh với các thành phần hoạt tính trơ, các bác sĩ phải có khả năng tham gia và đưa ra lời khuyên dựa trên khoa học. Cần giải thích rằng những sản phẩm này mang lại sự hài lòng nhanh chóng (thông qua nhìn, ngửi và cảm thấy dễ chịu) nhưng không mang lại lợi ích rõ ràng hoặc lâu dài. Cần phải nhấn mạnh thêm rằng các đặc tính dễ chịu không nhất thiết phải tương quan với việc cải thiện làn da. Những sản phẩm mang lại sự thoải mái này cuối cùng lại phản tác dụng, da bị suy yếu do rối loạn chức năng hàng rào, và các đặc tính tăng sinh cơ bản bị cản trở. Hơn nữa, bệnh nhân nên lưu ý rằng hầu hết các sản phẩm chống lão hóa trên thị trường hiện nay đều vô dụng và thành phần hoạt chất của chúng không hiệu quả, nồng độ quá thấp hoặc phân tử quá lớn để thâm nhập vào da và đạt được mục tiêu đã định.
CÁC CHẤT THIẾT YẾU
Các chất cần thiết là nền tảng để phục hồi sức khỏe làn da. Những chất này đã được khoa học chứng thực là có hoạt tính thật sự và chúng là những chất duy nhất được biết đến có thể trả lại làn da về trạng thái ban đầu tốt nhất có thể. Đánh giá toàn diện về các đặc điểm của chúng được đưa ra trong Bảng 3.1.
Thuốc thoa trong danh mục thiết yếu phải cung cấp một hoặc nhiều tính năng hoạt động nội bào, hiệu quả điều trị, lợi ích chống viêm, kích hoạt chức năng tế bào hoặc cải thiện hàng rào chức năng. Các sản phẩm này, rất quan trọng để đạt được sự phục hồi sức khỏe làn da và duy trì thành công, bao gồm các dẫn xuất vitamin A (tretinoin và retinol), hydroquinone (HQ), chất chống oxy hóa, chất sửa chữa DNA, chất chống viêm và các yếu tố tăng trưởng (Bảng 3.2)
TRETINOIN (RETINOIC ACID)
Tretinoin (axit retinoic) có tác động có lợi sâu sắc đến lớp sừng và các lớp sâu hơn của da. Nó có một cơ chế hoạt động nội bào, với tác động trực tiếp lên các thụ thể tại nhân. Bằng cách kích thích biểu hiện gen và điều chỉnh các chức năng tế bào, nó cuối cùng mang lại lợi ích điều trị mạnh mẽ cho vô số tình trạng da. Đáng chú ý nhất, keratin được làm mềm hơn, và lớp sừng trở nên mịn và săn chắc. Những tác dụng này kéo dài đến 4 tháng, ngay cả sau khi ngừng sử dụng. Điều này trái ngược với tác dụng nhẹ nhàng, ngắn hơn của axit alpha-hydroxy (AHA).
Ban đầu, tretinoin làm mất nước bề mặt ngoài của lớp sừng trong khi vẫn giữ nguyên các desmomes. Điều này dẫn đến việc tẩy da chết nhanh, thô và làm bong tróc một nhóm tế bào kèm theo. Điều này trái ngược với việc bong của các tế bào riêng lẻ, như xảy ra với AHA khi các desmosomes bị phân tách. Tretinoin là tác nhân được ưa thích để điều trị lớp sừng và các rối loạn tập trung ở các lớp sâu hơn của biểu bì vì nó sửa chữa các tế bào sừng bị hư hỏng, tăng quá trình phân bào tế bào đáy và phục hồi độ ẩm đầy đủ.
Tretinoin đã được sử dụng rộng rãi như một phương pháp điều trị tại cho hiệu quả đối với một số bệnh da liễu, bao gồm cả lão hóa. Hiệu quả của nó trong việc cải thiện tình trạng này lần đầu tiên được chứng minh bởi Kligman và các đồng nghiệp vào năm 1984. Các tác giả quan sát thấy rằng việc điều trị da chuột lão hóa với tretinoin trong 10 tuần dẫn đến một vùng phục hồi đáng kể của collagen mới trong lớp bì nhú. Điều này cũng tương quan đến hiệu ứng cải thiện nếp nhăn.
Tretinoin bôi ngoài da đã cho thấy hiệu quả hơn nữa trong việc cải thiện các dấu hiệu lão hóa (cả nội, ngoại sinh), bao gồm các nếp nhăn mảnh, tăng sắc tố và rãnh nhăn. Hiệu quả cũng đã được ghi nhận về mặt mô học. Một nghiên cứu với 0,025% tretinoin được áp dụng cho da có tuổi về bản chất cho thấy sự gia tăng độ dày biểu bì và mật độ tế bào sừng đồng đều hơn. Những thay đổi trên da bao gồm sự gia tăng lắng đọng glycosaminoglycan, sợi đàn hồi và tân tạo mạch. Nghiên cứu so sánh trên phương tiện cho thấy những thay đổi về mặt lâm sàng và mổ học tương tự khi tretinoin 0,1% và 0,025% được sử dụng ở những bệnh nhân lão hóa. Những thay đổi về mô học bao gồm dày lớp biểu bì, tăng độ dày lớp hạt, săn chắc lớp sừng, tăng mạch máu và giảm hàm lượng melanin. Một nghiên cứu sâu hơn cho thấy những thay đổi trong các thành phần nến da bao gồm tân tạo collagen. Ở đây, điều trị được tiếp tục sau 24 tháng, và chỉ có tổ chức collagen tiếp tục cải thiện trong khi độ đàn hồi giảm hơn nữa. Sự gia tăng sản xuất liên tục mucin biểu bì và bì đi cùng việc giảm sự hình thành hắc tố biểu bì cũng nhất quán trong suốt thời gian điều trị.
Nồng độ tretinoin có mối tương quan trực tiếp với hoạt tính có lợi của nó; nồng độ càng cao, tác dụng của nó càng sâu và mạnh hơn. Nồng độ thấp hơn (<0,025%) chủ yếu có lợi cho biểu bì, trong khi nồng độ cao hơn (0,05% đến 0,1%) có tác dụng cả biểu bì và hạ bì. Phương tiện vận chuyển tretinoin cũng ảnh hưởng đến hiệu lực của nó. Các phương tiện bổ sung các thành phần dưỡng ẩm vào công thức sẽ làm suy yếu hoạt động và lợi ích của tretinoin, bất kể nồng độ.
Sử dụng retinoid (tretinoin và retinol) có liên quan đến tình trạng khô da, ban đỏ và tróc da. Những yếu tố này đôi khi có thể hạn chế sự tuân thủ của bệnh nhân. “Phản ứng retinoid” dự đoán thay đổi theo nồng độ và tần suất sử dụng: Nồng độ càng cao và tần suất sử dụng càng nhiều thì càng có nhiều kích ứng dự kiến xảy ra. Những phản ứng này thường biểu hiện trong vài tuần đầu điều trị, nguyên nhân là giải phóng các cytokine tiền viêm. Khi da được điều trị bắt đầu thích ứng với việc sử dụng sản phẩm, các dấu hiệu và triệu chứng liên quan sẽ giảm dần. Nhạy cảm với ánh sáng là một tác dụng phụ đáng chú ý khác liên quan đến liệu pháp retinoid, và thông thường, nó phải được đề cập là khi bắt đầu điều trị. Để chống lại điều này, những bệnh nhân sử dụng retinoid tại chỗ được khuyên nên tránh tiếp xúc với ánh nắng mặt trời quá nhiều, sử dụng kem chống nắng phổ rộng và mặc quần áo chống nắng Khung 3.2 cho thấy tác dụng của tretinoin.
Bệnh nhân có thể tiếp tục sử dụng tretinoin tại chỗ cho mục đích duy trì. Trong trường hợp đó, tretinoin phải được áp dụng hai đến ba lần mỗi tuần và một sản phẩm có retinol được sử dụng vào những ngày còn lại. Ngoài ra, bệnh nhân có thể chuyển sang bôi thuốc retinol hàng ngày để duy trì và sửa chữa cụ thể. Lựa chọn đầu tiên đôi khi được dùng để duy trì làn da với mục tiêu ngăn ngừa bệnh lý (ví dụ: nám, mụn trứng cá, trứng cá đỏ). Tuy nhiên, lựa chọn thứ hai được ưu tiên hơn, đặc biệt là ở những bệnh nhân không có bệnh da cơ bản, vì lợi ích phòng ngừa và chống lão hóa hàng ngày.
Lý do cho những chỉ định này là tretinoin phục vụ hai chức năng: điều trị. và kích thích. Điều thứ nhất được hoàn thành sau 18 tuần sử dụng sản phẩm, và sau đó thứ hai chiếm ưu thế. Bệnh nhân không thể dung nạp được tretinoin và da của họ vẫn đỏ, khô và tróc da trong thời gian dài. Trạng thái kích ứng này là không thuận lợi, vì vậy nên ngừng sử dụng tretinoin sau khung thời gian 18 tuần. Retinol thay vào đó nên được sử dụng cho các mục đích duy trì; nó không liên quan đến kích ứng lâu dài vì da thường dung nạp thành công với tác nhân này.
| Khung 3.2 |
| Tác dụng của Tretinoin |
| Tretinoin có tác động có lợi sâu sắc đến lớp sừng và các lớp sâu hơn của da. |
Trong lớp biểu bì, tretinoin:
|
Trong lớp bì, tretinoin:
|
| Nồng độ thấp hơn (<0,025%) của tretinoin có tác dụng chủ yếu trên biểu bì, trong khi nồng độ cao hơn (0,05% đến 0,1%) tạo ra lợi ích cả biểu bì và bì. |
RETINOL
Retinol, giống như tretinoin, là một dẫn xuất của vitamin A, Cả hai đều là những thành phần phổ biến nhất được tìm thấy trong các sản phẩm chăm sóc da theo toa và không kê đơn. Chúng là những thành phần được nghiên cứu thường xuyên và có nhiều thông tin nhất về hiệu quả của chúng trong việc chăm sóc da.
Trong da, retinol đầu tiên bị oxy hóa thành retinaldehyde và sau đó thành tretinoin, dạng hoạt động sinh học của vitamin A. Retinol bôi tại chỗ (ở nồng độ lên đến 1,6%) đã được chứng minh là có các tác dụng có lợi tương tự như tretinoin (với nồng độ 0,025%). Đặc biệt, retinol bôi tại chỗ làm giảm sự xuất hiện của các nếp nhăn thông qua việc tăng sản xuất glycosaminoglycans (giữ lại lượng nước đáng kể) và collagen. Tuy nhiên, mặc dù thể hiện tác dụng có lợi tương tự như tretinoin, retinol tại chỗ chỉ tạo ra các dấu hiệu kích ứng và ban đỏ nhỏ nhất. Cụ thể hơn, retinol đã được chứng minh là ít gây bong vảy, mất nước qua biểu bì và ban đỏ hơn so với tretinoin.
Retinol, mặc dù cuối cùng được chuyển đổi trong da thành tretinoin (một sản phẩm kê đơn), vẫn có sẵn không cần kê đơn. Tuy nhiên, độ mạnh của retinol và tretinoin không thể so sánh được. Các sản phẩm retinol bôi ngoài da thường chứa nồng độ từ 1% trở lên, nhưng tretinoin hiếm khi có trên 0,1%. Điều quan trọng cần lưu ý là retinol có tác dụng kém hơn tretinoin khoảng 20 lần (Khung 3.3). Do đó, nồng độ retinol 1% tương đương với nồng độ 0,05% của tretinoin. Hơn nữa, khi xác định hiệu quả, phải xem xét loại chất dân vận chuyển retinol tại chỗ. Retinol cực kỳ không ổn định vì nó bị phân hủy thành dạng không hoạt động sinh học khi tiếp xúc với không khí và ánh sáng
HYDROQUINONE
HQ là một chất làm sáng da có nguồn gốc từ phenol. Nó thường được sử dụng trong thực hành da liễu để điều trị các tình trạng tăng sắc tố da, bao gồm nám da, tàn nhang, đồi mồi và tăng sắc tố sau viêm (PIH). HQ hoạt động bằng cách ức chế enzym tyrosinase, cần thiết để chuyển đổi dihydroxyphenylalanin (DOPA) thành melanin. Hoạt động của tyrosinase có thể giảm tới 90% khi sử ( dụng HQ. HQ cũng có thể phân hủy melanosomes và gây độc có chọn lọc đến tế bào hắc tố. Nó đạt được điều này thông qua việc thay đổi cấu trúc các bào quan của tế bào hắc tố, do đó làm giảm sản xuất melanosome và tăng sự phân hủy của chúng. Vì HQ chỉ ngăn chặn sự hình thành các hắc tố mới (từ các tế bào hắc tố nằm trong hoặc gần lớp đáy) nên da không thể sáng lên ngay lập tức
| Khung 3.3 |
| Hiệu lực của Retinol |
| Retinol ở nồng độ 1% xấp xỉ với nồng độ từ 0% đến 0,05% của tretinoin. |
HQ có sẵn ở dạng lotion, kem, chất lỏng hoặc gel. Các loại lotion và kem cáợc ưu tiên hơn vì dạng lỏng và gel dẫn đến việc thoa không đều. Điều quan trọng cần lưu ý là sau khi chế phẩm HQ đã bị oxy hóa và chuyển sang màu nâu, nó có rất ít hoặc không có hoạt tính.
HQ có bán tại quầy với nồng độ 2% và trong thuốc bôi kê đơn với nồng độ từ 3% đến 5%. Nồng độ cao hơn (6% đến 8%) da không được chứng minh là có hiệu quả hơn và làm tăng nguy cơ gây ra phản ứng đặc trưng trong hoặc sau khi ngừng điều trị (tương tự như ochronosis). Đôi khi, các hiệu thuốc sẽ kết hợp HQ tại chỗ với nồng độ cao tới 20% để điều trị cụ thể các tình trạng như bạch biến phổ quát. Tuy nhiên, việc sử dụng HQ với cường độ lớn hơn 4% thường không được khuyến khích vì chúng có liên quan đến việc tăng nguy cơ sạm da nghịch lý (Ochronosis ngoại sinh), có thể là vĩnh viễn. Ochronosis ngoại sinh biểu hiện dưới dạng các khoảng da màu xanh đen và nó phổ biến hơn ở những người da đen có nguồn gốc bộ lạc nhất định. Tuy nhiên, nó có thể xảy ra ở bất kỳ màu da hoặc loại da nào.
Việc sử dụng HQ được khuyến nghị được giới hạn trong khoảng thời gian 4 hoặc 5 tháng. Sử dụng kéo dài thậm chí với cường độ thấp hơn của HQ có thể gây độc cho tế bào và có liên quan đến tăng nguy cơ mắc Ochronosis ngoại sinh. Ở những bệnh nhân có biểu hiện của ochronosis ngoại sinh, hiệu quả thường có thể đạt được bằng cách cho bệnh nhân sử dụng HQ để tẩy trắng và pha trộn, cùng với peel trung bình và một loạt điều trị laser Nd: YAG.
Các tác dụng phụ hiếm gặp khác liên quan đến việc sử dụng HQ là châm chích, bỏng rát, kích ứng, phản ứng giống phát ban và viêm da tiếp xúc dị ứng. Sự hấp thu toàn thân hoặc độc tính do sử dụng HQ tại chỗ kéo dài (ở nồng độ 2% đến 4%) chưa được báo cáo. Ngay cả khi vô tình nuốt phải, HQ hiếm khi tạo ra độc tính toàn thân. Điều này trái ngược với các chất làm trắng được sử dụng trước đây, chẳng hạn như các hợp chất thủy ngân, gây tổn thương thận và mono-benzone, gây phá hủy tế bào hắc tố vĩnh viễn. Việc tăng nguy cơ ung thư da chưa được ghi nhận khi sử dụng HQ. Ngoài ra, HQ không trực tiếp gây ra tăng độ nhạy sáng. Tuy nhiên, lượng melanin giảm xuống sẽ cho phép da hấp thụ nhiều tia cực tím (UV) hơn. Điều này dẫn đến tổn thương ánh nắng mặt trời mãn tính. Do đó, chống nắng phổ rộng, ưu tiên loại vật lý, được khuyến khích sử dụng khi dùng HQ.
Để có kết quả tối ưu, với mỗi lần thoa, bệnh nhân nên thoa khoảng 1,5 gam HQ vào lớp biểu bì (tương tự như lượng trong 1 inch kem đánh răng). Lượng này cần được mát xa hoàn toàn vào da. Sau khi sử dụng HQ, độ pH của da sẽ chuyển sang trung tính, do đó tạo điều kiện thuận lợi cho quá trình oxy hóa của sản phẩm. Do hiện tượng này, hoạt động của HQ tương đối ngắn, và do đó nó nên được sử dụng hai lần mỗi ngày. Khi màu da đồng đều, tần suất sử dụng có thể giảm dần. Không nên dừng sử dụng đột ngột.
Mặc dù HQ là một chất khử màu mạnh, nhưng hiệu quả của nó có thể được tăng cường khi nó được sử dụng kết hợp với AHA, tretinoin hoặc cả hai. Sự hiện diện của AHA trong các sản phẩm có chứa HQ cũng ngăn chặn quá trình oxy hóa sau này, do đó duy trì hoạt động của nó. Vì HQ tương đối không ổn định, khi kết hợp nó với tretinoin, hai sản phẩm nên được kết hợp ngay trước khi bôi lên da. Sự thâm nhập của HQ cũng có thể được tăng lên bằng cách kết hợp nó với các tác nhân khác (ví dụ, axit azelaic) và bằng cách điều chỉnh độ pH của da trước trị liệu.
Cần lưu ý, quá trình tăng cường độ thẩm thấu nói trên hoàn toàn khác với trạng thái tăng độ thấm. Sự thâm nhập của các thành phần hoạt tính của sản phẩm có thể được tăng cường bằng cách sử dụng nó cùng với một chất bôi” ngoài da khác (như khi chúng ta đang điều trị bệnh). Ngược lại, sự gia tăng tính thẩm của biểu bì là một rối loạn đặc trưng bởi chức năng hàng rào biểu bà bị tổn thương. Điều này dẫn đến khô da, nhạy cảm, kích ứng và suy giảm khả năng hồi phục. Hơn nữa, khi sử dụng HQ, da dầu phải được lưu ý và giảm bớt. Da nhờn cần được nửa đúng cách và sử dụng thêm các chất bôi ngoài da hoặc toàn thân. Cả hai đều hỗ trợ giảm bã nhờn và cho phép tăng độ thâm nhập của HQ.
Việc sử dụng kết hợp HQ và tretinoin trong ít nhất 6 tuần là điều cần thiết trước khi thực hiện một quy trình như ZO Controlled Depth Peel (20% hoặc 26% đến 28% axit trichloroacetic [TCA]). Việc ổn định da trước này làm giảm khả năng sản xuất melanin của da và do đó làm giảm nguy cơ phát triển PIH, Sự kết hợp HQ và tretinoin tiếp tục tăng cường độ ẩm cho da, mang lại kết quả đồng đều hơn vì nước là đối tượng chính cho hoạt chất peel tác động.
Melamin (HQ 4%, ZO Medical), khi được sử dụng một mình, có thể giảm thiểu hầu hết các vấn đề về tăng sắc tố do sự gia tăng hoạt động của các tế bào hắc tố và sản xuất quá nhiều hắc tố của chúng. Trong trường hợp này, việc ức chế quá trình sản xuất melanin được gọi là tẩy trắng. Tuy nhiên, khi HQ được trộn với tretinoin hoặc AHAs, tác dụng tẩy trắng trở nên kém hấp dẫn hơn và một tác dụng khác sẽ được ưu tiên. Thuật ngữ pha trộn đề cập đến quá trình này, tạo sự phân bố melanin đồng đều hơn cho các tế bào sừng xung quanh.
Để có kết quả nhanh hơn, hiệu quả hơn, nên kết hợp cả hai bước. Bước tẩy trắng phải được thực hiện đầu tiên, sau đó là pha trộn. Khi một sản phẩm kết hợp HQ (Melamix, 4% HQ, ZO Medical) được dự định kết hợp với một sản phẩm khác có chứa tretinoin (cho mục đích pha trộn), chất dẫn HQ phải có độ pH có tính axit cao hơn để cho phép trộn hiệu quả với tretinoin. Điều này trái ngược với các sản phẩm chỉ chứa HQ loại cơ bản hơn và dành cho mục đích tẩy trắng. Do tác dụng ức chế tẩy trắng và pha trộn, các sản phẩm HQ bôi ngoài da có chứa steroid cũng nên tránh. Khung 3.4 trình bày tổng hợp các đặc tính và tác dụng của hydroquinone.
CHẤT CHỐNG OXY HÓA
Chất chống oxy hóa là những phân tử ức chế sự oxy hóa của các phần tử xung quanh. Quá trình oxy hóa liên quan đến việc chuyển các electron hoặc hydro từ phân tử này sang phân tử khác, là chất bị oxy hóa. Phản ứng hóa học này dẫn đến việc sản xuất các gốc tự do. Những phản ứng này kích hoạt chuỗi phản ứng nội bào và cuối cùng, tổn thương tế bào hoặc chết tế bào, Chất chống oxy hóa, thông qua quá trình oxy hóa ưu tiên của chúng,
ngăn chặn phản ứng dây chuyền này. Các gốc tự do vì vậy đã bị loại bỏ, và các phản ứng oxy hóa tiếp theo bị chấm dứt.
Tình trạng viêm gây ra sự suy giảm collagen và các chất chống oxy hóa giúp ức chế quá trình này. Chúng cũng bảo vệ chống lại tổn thương do ánh sáng cấp tính, mãn tính và ung thư da. Các chất chống oxy hóa bôi ngoài da phổ biến nhất bao gồm: axit alpha-lipoic, glutathione, idebenone, ubiquinone, vitamin C (axit L-ascorbic), vitamin E (tocopherol) và vitamin B3 (niacinamide).
| Khung 3.4 |
| Tóm tắt Hydroquinone |
| Hydroquinone (HQ) ngăn chặn sự hình thành hắc tố mới bằng cách ức chế enzym tyrosinase. |
| HQ có bán tại quầy với nồng độ 2% và trong thuốc kê toa với nồng độ từ 3 đến 5% |
| Ở nồng độ trên 4%, HQ có thể gây sạm da ngược (ochronosis ngoại sinh), có thể tồn tại vĩnh viễn. |
| Hiệu quả của HQ có thể được nâng cao khi được sử dụng kết hợp với axit alpha-hydroxy (AHA), tretinoin hoặc cả hai. |
| Tẩy trắng là việc sử dụng HQ để ngăn chặn sự sản sinh quá mức của melanin |
| Pha trộn là HQ được trộn với tretinoin hoặc AHAs để có được sự phân bổ melanin đồng đều hơn đến các tế bào sừng xung quanh. |
| Nên kết hợp tẩy và trộn để có hiệu quả nhanh hơn. |
| Để giảm nguy cơ tăng sắc tố sau viêm, nên sử dụng HQ và tretinoin trong khoảng 6 tuần trước khi thực hiện thủ thuật. |
Alpha-Lipoic Acid
Axit alpha-lipoic (ALA), được tạo ra trong ty thể của động vật và thực vật, hoạt động như một chất chống oxy hóa mạnh. Nó bảo vệ các tế bào khỏi tia UV và các tác hại do các gốc tự do khác được tạo ra từ môi trường. Nhờ khả năng hòa tan trong cả lớp nước và lớp lipid, ALA thâm nhập nhanh chóng qua lớp biểu bì để đến lớp bì và lớp dưới da. Mặc dù hầu hết ALA tự do được chuyển đổi nhanh chóng (giảm) thành axit dihydro-lipoic (DHLA), cả ALA và DHLA đều là chất chống oxy hóa hiệu quả cao. Giống như ALA, DHLA hoạt động như một bộ lọc các loại oxy phản ứng (ROS). DHLA cũng đã được chứng minh là có khả năng sửa chữa các protein bị hư hỏng do oxy và tái tạo các chất chống oxy hóa nội sinh như glutathione, ubiquinol, vitamin E và vitamin C. Hơn nữa, cả ALA và DHLA hoạt động như chất trung gian chống viêm thông qua việc loại bỏ ROS do đại thực bào và bạch cầu tiết ra tại các vị trí viêm nhiễm.
Glutathione
Một peptide chứa cysteine được tìm thấy trong hầu hết các dạng sống hiếu khí, glutathione là một chất chống oxy hóa nội bào mạnh vì nhóm thiol của nó (trong gốc cysteine). Hợp chất này chủ yếu hoạt động như một chất khử, loại bỏ ROS, Glutathione cũng đóng vai trò như một chất đồng vận chống oxy hóa, trong đó nó hỗ trợ vitamin E và axit L-ascorbic.
Ubiquinone (Coenzyme Q10)
Ubiquinone, có chức năng vừa là chất chống oxy hóa vừa là chất tạo năng lượng, có mặt ở hầu hết các tế bào sống (ngoại trừ một số loại nấm và vi khuẩn). Ubiquinone đã được chứng minh là làm giảm tổn thương DNA oxy hóa do tia UV gây ra trong tế bào sừng. Nó cũng được chứng minh là làm giảm sự suy thoái collagen do tia UV tạo ra thông qua khả năng ngăn an quá trình sản xuất collagenase của nguyên bào sợi. Hơn nữa, ubiquinone bôi tại chỗ làm giảm sự mất axit hyaluronic (một glycosamznoglycan được tạo ra bởi nguyên bào sợi) và làm chậm quá trình phân chia tế bào, cả hai đều góp. phần vào quá trình lão hóa nội sinh. Do đó, ubiquinone là một chất chống oxy hóa tại chỗ quan trọng vì nó bảo vệ lớp bì khỏi cả lão hóa nội sinh hay ngoại sinh.
Idebenone
Idebenone, một chất tương tự được tổng hợp của ubiquinone, hoạt động như một chất chống oxy hóa căn bản mạnh. Nghiên cứu lâm sàng đánh giá lợi ích tại chỗ của nó cho thấy khả năng loại bỏ gốc tự do toàn diện hơn so với các chất chống oxy hóa truyền thống khác (ALA, tocopherol và axit ascorbic). Các nghiên cứu in vivo về Idebenone thoa đã cho thấy giảm quá trình peroxy hóa lipid và ức chế tổn thương DNA, ban đỏ do tia UVB gây ra. Nghiên cứu cũng cho thấy rằng Idebenone được sử dụng tốt nhất khi kết hợp với các chất chống oxy hóa khác. Điều này là do nó thiếu tác dụng bảo vệ quang học, có trong một số chất chống oxy hóa tại chỗ khác.
Vitamin C (L-Ascorbic Acid)
Dạng sinh khả dụng duy nhất của Vitamin C, axit L-ascorbic, cũng là dạng duy nhất cung cấp lợi ích chống oxy hóa của phân tử. Khi thoa tại chỗ, axit L-ascorbic đóng vai trò như một chất chống oxy hóa đa chức năng, dập tắt ROS được tạo ra trong môi trường nước của da. Sự ổn định thích hợp công nghệ encapsule và chất dẫn khan hoặc este hóa) của thuốc bôi chứa vitamin C là rất quan trọng vì axit L-ascorbic dễ bị oxy hóa. Khi bào chế base nước, phương pháp ưu tiên, các sản phẩm bôi ngoài da chứa axit L-ascorbic phải có độ pH từ 3,5 trở xuống. Mặc dù các phiên bản ester của vitamin C (như magie ascorbyl phosphate và ascorbyl palmitate) đã cho thấy một số khả năng chống oxy hóa trong các nghiên cứu lâm sàng, chúng không cung cấp các hoạt động tổng hợp collagen, kháng viêm và chống nắng. Do đó, ester hóa không phải là phương pháp ổn định ưu tiên so với các chế phẩm encapsule hoặc khan.
Vitamin E (a-Tocopherol)
Vitamin E là chất chống oxy hóa ưa mỡ dồi dào nhất được tìm thấy trong da. Tocopherol, bao gồm bốn nhóm phụ khác nhau (alpha-, beta-, gamma và delta-tocopherol), là dạng vitamin E dồi dào nhất trong cơ thể. Alphatócopherol là dạng vitamin E chính có trong da; các chế phẩm tại chỗ thấm qua cả biểu bì và hạ bì. Sau khi thoa, vitamin E sẽ tích tụ trong màng tế bào và trong chất nền lipid ngoại bào của lớp sừng. Ở đây, nó đóng góp vào lợi ích chống oxy hóa. Vì nó làm giảm ROS và do đó bảo vệ màng tế bào khỏi quá trình peroxy hóa lipid bởi các gốc tự do, vitamin E được xếp vào nhóm chất chống oxy hóa. Ngoài ra, vitamin E có thể hấp thụ năng lượng từ tia UV. Điều này cho phép nó được xem là một chất chống nắng vì về sau nó ngăn ngừa tổn thương da do các gốc tự do gây ra bởi tia cực tím.
Alpha-tocopherol cũng có sẵn dưới dạng dẫn xuất este, giúp tăng tính ổn định khi tiếp xúc với không khí, ánh sáng và nhiệt. Hàm lượng vitamin E trong da giảm khi tiếp xúc với tia UV, ozone và tuổi tác. Vitamin E bôi tại chỗ cá được nghiên cứu ở các nồng độ khác nhau, thường từ 0,1% đến 1%. Ngay cả với các dung dịch chứa nồng độ thấp tới 0,1%, nồng độ vitamin E cũng tăng lên trong da. Tuy nhiên, các nghiên cứu so sánh sự tích lũy phụ thuộc vào liều lượng của vitamin E và hiệu quả của nó về lợi ích chống oxy hóa còn thiếu.
Vitamin B3 (Niacinamide)
Vitamin B3, một chất chống oxy hóa mạnh, làm giảm sự mất nước qua lớp biểu bì, do đó cải thiện chức năng hàng rào lipid của lớp biểu bì. Điều thú vị là, vitamin B3 cũng làm giảm sự xuất hiện của chứng tăng sắc tố bằng cách ức chế quá trình vận chuyển của melanosome. Các nghiên cứu đánh giá tác dụng của vitamin B3 bôi tại chỗ cũng cho thấy sự cải thiện đáng kể về nếp nhăn mảnh, rãnh nhăn và độ đàn hồi của da. Thuộc tính của chất chống oxy hóa được hiển thị trong Khung 3.5.
Chất sửa chữa DNA
Tiếp xúc nhiều lần với tia UVA và UVB gây ra hiện tượng mỏng da, ban đỏ cấp tính, nếp nhăn và sắc tố mãn tính. Những biểu hiện bên ngoài này phản ánh tổn thương cấp độ phân tử đối với chuỗi xoắn kép DNA nằm trong nhân tế bào. Một ví dụ về tổn thương DNA liên quan đến tia UVB là sự hình thành các chất dimer cyclobutane Pyrimidine (CPDs). Đây là những đột biến được hình thành giữa các gốc pyrimidine liên kết trên cùng một sợi DNA, CPD làm thay đổi chức năng của DNA và gây ra các đột biến tế bào, tạo khối u và gây chết tế bào. Hơn nữa, với sự lão hóa theo trình tự thời gian, các cơ chế sửa chữa DNA bẩm sinh giảm xuống, dẫn đến nguy cơ đột biến cao. Tiếp xúc với tia cực tím tiếp tục gây ra sự hình thành ROS. Protein là một trong những mục tiêu chính cho quá trình oxy hóa qua trung gian ROS này. Không còn chức năng, các protein bị oxy hóa hoặc được sửa chữa, loại bỏ bằng cách xuất bào, hoặc bị phân hủy bằng cách phân giải protein thành các axit amin và peptit.
Ngoài tổn thương DNA tế bào, việc tiếp xúc mãn tính với tia UVA và UVB dẫn đến tăng biểu hiện của ma trận metalloproteinase (MMPs) thường liên quan đến lão hóa da nội sinh. Do đó, lão hóa ngoại sinh dẫn đến DNA bị hư hồng và tăng sản xuất MMP. Các yếu tố liên quan đến việc tạo ra những thay đổi này bao gồm stress oxy hóa (hạt nhân và ty thế), tiếp xúc với tia cực tím, glycation và alkyl hóa. Được áp dụng tại chỗ, các phức hợp enzym phục hồi DNA, loại bỏ, chiết xuất và sửa chữa DNA bị hư hỏng bởi nhiều tư nhân
| Box 3.5 |
| Antioxidants |
| Oxidation involves the transfer of electrons or hydrogen from one molecule to another, the oxidizing agent. This chemical reaction leads to the production of free radicals. These trigger intracellular chain reactions that produce cell damage. |
| Antioxidants, through being oxidized themselves, remove free radi cals. Further oxidation reactions are thereby terminated. |
| Alpha-lipoic acid, glutathione, idebenone, ubiquinone, vitamin C, vitamin E, and vitamin B, are all potent topical antioxidants in human skin. |
Oxo-Guanine Glycosylase-1 (OGG-1)
Oxo-guanine glycosylase-1 (OGG-1) là một loại enzyme sửa chữa DNA bị hư hỏng do stress oxy hóa. Để thâm nhập hiệu quả vào lớp biểu bì, OGG-1 có thể được bao bọc trong các liposome nhạy cảm với pH. Phản ứng viêm do tiếp xúc với UVB dẫn đến sự hình thành các sản phẩm phụ DNA oxy hóa như 8-hydroxy-2-deoxyguanine (8-oxo-dG). Chúng có liên quan đến sự phát triển của ung thư da. Enzyme OGG-1 sửa chữa các 8-oxo-dG, cho thấy rằng việc bổ sung hoạt động của nó thông qua bội tại chỗ có thể làm tăng sửa chữa 8-o0o-dG và sau đó ngăn ngừa sự phát triển ung thư da.
Ultraviolet Endonuclease
Endonuclease UV cũng được phân phối tốt nhất nếu dùng còn nghệ liposomal. Nó hoạt động để nhận ra các phần tử DNA bị méo mó (ví dụ, chất dimer thymine do tia cực tím gây ra), phá vỡ chuỗi DNA gần dimer, loại bỏ vùng bị hư hỏng nhỏ và vá lại sợi bằng các bazơ bổ sung với các bazơ trên sợi nguyên vẹn. Để da tiếp xúc với endonuclease UV cũng giúp giảm các cytokine thường xuyên được giải phóng khi căng thẳng (ví dụ: interleukin-1 [IL-1], IL-6, IL-8, IL-10 và yếu tố hoại tử khối u-a [TNF-a]) . UV endonuclease tiếp tục điều chỉnh giảm nồng độ MMPs tăng cao do tia UV gây ra (ví dụ: MMP-1, còn được gọi là collagenase-1, phân cất collagen I, loại phụ chính của collagen trong ma trận ngoại bào của lớp bì). Một phân nhóm của endonuclease UV, T4 endonuclease V, là một loại enzyme sửa chữa DNA đặc hiệu cho pyrimidinedimers. Khi được sử dụng công nghệ liposomal vào các tế bào người được chiếu UV, hình thức này làm tăng quá trình cắt DNA được chiếu xạ tia cực tím, sự sống sót của các tế bào này và quá trình sao chép sửa chữa DNA. Do đó, việc thoa enzyme sửa chữa DNA này tại chỗ trên da người có thể ngăn ngừa sự hình thành ung thư da.
Photolyase
Photolyase cũng được phân phối tốt nhất khi được đóng gói trong liposome. Nó phân cắt và đảo ngược tổn thương DNA đặc biệt liên quan đến CPD do tia UV có bước sóng ngắn hơn. Quá trình này, được gọi là quá trình kích quang học, phân cắt cyclobutan do tia cực tím gây ra. Photolyase cũng làm giảm quá trình apotosis tế bào do bức xạ UV gây ra.
Tiền chất sửa chữa DNA tự nhiên
Các tiền chất sửa chữa DNA tự nhiên như acetyl tyrosine, Proline, protein thực vật thủy phân và adenosine triphosphate (ATP) có thể được đưa đến các khu vực DNA bị hư hỏng để có thêm lợi ích. Một nghiên cứu gần đây đã chứng minh tính an toàn và hiệu quả của phác đồ thoa có chứa các enzym sửa chữa DNA ổn định về mặt sinh học (OGG-1, UV endonuclease và photolyase) và các protein tiến chất tự nhiên (hỗn hợp của acetyl tyrosine, proline, protein thực vật thủy phân và ATP ). Kết quả của nghiên cứu được đo lường thông qua sự cải thiện trong các dấu hiệu phổ biến nhất của lão hóa ánh sáng. Các biến này bao gồm những yếu tố sau: nếp nhăn mảnh và sâu, kết cấu da, màu sắc, độ mềm mại, độ sáng, độ nhám, độ đàn hồi, sắc tố cm, lỗ chân lông và lão hóa tổng thể. Các nhà điều tra nghiên cứu kết luận rằng việc sử dụng hai lần mỗi ngày một chế độ chăm sóc da tại chỗ có chứa phức hợp enzyme sửa chữa DNA và tiền chất sửa chữa protein tự nhiên được dung nạp tốt và có hiệu quả trong việc cải thiện các dấu hiệu phổ biến nhất của lão hóa trên khuôn mặt.
Unirepair T-43, một sản phẩm của Induchem (Thụy Sĩ), là một phức hợp hoạt tính sinh học sửa chữa DNA, tăng cường cơ chế sửa chữa DNA tự nhiên của tế bào da thông qua việc bổ sung các axit amin như proline và acetyl tyrosine. Cả proline và acetyl tyrosine đều thể hiện tính chất oxy hóa khử. Trong con đường sửa chữa DNA, proline và acetyl tyrosine là mục tiêu của protein kinase, liên quan đến việc sửa chữa DNA bị hư hỏng. Một số nghiên cứu đã tìm thấy mối liên hệ chặt chẽ giữa sự hình thành ban đỏ và việc sửa chữa các tổn thương DNA. Bảo vệ hoặc sửa chữa khỏi tổn thương DNA do tia UV gây ra làm giảm sự phát triển của ban đỏ. Điều thú vị là những bệnh nhân được điều trị trước bằng Unirepair T-43 tại chỗ cho thấy giảm ban đỏ sau khi tiếp xúc với tia cực tím. Điều này được cho là do Unirepair T-43 có khả năng đẩy nhanh quá trình sửa chữa CPD, do đó làm giảm tổn thương DNA và kích hoạt phản ứng viêm sau đó. Khung 3.6 trình bày các tác nhân sửa chữa DNA đã biết.
Chất kháng viêm
Viêm da làm suy yếu chức năng hàng rào biểu bì bằng cách thay đổi tính thẩm thấu của da. Nó gây ra rối loạn chức năng tế bào và gây ra sự bất thường cấu trúc. Cho đến gần đây, viêm (cả cấp tính và mãn tính) không được coi là một yếu tố quan trọng cần phải kiểm soát. Ngày nay, ngày càng thấy rõ rằng viêm là một quá trình phá hủy ở cả da bị bệnh và da không bị bệnh. Ví dụ, viêm là nguyên nhân chính gây ra sẹo (như trong mụn trứng cáp, cảm ứng ung thư da (như trong tổn thương DNA do tia UV gây ra), lão hóa da nhanh (ngoại sinh) và cả tăng sắc tố và giảm sắc tố (sau Rối loạn chức năng hoặc tổn thương tế bào hắc tố do tia UV mạn tính).
Viêm là cách bảo vệ của hệ thống miễn dịch chống lại sự xâm hại đến tính toàn vẹn của nó. Trong một số điều kiện nhất định, chẳng hạn như chữa lành vết thương, tình trạng viêm có thể mang tính xây dựng do nó cần thiết để phục hồi tổn thương. Đây là một ví dụ về viêm cấp tính, là một quá trình có lợi và cần được tạo điều kiện để giải quyết tổn thương nhanh hơn. Tình trạng viêm
| Khung 3.6 |
| Chất sữa chữa DNA |
| Lão hóa được cho là hậu quả của sự tích tụ các tổn thương DNA tự nhiên không được sửa chữa |
Các chất sữa chữa DNA được biết gồm:
|
thường thuyên giảm sau 8 đến 20 ngày khi điều trị đầy đủ. Giải quyết tình trạng viêm cấp tính được đánh dấu bằng tái biểu mô hóa, tăng nguyên phâu Á bào đáy và sửa chữa ma trận ngoại bào. Sau một chấn thương cấp tính, quá trình điều chỉnh lớp bì có lợi và hỗ trợ có thể kéo dài từ 4 đến 6 tháng. Ngược lại, khi tình trạng viêm trở nên mãn tính, nó có thể dẫn đến trạng thái phá hủy, với các di chứng vĩnh viễn và bất lợi (ví dụ: sẹo).
Quá trình chữa lành vết thương thu hút bạch cầu trung tính và đại thực bào, cuối cùng được thay thế bằng tế bào lympho và mô bào. Việc giải phóng các MMP sau đó, và chúng kích hoạt một số con đường gây viêm. Cuối cùng, điều này dẫn đến các quá trình phá hủy như sẹo và các bất thường về kết cấu. Khi một xâm hại lớp sừng không được tái tạo về bình thường, sự phá hủy xảy ra. Nếu tình trạng viêm cấp tính như vậy không được điều trị thích hợp, sẽ dẫn đến tình trạng viêm mãn tính.
Viêm mãn tính cũng có thể xảy ra từ ba quá trình khác: glycation, hình thành ROS và cảm ứng dòng thác axit arachidonic. Glycation được đặc trưng bởi saccharid (đường) trong tuần hoàn lắng đọng trong các mạch máu. Điều này dẫn đến tổn thương mạch máu. Tuy nhiên, sự hoạt hóa của dòng axit arachidonic, thường được gây ra khi tiếp xúc với tia UV, dẫn đến tổn thương lớp lipid kép (chức năng hàng rào). Nó cũng dẫn đến việc kích hoạt các prostaglandin, ức chế quá trình apoptosis, tăng hình thành mạch (để cung cấp oxy và chất dinh dưỡng cho khối u), tăng sinh các tế bào khối u, và cuối cùng là sự xâm lấn và di căn tại chỗ của chúng.
Viêm cấp tính có thể được điều trị dễ dàng thông qua việc thoa các thành phần cụ thể, giúp phục hồi nhanh chóng chức năng hàng rào mạnh mẽ vốn có của da. Mặt khác, điều trị viêm mãn tính cần có phương pháp lâu dài và bài bản hơn. Điều này có thể được thực hiện thông qua việc sử dụng kết hợp các chất chống oxy hóa thoa tác động vào viêm mãn tính thông qua nhiều con đường. Để làm rõ, việc sử dụng một chất chống oxy hóa hoặc chống viêm là không đủ để điều trị đầy đủ viêm mãn tính. Khi được thoa, tác nhân đơn lẻ có thể chuyển đổi qua phản ứng viêm thành tác nhân oxy hóa gây hại; Do đó, một phương pháp kết hợp trong đó tác nhân thứ hai hoạt động như một chất chống oxy hóa thay thế. Đặc điểm của viêm mãn tính được trình bày trong khung 37.
| Khung 3.7 |
| Viêm mạn tính |
| Viêm mãn tính dẫn đến các quá trình phá hủy, chẳng hạn như các vết sẹo và các bất thường về cấu trúc. |
| Có thể điều trị viêm mãn tính bằng cách gây ra giai đoạn viêm cấp tính có kiểm soát, được điều trị. |
| Một chất chống oxy hóa hoặc chất chống viêm không đủ để điều trị dứt điểm tình trạng viêm mãn tính và chất này có thể chuyển đổi thành chất oxy hóa có hại. |
| Phải sử dụng kết hợp các chất chống oxy hóa để điều trị chứng viêm mãn tính. |
Một cách tiếp cận hiệu quả để loại bỏ tình trạng viêm mãn tính là thông qua việc vi ra tình trạng viêm cấp tính được kiểm soát, điều trị sử dụng lượng và nồng độ thích hợp của các chất bôi ngoài da được chọn lọc, tạo ra giai đoạn viêm cấp tính được kiểm soát trong 2 tuần. Da sẽ phản ứng với điều này và thông qua các cơ chế bẩm sinh, sẽ khắc phục được cả tình trạng viêm cấp tính và mãn tính. Quá trình này sẽ lần lượt củng cố chức năng hàng rào, khôi phục khả năng đổi mới của da, loại bỏ tác nhân vi phạm và đưa da trở lại trạng thái khỏe mạnh.
Ngoài chức năng chính của chúng, nhiều chất chống oxy hóa tại chỗ (ví dụ: vitamin E) và kháng sinh tại chỗ (ví dụ, metronidazole) cung cấp lợi ích chống viêm. Tương tự, một số tác nhân thực vật bôi tại chỗ, bao gồm trà xanh và Ginko biloba, cũng tạo ra tác dụng chống viêm.
Ginkgo Biloba
Ginkgo biloba là một loại cây có lá chứa flavonoid, glycoside flavonol và polyphenol (chẳng hạn như terpenoit). Những chất này làm giảm viêm nhờ các đặc tính chống oxy hóa và chống gốc tự do. Các nghiên cứu lâm sàng có kiểm soát đánh giá tác dụng chống viêm và các tác dụng có lợi khác của Ginkgo biloba tại chỗ hiện đang thiếu.
Trà xanh
Chiết xuất trà xanh bồi tại chỗ có chứa epigallocatechin-3-gallate, một polyphenol có tác dụng làm giảm viêm do tia UVB gây ra. Những phát hiện này đã được xác nhận thông qua phép đo độ dày nếp gấp da ở chuột cả trước và sau khi tiếp xúc với tia UVB, Phép đo này phản ánh lượng phù nề của mô (một dấu hiệu của viêm) và là tiêu chuẩn ngành thẩm mỹ hiện hành để định lượng tình trạng viêm. Mặc dù đây là tiêu chuẩn công nghiệp hiện tại, nhưng đây là một thử nghiệm khó để nhân rộng và những phát hiện trên mô hình có thể không bắt buộc phải tương quan với những phát hiện tương tự ở người.
Growth Factors
Yếu tố tăng trưởng là tín hiệu hóa học giữa các tế bào để bật hoặc tắt các hoạt động cụ thể như tăng sinh tế bào, hóa ứng động và hình thành chất nền ngoại bào. Việc thoa các yếu tố tăng trưởng cũng làm giảm các dấu hiệu của lão hóa, chúng thúc đẩy tăng sinh nguyên bào sợi và tế bào sừng, giúp hình thành chất nền ngoại bào. Các yếu tố tăng trưởng có thể được lấy từ một số nguồn, bao gồm tế bào biểu bì, bao quy đầu của con người, tế bào nhau thai, sữa non, vi khuẩn tái tổ hợp, nấm men và thực vật. Các yếu tố tăng trưởng cũng có thể được sản xuất tổng hợp. Danh sách một phần các yếu tố tăng trưởng của con người và các chức năng tương ứng của chúng trên da được thể hiện trong Bảng 3.3.
Việc sử dụng các yếu tố tăng trưởng có nguồn gốc từ con người trong các sản phẩm chăm sóc da tại chỗ đang gây tranh cãi. Mặc dù các yếu tố tăng trưởng của con người đã được chứng minh là có thể sửa chữa hiện tượng lão hóa thông qua cảm ứng tăng sinh và biệt hóa tế bào, sự gia tăng hình thành mạch liên quan (thứ phát sau tiếp xúc VEGF quá mức) cũng được chứng minh là một bước quan trọng trong quá trình chuyển đổi khối u lành thành khối u ác tính (khung 3.8). Hơn nữa, các loại u tế bào hắc tố ác tính khác nhau có các thụ thể cho các yếu tố tăng trưởng (ví dụ, VEGF). Do đó, các nguồn yếu tố tăng trưởng thay thế, không phải con người đã được tìm kiếm để cung cấp các lợi ích cho da giống như các yếu tố tăng trưởng có nguồn gốc từ con người, nhưng không có khả năng kích thích ung thư da. Các yếu tố tăng trưởng có nguồn gốc từ động vật, chẳng hạn như yếu tố có nguồn gốc từ động vật thân mềm, đã được chứng minh là chất thay thế hiệu quả trong việc sửa chữa vấn đề lão hóa.
| Bảng 3.3 Các yếu tố tăng trưởng của người và các chức năng tương ứng của chúng trên da | |
| Growth Factor | Chức năng |
| Fibroblast growth factor (bFGF [FGF-2], FGF-4, FGF-6, KGF [FGF-7), FGF-9) | “Tạo mạch và phân chia nguyên bào sợi” |
| Transforming growth factor (TGP-B1, TGF-B2, TGF-B3) | Di chuyển tế bào sừng, hóa ứng động đại thực bào và nguyên bào sợi |
| Platelet derived growth factor (PDGF AA, PDGF BB, PDGF Rb) | Hóa ứng động đại thực bào và nguyên bào sợi; phân chia nguyên bào sợi và sản xuất chất nền; hoạt hóa đại thực bào |
| Vascular endothelial growth factor (VEGF) | Ảnh hưởng đến sự hình thành mạch và tính thẩm thành mạch, giúp cải thiện dinh dưỡng mô |
| Placental growth factor (PGF) | Thúc đẩy tăng trưởng tế bào nội mô (thành viên của VEGF) |
| Insulin-like growth factors (IGF-1, IGF-BP1, IGF-BP2, IGF-BP3, IGF-BP6) | Phân chia tế bào nội mô và nguyên bào sợi |
| Hepatocyte growth factor (HGF) | Nguyên phân mạnh, lành vết thương và tái tạo mô 3 chiều |
| *Nguyên nhân dẫn đến phân chia, chuyển dạng và biệt hóa tế bào. Adapted from Mehta RC, Smith SR, Grove GL, et al. Reduction in facial photodamage by a topical growth factor product. Drugs Dermatol. 2008;7:864-871; and Sundaram H, Mehta R. Norine J, et al. Role of physiologically balanced growth factors in skin rejuvenation. J Drugs Dermatol. 2009;8(5 Suppl):1-13. |
|
| Khung 3.8 |
| Growth Factors |
| Việc sử dụng các yếu tố tăng trưởng có nguồn gốc từ con người trong các sản phẩm chăm sóc da tại chỗ đang gây tranh cãi. |
| Các yếu tố tăng trưởng đã được chứng minh là có thể sửa chữa hiện tượng lão hóa, nhưng có lo ngại rằng các khối u không hoạt động có thể chuyển thành khối u ác tính. |
| Các loại yếu tố tăng trưởng không có nguồn gốc tử con người và tổng hợp được ưa thích hơn vì tính an toàn được nâng cao. |
| Ossential Advanced Growth Factor Serum chứa lipopeptide tổng hợp |
Kinetin, một yếu tố tăng trưởng tại chỗ có nguồn gốc từ thực vật, cũng có triển vọng tương tự trong việc sửa chữa hiện tượng lão hóa. Yếu tố tăng trưởng được sản xuất tổng hợp, bao gồm lipopeptide (phần hoạt động chính của yếu tố tăng trưởng, bao gồm các axit amin chuỗi nhỏ), đã cho thấy tiềm năng lớn trong việc cung cấp nguyên liệu cần thiết cho nguyên bào sợi sản xuất collagen và elastin, Các lipopeptide tổng hợp này là một trong những thành phần chính trong Ossential Advanced Growth Factor Serum. Bởi vì không có sản phẩm nào của người hoặc động vật được bôi trực tiếp lên da khi sử dụng các yếu tố tăng trưởng tổng hợp, nên tính an toàn của chúng được nâng cao.
CÁC CHẤT HỖ TRỢ
Vì chúng thường chỉ có cơ chế hoạt động ngoại bào và chỉ mang lại lợi ích điều trị nhẹ, nên các chất hỗ trợ nên được sử dụng kết hợp với các chất thiết yếu.
Cá sản phẩm bôi ngoài da được coi là tác nhân hỗ trợ bao gồm AHA, Pat beta-hydroxy (BHA), chất ổn định sắc tố không phải HQ (axit kojic, axit azelaic và arbutin), resorcinol và các chất đặc trị bệnh (5- fluorouracil, imiquimod, benzoyl peroxide, thuốc kháng sinh và thuốc chống nấm tại chỗ).
Alpha-Hydroxy Acids
Cơ chế hoạt động chính xác của AHA, chẳng hạn như axit glycolic, lactic và malic, vẫn chưa được biết. Tuy nhiên, tác động ngoài da được cho là chủ yếu giới hạn ở lớp biểu bì. AHA, còn được gọi là axit trái cây, có tính hút nước yếu (tức là chúng hút nước vào các tế bào da khô). AHA được đặc trưng là có gốc rượu (hydroxyl) ở vị trí alpha so với nguyên tử cacbon mang chức năng carboxyl. Da cảm thấy thô ráp khi có sự tích tụ cục bộ của các tế bào sừng trên bề mặt. Tẩy da chết cưỡng bức bằng các chất bôi ngoài da, chẳng hạn như AHA, có thể khôi phục làn da mịn màng hơn. Nồng độ của tác nhân AHA là rất quan trọng. Ở nồng độ thấp (2% đến 8%), chỉ một số lớp sừng bị loại bỏ, và vẫn còn đủ tế bào để giữ nguyên chức năng hàng rào của da. Ngược lại, nồng độ cô đặc cao hơn 12% có thể dẫn đến mất toàn bộ lớp sừng (ảnh hưởng đến 10 đến 20 lớp tế bào) và gây kích ứng da. Điều này đặc biệt đúng nếu AHA được sử dụng nhiều hơn một lần mỗi ngày.
Mặc dù cơ chế hoạt động chính xác của AHA vẫn chưa được biết, nhưng có giả thuyết cho rằng AHA hoạt động như tác nhân chelate hóa canxi và làm giảm nồng độ ion canxi biểu bì. Việc loại bỏ các ion canxi khỏi sự kết dính của các tế bào sừng sẽ phá vỡ chức năng của chúng và dẫn đến bong vảy. Hơn nữa, những mức độ ion giảm này thúc đẩy sự phát triển của tế bào và làm chậm quá trình biệt hóa, mang lại cho làn da vẻ tươi trẻ. Tuy nhiên, tác dụng do AHA gây ra chỉ là tạm thời vì chúng không điều chỉnh quá trình sừng hóa, cũng như không làm chất sừng mềm hơn như tretinoin. Do đó, khi ngừng sử dụng AHAs, tình trạng đang được điều trị thường trở lại trong vòng 2 hoặc 3 tuần.
Trong nỗ lực tạo ra một sản phẩm mạnh hơn, xu hướng gần đây là tăng nồng độ AHA, do đó làm giảm độ pH tổng thể của chúng. Tuy nhiên, điều này không hoàn toàn có lợi. Sử dụng axit glycolic làm ví dụ, khi độ pH tăng lên, hiệu quả cũng tăng lên (ở mức độ nhẹ), nhưng kích ứng và tác dụng phụ cũng tăng lên (Bảng 3.4). Chỉ riêng tính axit không dự đoán được hiệu quả bong lớp gai. Hiệu ứng liên kết hydro, tĩnh điện, cảm ứng và steric cũng là liên quan.
| Bảng 3.4 Nồng độ axit glycolic và các giá trị pH khác nhau của chúng | |
| Nồng độ (%) | pH |
| 5 | 1.7 |
| 10 | 1.6 |
| 20 | 1.5 |
| 30 | 1.4 |
| 40 | 1.4 |
| 40 | 1.3 |
| 50 | 1.2 |
| 60 | 1.0 |
Cần lưu ý nghiêm túc đến sự thay đổi độ pH trên bề mặt da do AHAs gây ra vì những thay đổi này có thể kéo dài đến 4 giờ sau khi thoa.
Độ pH của axit glycolic được đệm khoảng 2,8 đến 3,5 để sử dụng cho da mặt. Nhiều sản phẩm mỹ phẩm trên thị trường công bố là trung hòa” hoặc “chất đệm”, do đó ít gây kích ứng hơn. Tuy nhiên, cần lưu ý rằng các sản phẩm trung hòa sẽ có ít hiệu quả trên da.
Axit glycolic và axit lactic là AHA được sử dụng phổ biến nhất trong các sản phẩm chăm sóc da. Khi kích thước phần tử của AHA khác nhau, hiệu quả tương ứng của chúng cũng khác nhau. Axit glycolic là nhỏ nhất và do đó có hoạt tính thâm nhập tốt nhất. Axit glycolic có tính hút nước và liên kết với nước trong da. Nó cũng làm giảm liên kết giữa các tế bào sừng. Ở nồng độ cao hơn, axit glycolic tách lớp biểu bì khỏi lớp bì (epidermolysis) thông qua ly giải hemidesmosomes. Nó có thể được sử dụng một mình hoặc kết hợp với các hóa chất khác trong peel.
Nồng độ nhẹ đến trung bình (<30%) của axit glycolic đã được sử dụng để peel da “vào giờ ăn trưa”, Chủng loại bỏ các tế bào lớp sừng và tạo ra sự tẩy da chết ở các tầng dưới của lớp sừng. Vì chúng không có tác động đến lớp bì, nên peel da vào bữa trưa không phải là peel da thật. Thật vậy, chúng có thể mang lại làn da mịn màng tạm thời và cải thiện mụn trứng cá, nhưng chúng không có tác dụng làm mờ nếp nhăn, sẹo hoặc làm săn chắc da. Tác dụng của AHA được trình bày trong Khung 3.9.
Beta-Hydroxy Acids
BHA tạo ra sự mịn màng của bề mặt lớp sừng thông qua hoạt động tiêu sừng của chúng. Tuy nhiên, BHA, chẳng hạn như axit salicylic, gây kích ứng và làm tăng độ nhạy cảm của da. Chúng không được khuyến khích sử dụng hàng ngày trên da bình thường vì có khả năng gây dị ứng. Thông thường, BHA được sử dụng để tăng hiệu quả của peel da hóa học hoặc điều trị mụn cóc và mụn trứng cá. Chúng cũng có thể được sử dụng độc lập (như trong peel” axit salicylic). Điều đáng lưu ý ở đây là việc sử dụng thuật ngữ peel
| Box 3.9 |
| Tác dụng của Alpha-Hydroxy Acids |
| Axit alpha-hydroxy (AHA) tẩy tế bào chết ở tầng sừng có thể khôi phục độ mịn màng cho da. |
| Ở nồng độ thấp (2% đến 8%), AHA chỉ loại bỏ một số lớp sừng, để lại đủ tế bào để giữ nguyên chức năng hàng rào của da |
| Nồng độ cao hơn 12% có thể làm mất đi toàn bộ lớp sừng (10 đến 20 lớp tế bào) và gây kích ứng da và các tác dụng phụ. |
| Axit glycolic có kích thước phân tử nhỏ nhất và do đó cho thấy khả năng thẩm thấu qua da tốt nhất. |
| Tẩy da chết “ăn trưa” với AHA là tẩy da chết chứ không phải peel da thật, chúng không đến được lớp bì, không có tác dụng làm mờ nếp nhăn hoặc sẹo, và không thể làm căng da. |
da để mô tả tác dụng của axit salicylic bôi tại chỗ là không chính xác vì nó Fông có tác động đến lớp bì. Do đó, BHA không được khuyến khích dùng “làm phương pháp điều trị chính cho các nếp nhăn, sẹo hoặc làm săn chắc da.
Ổn định sắc tố không Hydroquinone
Kojic Acid
Axit Kojic là một chất làm sáng da, ức chế enzym tyrosinase liên quan đến quá trình hình thành hắc tố. Nó có nguồn gốc từ một số loài nấm như Penicillium và Aspergillus. Axit kojic thường được sử dụng với nồng độ từ 1% đến 4% và nó thường hiệu quả hơn trong việc làm sáng da khi được sử dụng kết hợp với các chất khác (ví dụ: vitamin C, arbutin, axit glycolic, axit hydroxy, axit gamma-aminobutyric, chiết xuất cam thảo). Kojic acid là một lựa chọn làm sáng da tốt cho những bệnh nhân không thể dung nạp HQ. Các sản phẩm có chứa axit kojic được khuyến khích sử dụng hai lần mỗi ngày trong khoảng 2 tháng hoặc cho đến khi đạt được mức độ làm sáng da mong muốn. Tuy nhiên, vì có khả năng gây mẫn cảm cao, nó thường gây ra viêm da tiếp xúc kích ứng và do đó dung nạp kém.
Azelaic Acid
Một axit dicarboxylic có nguồn gốc từ Pityrosporum ovale, axit azelaic hoạt động như một chất ức chế tyrosinase để làm sáng da. Sự ổn định tối ưu của hoạt động tế bào hắc tố, và do đó điều chỉnh sự tăng sắc tố, đạt được khi sử dụng axit azelaic đồng thời với một sản phẩm giúp tăng cường khả năng thâm nhập của nó (ví dụ: axit glycolic, retinol).
Arbutin
Arbutin, một glycoside có nguồn gốc từ quả bearberry, có tác dụng làm sáng da thông qua việc ức chế tyrosinase. Nói chung, arbutin được cho là ít tác dụng hơn axit kojic và azelaic. Vì vậy, tốt nhất nên sử dụng kết hợp với các chất làm sáng da khác để đạt được hiệu quả điều chỉnh tối ưu tình trạng tăng sắc tố.
Resorcinol
Resorcinol (m-dihydroxybenzene) có hoạt tính tiêu sừng và có thể được sử dụng như một chất lột bề mặt để giảm sự hình thành mụn ẩn. Khi được sử dụng trong các tình trạng như mụn trứng cá, nó có thể tăng cường sự xâm nhập của các chất bôi ngoài da cần thiết được sử dụng đồng thời. Ở nồng độ thấp (1% đến 2%), resorcinol là một thành phần trong nhiều sản phẩm bôi tiêu sừng và sát trùng Nồng độ cao hơn (lên đến 40%) dạng hố bột có thể được sử dụng như một chất lột tẩy để có một lựa chọn điều trị mụn mạnh hơn. Việc sử dụng resorcinol có cường độ cao hơn không được khuyến khích vì chúng có thể gây ra methemoglobin huyết và các tác dụng phụ hệ thần kinh trung ương toàn thân khác tương tự như những tác dụng phụ đã thấy khi sử dụng phenol.
5-Fluorouracil
5-Fluorouracil (5-FU), một chất tương tự Pyrimidine được fluor hóa, có tác dụng gây độc tế bào. Điều thú vị là nó thâm nhập vào các vùng da bất thường (ví dụ: bị tổn thương do ánh sáng) kỹ hơn các vùng da bình thường. Bôi tại chỗ, nồng độ 5% của 5-FU được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận để điều trị nhiều dày sừng ánh sáng và ung thư biểu mô tế bào đáy. Khi điều trị bệnh nhân bị dày sừng ánh sáng, kem có chứa 5 6 5 FU được khuyến khích sử dụng hai lần mỗi ngày trong 2 đến 4 tuần. Để di trị ung thư biểu mô tế bào đáy bể mặt, kem có chứa 5% 5-FU cũng được khuyên dùng hai lần mỗi ngày, nhưng trong thời gian dài hơn (3 đến 6 tuần). Các tác dụng phụ thường gặp nhất, chỉ giới hạn ở vị trí điều trị, bao gồm viêm (đỏ, sưng tấy và tróc da) và đôi khi trợt bề mặt. Các phương pháp điều trị thay thế cho dày sừng ánh sáng bao gồm phương pháp áp lạnh, đốt điện với thìa nạo, peel hóa chất và liệu pháp quang động.
Imiquimod
Một amin dị vòng không nucleoside và là thành viên tổng hợp của họ imidazoquinolone, imiquimod (Aldara) hoạt động như một loại thuốc điều hòa miễn dịch. Nó đã được FDA chấp thuận để điều trị tại chỗ dày sừng ánh sáng, ung thư biểu mô tế bào đáy và mụn cóc sinh dục, Nồng độ 5% của imiquimod trong dạng kem được khuyến nghị sử dụng hai lần mỗi tuần trong 16 tuần đối với bệnh dày sừng ánh sáng và năm lần mỗi tuần trong 6 tuần đối với ung thư biểu mô tế bào đáy. Đối với mụn cóc sinh dục ngoài, bạn nên thoa imiquimod ba lần mỗi tuần trong 16 tuần. Imiquimod liên kết với thụ thể Tool-like-7 (TLR-7) trên đại thực bào, bạch cầu đơn nhân và tế bào hình cây. Sự kích thích các tế bào này thông qua TLR-7 khiến các cytokine tiền viêm được giải phóng(TNF-a, IFN-a, IL-1, IL-6, IL-8, IL-10 và IL-12), sau đó kích hoạt phản ứng miễn dịch qua trung gian tế bào T cell type 1 (T-1). Con đường TH-2 lần lượt bị ức chế. Ngoài việc điều chỉnh hệ thống miễn dịch này, imiquimod còn điều chỉnh hoạt động của tế bào giết tự nhiên bằng cách tạo ra 2’5′-oligoadenylate synthetase. Cùng với nhau, những hành động này ức chế sự phát triển của khối u và vi rút. Các tác dụng phụ thường gặp bao gồm ngứa, mẩn đỏ, sưng tấy, bong tróc da và đôi khi hình thành trợt tại vị trí bôi thuốc.
Benzoyl Peroxide
Benzoyl peroxide bôi tại chỗ, một chất oxy hóa và diệt khuẩn mạnh chống lại vi khuẩn Propionibacterium acnes, Pityrosporum ovale và một số chủng Staphylococcus, được chỉ định để điều trị mụn trứng cá nhẹ đến trung bình. Nó cũng có hoạt tính tiêu nhân mụn và tiêu sừng. Benzoyl peroxide tại chỗ có sẵn ở nhiều nồng độ khác nhau (2,5% đến 20%) và trong nhiều loại chế phẩm (gel, kem và lotion).
KHÁNG SINH THOA
Một danh sách đầy đủ về tất cả các loại thuốc kháng sinh thoa được sử dụng trong da liễu sẽ dài và nằm ngoài phạm vi của chương này. Tuy nhiên, hầu hết các loại thuốc kháng sinh tại chỗ được sử dụng trong da liễu có thể được phân loại đơn giản thành một (hoặc cả hai) trong số hai nhóm sau: những loại được sử dụng để điều trị mụn trứng cá hoặc trứng cá đỏ và những loại được sử dụng để điều trị vết thương đang lành.
Để điều trị mụn trứng cá hoặc trứng cá đỏ, thuốc kháng sinh tại chỗ thường được kê đơn là erythromycin (thuộc nhóm macrolide), clindamycin (thuộc nhóm lincosamide) và metronidazole (thuộc nhóm nitroimidazole). Để điều trị vết thương ngoài da, thuốc kháng sinh tại chỗ thường được sử Cung nhất là mupirocin, bacitracin, neomycin, gentamicin, polymyxin B và bạc sulfadiazine.
Điều trị trứng cá và rosacea
Erythromycin, nhóm macrolide, có tác dụng diệt khuẩn. Nó ức chế tổng hợp Protein bằng cách liên kết không thuận nghịch với tiểu đơn vị 50s của ribosome vi khuẩn. Erythromycin có hiệu quả chống lại các vi khuẩn sau: cầu khuẩn gram dương, Legionella pneumophila, Chlamydia, Corynebacterium diphtheriae, Haemophilus influenzae, Treponema pallidum, Ureaplasma urealyticum và Mycoplasma pneumoniae. Cải thiện mụn trứng cá là do hoạt động tiếp theo của erythromycin chống lại vi khuẩn Propionibacterium acnes. Erythromycin hòa tan kém trong nước. Do đó, các chế phẩm chứa liposomal và nhũ tương thông thường có hiệu quả hơn trong việc cung cấp thuốc này so với loại chứa cồn. Nồng độ tại chỗ của erythromycin thường nằm trong khoảng từ 1% đến 4%.
Clindamycin, một dẫn xuất lincomycin tổng hợp, có tác dụng cơ học giống như erythromycin (liên kết tiểu đơn vị 50S của vi khuẩn). Clindamycin có hiệu quả chống lại vi khuẩn gram dương và gram âm kỵ khí, cũng như hầu hết các cầu khuẩn gram dương hiếu khí. Cũng như erythromycin, clindamycin cải thiện mụn trứng cá thông qua tác dụng diệt khuẩn đối với P. acnes. Clindamycin tại chỗ có sẵn ở nồng độ 1% ở dạng lotion, gel hoặc dung dịch (gốc cồn).
Metronidazole, một loại kháng sinh nitroimidazole tổng hợp, cũng có tác dụng diệt khuẩn. Nó ức chế sự tổng hợp axit nucleic và phá vỡ DNA ở vi khuẩn nhạy cảm (bao gồm hầu hết các vi khuẩn kỵ khí và động vật nguyên sinh). Nhưng không giống như erythromycin và clindamycin, metronidazole không có hoạt tính chống lại P. acnes. Nó cũng không có hoạt tính chống lại Demodex folliculorum, streptococci và staphylococci. Bởi vì hệ vi sinh của da ở bệnh nhân rosacea không thay đổi đáng kể khi sử dụng metronidazole tại chỗ, các tác dụng có lợi rất có thể là do tác dụng chống viêm của thuốc. Tình trạng viêm giảm đi thông qua việc ức chế miễn dịch qua trung gian tế bào và bằng cách hạn chế hóa ứng động bạch cầu.
Điều trị vết thương
Mupirocin, một chất chuyển hóa của Pseudomonas fluorescens, có tác dụng diệt khuẩn khi bôi tại chỗ. Mupirocin làm gián đoạn quá trình tổng hợp protein của vi khuẩn, sự tổng hợp RNA và tổng hợp thành tế bào thông qua việc ức chế men tổng hợp isoleucyl-tRNA của vi khuẩn. Mupirocin có hoạt tính chống lại Staphylococcus epidermidis, Staphylococcus aureus, Streptococcus pyogenes, liên cầu tan huyết beta và một số chủng S. aureus kháng methicillin (MRSA). Điều thú vị là do việc sử dụng mupirocin ngày càng cao, một nghiên cứu cho thấy có tới 65% các chủng MRSA được thử nghiệm kháng lại mupirocin, Mupirocin có ở dạng thuốc mỡ hoặc kem 2%. Vì rất ít mupirocin được chuyển hóa qua da nên hầu hết lượng thuốc bôi vẫn còn trên bề mặt để chống lại vi khuẩn.
Bacitracin có tính kìm khuẩn. Nó có nguồn gốc từ một chủng Bacillus subtilis, và nó ức chế sự tổng hợp thành tế bào vi khuẩn. Bacitracin có hoạt tính chống lại các chủng Streptococcus pneumoniae, S. aureus, H. influenzac
T. Pallidum và Neisseria, Bacitracin được chỉ định sử dụng trong thời gian ngắn trên các vết thương nhỏ vì bệnh nhân có thể bị mẫn cảm với thuốc và sau đó phát triển thành viêm da tiếp xúc dị ứng. Điều này đặc biệt phổ biến khi nó được áp dụng cho da không phản ứng và sử dụng trong thời gian dài.
Có nguồn gốc từ Streptomyces fradiae, neomycin là một aminoglycoside có tính diệt khuẩn, ức chế tổng hợp protein bằng cách liên kết với tiểu đơn vị 30s của ribosome vi khuẩn. Neomycin cũng có thể ức chế các enzym DNA polymerase trong vi khuẩn. Nó có hiệu quả chống lại hầu hết các vi khuẩn gram âm và một số gram dương, bao gồm H. influenzae, Escherichia coli, S. aureus, Proteus, Klebsiella và Serratia. Để giảm khả năng kháng thuốc của vi khuẩn và bù đắp cho khả năng bao phủ liên cầu tương đối yếu của neomycin, bacitracin thường được kết hợp với neomycin và đôi khi với polymyxin B, Polymyxin B cải thiện khả năng bao phủ gram âm gồm cả Pseudomonas, Như đã thấy với bacitracin, khi neomycin được sử dụng trong thời gian dài, khả năng xuất hiện viêm da tiếp xúc dị ứng tăng lên. Do đó, điều trị thường được giới hạn trong một tuần.
Gentamicin, có nguồn gốc từ Micromonospora purpurea, là một aminoglycoside kiếm khuẩn. Nó liên kết một chiều với tiểu đơn vị ribosom của vi khuẩn 30s, có hiệu quả trên vi khuẩn gram âm như Proteus, Pseudomonas aeruginosa và E. coli, Gentamicin cũng có một số tác dụng tích cực đối với các chủng như S, aureus, Lưu ý, gentamicin không tác dụng lên liên cầu. Mặc dù hiếm gặp viêm da tiếp xúc do dị ứng với gentamicin, nhưng khoảng 40% bệnh nhân bị dị ứng ngonmycin (không tiếp xúc với gentamicin trước đó) cũng cho patch test dương tính với gentamicin.
Polymyxin B có tác dụng diệt khuẩn và có nguồn gốc từ Bacillus polymyxa. Nó phá hủy màng tế bào vi khuẩn thông qua một cơ chế giống như chất tẩy rửa. Polymyxin B đặc biệt hiệu quả đối với vi khuẩn gram âm, chẳng hạn như P. aeruginosa, Serratia marcescens và Proteus mirabilis. Do không có khả năng bao phủ vi khuẩn gram dương, polymyxin B thường được kết hợp với bacitracin và neomycin để mở rộng phạm vi bao phủ.
Silver sulfadiazine thường được sử dụng để điều trị bỏng. Nó được tạo thành thông qua phản ứng giữa bạc nitrat và natri sulfadiazine. Silver sulfadiazine ức chế sự nhân lên của vi khuẩn bằng cách liên kết với DNA của vi khuẩn. Nó tác động cả vi khuẩn gram dương và gram âm, bao gồm cả MRSA và P. aeruginosa.
Thuốc kháng nấm tại chỗ
Nhiễm nấm da là một trong những tình trạng phổ biến nhất mà các bác sĩ da liễu gặp phải. Các chất bôi ngoài được sử dụng để điều trị da liễu thường thuộc một trong các loại sau: azoles, polyenes và allylamines-benzylamines, Ba lớp kháng nấm chính này sẽ được trình bày chi tiết hơn ở phần sau. Thuốc kháng nấm tại chỗ ít được sử dụng hơn gồm selen sulfide, hydroxypyridone (ciclopirox olamine) và thiocarbonate (tolnaftate).
Azoles
Azoles, có hiệu quả chống lại nấm Candida, dermatophytes và Malassezia furfur (còn được gọi là Pityrosporum ovale), hoạt động bằng cách ngăn chặn việc sản xuất ergosterol, một thành phần chính của màng tế bào nấm. Cụ thể bon, azoles ngắn tổng hợp ergosterol bằng cách ức chế lanosterol 14ademethylase, một enzym phụ thuộc cytochrom P-450 chuyển đổi lanosterol thành ergosterol. Sau khi màng tế bào nấm bị tổn thương (do giảm ergosterol và tích tụ 14a-methylsterol trong tế bào), độ cứng tăng lên, tính thẩm bị thay đổi ngăn cản nấm phát triển và tồn tại. Các loại thuốc bôi ngoài da thường được kê toa nhất bao gồm ketoconazole, clotrimazole, miconazole và econazole.
Ketoconazole là một dẫn xuất imidazole hòa tan trong nước. Nó có phổ hoạt động rộng chống lại Candida albicans, M. furfur, và dermatophytes. Trong một nghiên cứu, kem ketoconazole 2%, khi bồi hai lần mỗi ngày trong 4 tuần, cho thấy sự cải thiện lâm sàng rõ rệt ở khoảng 82% bệnh nhân bị nấm thân mình, nấm chân và nấm kẽ. Trong một nghiên cứu khác, khoảng 80% trẻ sơ sinh bị viêm da tiết bã được điều trị bằng ketoconazole tại chỗ trong 10 ngày cho thấy mức độ khỏi bệnh từ tốt đến xuất sắc. Hiệu quả tương tự đã được quan sát thấy ở người lớn với tình trạng này, những người được điều trị bằng kem ketoconazole, dầu gội ketoconazole 2%, hoặc cả hai. Những tác động này phần lớn là do hoạt động của nó chống lại M. furfur. Bệnh lang ben và nhiễm nấm Candida ở da cũng cho thấy tỷ lệ khỏi bệnh tuyệt vời với kem ketoconazole.
Clotrimazole thể hiện cơ chế hoạt động tương tự như các thuốc chống nấm azole khác. Nó có hiệu quả chống lại hầu hết các chủng Epidermophyton, Trichophyton, Microsporum, vi khuẩn gram dương và Candida. Khi được sử dụng hai lần mỗi ngày, clotrimazole là một phương pháp điều trị hiệu quả đối với các loại nấm thân mình, tay chân, nấm kẽ, lang ben và nấm candida trên da. Nó có dạng lotion, kem và dung dịch.
Mặc dù thể hiện cơ chế hoạt động tương tự như các thuốc kháng nấm azole khác, miconazole khá đặc biệt. Sau một lần bôi, nó có thể được phát hiện trong lớp sừng trong tối đa 4 ngày. Đây là khoảng thời gian dài hơn đáng kể so với các loại thuốc bôi khác cùng lớp. Miconazole có hoạt tính chống lại các loại nấm da phổ biến sau: Trichophyton mentagrophytes, Trichophyton rubrum, và Epidermophyton floccosum. Nó cũng ức chế sự phát triển của M, furfur và C. albicans. Công thức kem chứa miconazole đã cho thấy hiệu quả trong điều trị nấm thân mình, nấm kẽ, tay chân, lang ben và nấm candida ở da. Nên sử dụng hai lần mỗi ngày cho từng tình trạng bệnh, ngoại trừ lang beng, bôi một lần mỗi ngày cũng có hiệu quả.
Econazole, thể hiện cơ chế hoạt động tương tự như các thuốc kháng nấm azole khác, đáng chú ý là khả năng thâm nhập sâu. Nồng độ ức chế tối thiểu của nó đối với dermatophy kéo dài đến tận lớp trung bì. Econazole ức chế hầu hết các chủng Microsporum, Trichophyton và Epidermophyton, cũng như M, furfur và C. albicans. Econazole tại chỗ điều trị hiệu quả bệnh nấm thân mình, nấm kẽ, tay chân do dermatophy, lang ben, nấm Candida ở da. Điều thú vị là, đối với việc điều trị nhiễm nấm Candida ở da và nấm da, kem econazole 1% đã được chứng minh là có hiệu quả tương tự như kem clotrimazole 1%. Tuy nhiên, những bệnh nhân được điều trị bằng econazole cho thấy sự cải thiện nhanh chóng hơn.
Polyenes
Được xác định thông qua cấu trúc phân tử của chúng, thuốc kháng nai polyene bao gồm các nguyên tử cacbon với các liên kết đôi liên hợp trong một vòng macrolide. Vòng macrolide được đóng lại bởi lactose hoặc bởi một este bên trong. Mặc dù có hai loại thuốc kháng nấm polyene quan trọng trong lâm sàng là nystatin và amphotericin B, nhưng loại thuốc này hiếm khi được sử dụng ở Hoa Kỳ.
Nystatin, được sản xuất bởi Streptomyces albidus và Streptomyces noursei, thể hiện cả đặc tính kiềm nấm và diệt nấm. Cơ chế hoạt động của Nystatin liên quan đến liên kết một chiều với sterol trong màng tế bào của một số chủng Candida. Điều này dẫn đến tăng tính thẩm của màng tế bào và dẫn đến rò rỉ của các yếu tố nội bào. Nystatin không tan trong nước và do đó không được da toàn vẹn hấp thụ. Mặc dù nystatin không có hiệu quả đối với các vi khuẩn, nhưng nó lại có hiệu quả trong điều trị viêm da và niêm mạc do C. albicans, Candida krusei, Candida Tropicalis và Candida parapsilosis. Khuyến cáo điều trị bằng cách bôi nystatin hai lần mỗi ngày vào các khu vực bị ảnh hưởng. Có thể sử dụng công thức dạng kem, bột hoặc thuốc mỡ. Đối với nấm niêm mạc miệng, dạng hỗn dịch thích hợp hơn, và khuyến cáo sử dụng là bốn đến năm lần mỗi ngày.
Allylamines và Benzylamines
Allylamine, bao gồm naptifine và terbinafine, và benzylamine, bao gồm butenafine, có chung cấu trúc và cơ chế hoạt động. Cả allylamine và benzylamine đều có cơ chế hoạt động tương đương với nhóm azole của chất chống nấm. Tất cả chúng đều ức chế sự tổng hợp ergosterol, một yếu tố cần thiết trong màng tế bào nấm. Điều này dẫn đến tăng tính thẩm của màng tế bào nấm, cho phép các yếu tố nội bào quan trọng thoát ra từ bên trong. Sự tích tụ nội bào của tiền chất sterol cũng xảy ra.
Allylamin và benzylamin khác với azoles ở chỗ hai tác nhân này ức chế tổng hợp ergosterol độc lập với cytochrom P450 (một enzym liên quan đến chuyển hóa thuốc và hoạt hóa sinh học). Ngược lại, azoles hoạt động theo cách phụ thuộc cytochrome P-450. Hơn nữa, allylamine và benzylamine ngăn chặn sự tổng hợp ergosterol ở giai đoạn sớm hơn trong con đường sản xuất so với azoles.
Natifine là một allylamine tổng hợp có cả tác dụng diệt nấm và kiểm nấm. Nó có ái lực cao với mỡ, dẫn đến sự xâm nhập hiệu quả của nó và sự tích tụ nồng độ lớn sau đó trong lớp sừng. Naftifine đặc biệt ức chế squalene epoxidase, một loại enzyme cần thiết cho việc chuyển đổi squalene thành squalene oxide trong quá trình sản xuất ergosterol, Naftifine có hiệu quả chống lại nhiều loại nấm da (bao gồm T. mentagrophytes), saprophytes (bao gồm cả Sporothrix schenckii) và nấm men. Một nghiên cứu đã đánh giá việc điều trị nấm thân mình và nấm kẽ bằng cách so sánh kem naftifine 1% với kem econazole 1%. Mặc dù cả hai đều có hiệu quả tương tự nhau, naptifine cho thấy tác dụng khởi phát nhanh hơn. Khi so sánh với clotrimazole, naptifine không chỉ có hiệu quả trong việc điều trị nấm thân mình, nếm kẽ, nấm tay chân và cả candida, mà nó có tác dụng sớm hơn so với clotrimazole. Có sẵn trong cả công thức gel và kem, tần suất sử dụng được đề nghị của naftifine là một đến hai lần mỗi ngày trong mỗi điều kiện đã nói ở trên.
Terbinafine, giống như naftifine, là một chất kháng nấm nhóm allylamine tổng hợp. Thông qua cơ chế độc lập với cytochrome P-450, nó làm tổn hại đến tính toàn vẹn của màng tế bào nấm. Terbinafine ngừng tổng hợp ergosterol bằng cách ức chế epoxidase squalene. Tương tự như naftifine, terbinafine có cả khả năng diệt nấm và kiểm nấm. Nó cũng rất ưa mở, cho phép nồng độ cao tích tụ trong lớp sừng. Điều thú vị là nồng độ tồn lưu cao hơn nồng độ ức chế trung bình đối với các loại nấm da thông thường, người ta phát hiện ra nó 7 ngày sau khi bồi tại chỗ. Terbinafine được tạo bằng cách sửa đổi cấu trúc thành naptifine, làm cho naptifine trước đây mạnh hơn 10 đến 100 lần (về hoạt tính kháng nấm). Terbinafine có tác dụng diệt nấm đối với nhiều loại Dermatophy, C. albicans và một số loại nấm lưỡng hình, bao gồm S. schenckii, Histoplasma capsulatum và Blastomyces dermatitidis. Kem Terbinafine 1% có tác dụng điều trị nấm kẽ, nấm thân mình, tay chân, nấm Candida vùng kẽ. Một nghiên cứu cho thấy hiệu quả tổng thể của terbinafine trong điều trị tất cả các bệnh nhiễm nấm da là khoảng 70% đến 90%, với hiệu quả cao nhất được thấy trong điều trị nấm kẽ và nấm thân mình.
Butenafine, một chất kháng nấm nhóm benzylamine, có cấu trúc tương tự như các allylamine, ngoại trừ nhóm butylbenzyl ở benzylamine, thay thế nhóm allylamine trong nhóm sau. Một đặc tính ấn tượng của butenafine là nồng độ diệt nấm của nó có thể được phát hiện trong lớp sừng ít nhất 72 giờ sau khi bôi, Cơ chế hoạt động của butenafine giống như của nafirìne và terbinafine. Butenafine có tác dụng diệt nấm đối với aspergilli, dermatophytes và nấm lưỡng hình, bao gồm cả S. schenckii. Khả năng ức chế của nó đã được phát hiện là bằng hoặc hơn cả natifine và terbinafine. Tỷ lệ chữa khỏi bệnh nấm kẽ được điều trị bằng butenafine nằm trong khoảng từ 84% đến 100%. Butenafine tại chỗ cũng là một phương pháp điều trị hiệu quả chống lại nấm thân mình, tay chân, lang ben và nấm Candida ở da. Nói chung, đối với các tình trạng trên, nên sử dụng butenafine một lần đến hai lần mỗi ngày trong khoảng 2 tuần. Đáng chú ý, sau khi ngừng butenafine, tỷ lệ khỏi bệnh lâm sàng tiếp tục kéo dài đến 2 tuần. Điều này có thể là do khả năng liên kết mạnh mẽ của nó với chất sừng.
Làm lành vết thương
Biafine
Biafine (OrthoNeutrogena), một loại nhũ tương bôi ngoài da, được sử dụng để đẩy nhanh quá trình chữa bệnh sau viêm da do bức xạ, bỏng, vết thương và điều trị bằng laser bóc tách. Biafine chứa các thành phần sau trong pha nước của nó: muối natri alginate, nước khử khoáng và triethanolamine, Trong trạng thái lipid, tồn tại những chất sau: axit stearic etylen glycol, chất lỏng parafin, propylen glycol, sáp parafin, squalene, cetyl palmitat, dầu bơ và hương liệu. Biafine là một tác nhân hóa ứng động cho đại thực bào và hoạt động ở lớp bì (trong mô hạt). Biafine cũng làm giảm sự bài tiết IL-6, do đó làm tăng tỷ lệ IL-1/ IL-6. Do đó, sự hình thành mổ hạt được tăng cường, cũng như việc sản xuất collagen.
CÁC TÁC NHÂN ĐÁNG NGHI VẤN
Các tác nhân đang nghi vấn đã không cho thấy bất kỳ lợi ích điều trị được chứng minh nào. Do đó, chúng chỉ nên được sử dụng sau khi các chất bôi ngoài da cần thiết hoặc hỗ trợ đã được sử dụng. Có vẻ như vô tận các tác nhân đáng nghi vấn được thêm vào các sản phẩm chăm sóc da khác nhau hiện có trên thị trường. Một danh sách đầy đủ các tác nhân này không chỉ không phù hợp với giới hạn của cuốn sách này mà còn không liên quan vì chúng không cho thấy lợi ích khoa học nào trong các quy trình phục hồi hoặc duy trì sức khỏe làn da. Nhiều loại kem chăm sóc da không kê đơn đắt tiền nhất (có giá từ 200 đô la đến 1.000 đô la cho mỗi hộp nhỏ) chỉ chứa các thành phần hoạt động đáng ngờ, Ví dụ về chúng bao gồm vàng, bạch kim, trứng cá muối, lụa, axit ursolic, Planifolia PFA và chiết xuất phân tử Imperiale Orchidee. Các nghiên cứu lâm sàng ngẫu nhiên, có đối chứng chứng minh hiệu quả của các tác nhân gây nghi vấn phổ biến sau đây hiện không tồn tại: vàng (có trong Kem tăng năng lượng Nano Gold của Chantecaille và Creme Royale của Orlane), bạch kim (có trong La Prairie’s Cellular Radiance Cream), trứng cá muối (có trong La Prairie’s White Caviar Illuminating Cream), lụa (có trong Kanebo’s Sensai Collection Premier The Cream), axit ursolic (có trong Kem chống lão hóa toàn cầu Sisley của Sisley), Planifolia PFA (có trong Kem tái tạo chính xác của Chanel’s Precision Sublimage Serum Essential Regenerating Cream) và Imperiale Orchidee Chiết xuất phân tử (được tìm thấy trong Guerlain’s Orchidee Imperiale Cream Next Generation). Thư từ các công ty đã đề cập trước đây yêu cầu dữ liệu lâm sàng để hỗ trợ hiệu quả của sản phẩm hầu như không được trả lời. Tuy nhiên, một số Công ty đã trả lời chỉ đưa ra những báo cáo vặt vãnh về hiệu quả. Vì vậy, giá cao của nhiều sản phẩm chăm sóc da phổ biến không nhất thiết phản ánh hiệu quả của nó. Do đó, ăn trứng cá muối, mặc quần áo lụa, trang sức bằng vàng và bạch kim, và chiêm ngưỡng hoa lan bằng mắt thường sẽ thích hợp hơn là thoa các sản phẩm có chứa các thành phần đáng ngờ này lên da.
REFERENCES
1. Kligman LH, Chen HD, Kligman AM. Topical retinoic acid enhances the repair of ultraviolet damaged dermal connective tissue. Connect Tissue Res. 1984;12: 139-150.
2. Kligman AM, Dogadkina D, Lavker RM. Effects of topical tretinoin on the non-sun exposed protected skin of the elderly. J Am Acad Dermatol. 1993:29:25-33.
3. Kligman DE, Sadiq I, Pagnoni A, et al. High-strength tretinoin: a method for rapid retinization of facial skin. J Am Acad Dermatol. 1998;39:893-97.
4. Kligman AM. Cosmeceuticals. Dermatol Clin. 2000;18:1-7.
5. Goldfarb MT, Ellis CN, Weiss JS, et al. Topical tretinoin therapy: its use in photoaged skin. J Am Acad Dermatol. 1989;21:654-650.
6. Ellis CN, Weiss JJ, Hamilton TA, et al. Sustained improvement with prolonged 629-637.
7. Green LJ, McCormick A, Weinstein GD. Photoaging and the skin: the effects of treti noin. Dermatol Clin. 1993;11:97-105.
8. Gilchrest BA. Treatment of photodamage with topical tretinoin: an overview. J Am Acad Dermatol. 1997;36:S27-36.
9. Olsen EA, Katz HI, Levine N, et al. Tretinoin emollient cream for photodamaged skin: results of 48-week, multicenter, double-blind studies. J Am Acad Dermatol. 1997;37:217-216.
10. Olsen EA, Katz HI, Levine N, et al. Sustained improvement in photodamaged skin with reduced tretinoin emollient cream treatment regimen: effect of once-weekly and three times-weekly applications. J Am Acad Dermatol. 1997;37:227-230.
11. Chew AL, Bashir SJ, Maibach HI. Topical retinoids. In: Elsner P, Maibach H., eds. Cosmeceuticals: Drugs vs. Cosmetics. New York: Marcel Decker; 2000:107-122.
12. Samuel M, Brooke RC, Hollis S, Griffiths CE. Interventions for photodamaged skin. Cochrane Database Syst Rev. 2005;CD001782.
13. Mukherjee S, Date A, Patravale V, et al. Retinoids in the treatment of skin aging: an overview of clinical efficacy and safety. Clin Interv Aging. 2006;1:327-348.
14. Sorg 0, Antille C, Kaya G, Saurat JH. Retinoids in cosmeceuticals. Dermatol Ther. 2006;19:289-296.
15. Ting W. Tretinoin for the treatment of photodamaged skin. Cutis. 2010;86:47.52.
16. Griffiths CE, Kang S, Ellis CN, et al. Two concentrations of topical tretinoin (retinoic acid) cause similar improvement of photoaging but different degrees of irritation: a double blind, vehicle controlled comparison of 0.1% and 0.025% tretinoin creams. Arch Dermatol. 1995;131:1037-1044.
17. Bhawan J. Short and long-term histologic effects of topical tretinoin on photodam aged skin. Int J Dermatol. 1998;37:286-292.
18. Fluhr JW, Vienne MP, Lauze C, et al. Tolerance profile of retinol, retinaldehyde and retinoic acid under maximized and long-term clinical conditions. Dermatology. 1999;199(Suppl 1):57-60.
19. Kligman AM, Grove GL, Hirose R, et al. Topical tretinoin for photoaged skin. J Am Acad Dermatol. 1986;15:836-859.
20. Kim BH, Lee YS, Kang KS. The mechanism of retinol-induced irritation and its application to anti-irritant development. Toxicol Lett. 2003;146:65-73.
21. Connor MJ, Smit MH. Terminal-group oxidation of retinol by mouse epidermis: inhibition in vitro and in vivo. Biochem J. 1987;244:489-492.
22. Duell EA, Derguini F, Kang S, et al. Extraction of human epidermis treated with retinol yields retro retinoids in addition to free retinol and retinyl-esters. J Invest Dermatol.
23. Kang S, Duell EA, Fisher GJ, et al. Application of retinol to human skin in vivo induces epidermal hyperplasia and cellular retinoid binding proteins characteristic of retinoic acid but without measurable retinoic acid levels or irritation. Invest Dermatol. 1995;105:549-556.
24. Kafi R, Kwak HSR, Schumacher WE, et al. Improvement of naturally aged skin with vitamin A (retinol). Arch Dermatol. 2007;143:606-612.
25. Fluhr JW, Vienne MP, Lauze C, et al. Tolerance profile of retinol, retinaldehyde and retinoic acid under maximized and long-term clinical conditions. Dermatology 1999;199(Suppl 1):57-60.
26. Kurlandsky SB, Xiao JH, Duell EA, et al. Biological activity of all-trans retinol requires metabolic conversion to all-trans retinoic acid and is mediated through acti vation of nuclear retinoid receptors in human keratinocytes. J Biol Chem. 1994;269: 32821-32827
27. Brisaert MG, Everaerts I, Plaizier-Vercammen JA. Chemical stability of tretinoin in
28. Ball Arefiev KL, Hantash BM. Advances in the treatment of melasma: a review of the recent literature. Dermatol Surg. 2012;38:971-984.
29. Rendon MI, Gaviria JI. Skin lightening agents. In: Draelos ZD, Dover JS, Alam M, eds. Procedures in Cosmetic Dermatology: Cosmeceuticals. Philadelphia: Saunders/ Elsevier; 2005:104.
30. Palumbo A, d’Ischia M, Misuraca G, et al. Mechanism of inhibition of melanogenesis by hydroquinone. Biochim Biophys Acta. 1991;1073:85-90.
31. Jimbow K, Obata H, Pathak MA, Fitzpatrick TB. Mechanism of depigmentation by hydroquinone. J Invest Dermatol. 1974;6:436-449.
32. Biewenga GP, Haenen GR, Bast A. The pharmacology of the antioxidant lipoic acid. Gen Pharmacol. 1997;29:315-331.
33. Burke KE: Nutritional antioxidants. In: Draelos ZD, Dover JS, Alam M, eds. Procedures in Cosmetic Dermatology: Cosmeceuticals. Philadelphia: Saunders/Elsevier; 2005:125-132.
34. Meister A, Anderson, ME. Glutathione. Ann Rev Biochem. 1983;52711-760.
35. Linder J. Antioxidants: Essential preventative and corrective topicals. Dermatologist 2011;19:28-33.
36. Chan AC. Partners in defense, vitamin E and vitamin C. Can Physiol Pharmacol. 1993;71:725-731.
37. Montenegro L, Bonina F, Rigano L, et al. Protective effect evaluation of free radical scavengers on UVB induced human cutaneous erythema by skin reflectance spec trophotometry. Int J Cosmet Sci. 2007;17:91-103.
38. McDaniel DH, Neudecker BA, DiNardo JC, et al. Idebenone: a new antioxidant. Part I. Relative assessment of oxidative stress protection capacity compared to commonly known antioxidants. J Cosmet Dermatol. 2005;4:10-17.
39. Tournas JA, Lin FH, Burch JA, et al. Ubiquinone, idebenone, and kinetin provide ineffective photoprotection to skin when compared to a topical antioxidant combi nation of vitamins C and E with ferulic acid. J Invest Dermatol. 2006;126:1185-1187.
40. Huang C, Miller T. The truth about over-the-counter topical anti-aging products: a comprehensive review. Aesthet Surg J. 2007;27:402-412.
41. Farris PK. Topical vitamin C: a useful agent for treating photoaging and other der matologic conditions. Dermatol Surg. 2005;31:814-818.
42. Heber GK, Markovic B, Hayes A. Anhydrous topical ascorbic acid on human skin. Cosmet Dermatol. 2006;5:150-156.
43. Pinnell SR, Yang HS, Omar M, et al. Topical L-ascorbic acid: percutaneous absorption studies. Dermatol Surg. 2001:27:137-142.
44. Traikovich ss. Use of topical ascorbic acid and its effects on photodamaged skin topography, Arch Otolaryngol Head Neck Surg. 1999;125:1091-1098.
45. Lopez Torres M, Thiele JJ, Shindo Y, et al. Topical application of alpha-tocopherol modulates the antioxidant network and diminishes ultraviolet-induced oxidative damage in murine skin. Br J Dermatol. 1998;138:207-215.
46. Thiele JJ, Traber MG, Packer L. Depletion of human stratum corneum vitamin E: an early and sensitive in vivo marker of UV induced photo-oxidation. J Invest Dermatol. 1998;110:756-761.
47. Shindo Y, Witt E, Han D, et al. Dose-response effects of acute ultraviolet irradiation on antioxidants and molecular markers of oxidation in murine epidermis and der mis. J Invest Dermatol. 1994;102:470-475.
48. Weber C, Podda M, Rallis M, et al. Efficacy of topically applied tocopherols and tocotrienols in protection of murine skin from oxidative damage induced by UV-irradiation Free Radic Biol Med. 1997:22:761-769.
49. Weber SU, Thiele JJ, Cross CE, et al. Vitamin C, uric acid, and glutathione gradients in murine stratum corneum and their susceptibility to ozone exposure. J Invest Dermatol. 1999;113:1128-1132.
50. Thiele II. Traber MG, Podda M, et al. Ozone depletes tocopherols and tocotrienols topically applied to murine skin. FEBS Lett. 1997;401:167-170.
51. Valacchi G, Weber SU, Luu C, et al. Ozone potentiates vitamin E depletion by ultra violet radiation in the murine stratum corneum. FEBS Lett. 2000;466:165-168.
52. Baumann L. Skin ageing and its treatment. J Pathol. 2007;211:241-251.
53. Thiele JJ. Ekanayake Mudiyanselage S. Vitamin E in human skin: organ-spe cific physiology and considerations for its use in dermatology. Mol Aspects Med. 2007:28:646-667.
54. Bissett DL, Miyamoto K, Sun P, et al. Topical niacinamide reduces yellowing, wrin kling, red blotchiness, and hyperpigmented spots in aging facial skin. Int J Cosmet Sci. 2004;26:231-238.
55. Bissett DL, Oblong JE, Berge CA. Niacinamide: a B vitamin that improves aging facial skin appearance. Dermatol Surg. 2005;31:860-865.
56. Rivers JK. The role of cosmeceuticals in antiaging therapy. Skin Therapy Lett. 2008;13:5-9.
57. Dell’Acqua G, Schweikert K. A DNA repair complex to decrease erythema and UV induced CPD formation. Cosmetics Toiletries. 2008;123:69-78.
58. Setlow RB, Cyclobutane-type pyrimidine dimers in polynucleotides. Science. 1966;153:379-386.
59. Sutherland BM, Delihas NC, Oliver RP, et al. Action spectra for ultraviolet light induced transformation of human cells to anchorage-independent growth. Cancer Res. 1981;41:2211-2214.
60. Hart R, Setlow RB, Woodhead AD. Evidence that pyrimidine dimers in DNA can give rise to tumors. Proc Natl Acad Sci US A. 1977:74:5574-5578.
61. Harm H. Repair of UV irradiated biological systems: photoreactivation. In: Yang SY, ed. Photochemistry and Photobiology of Nucleic Acids. Vol. 2. New York: Academic Press; 1976:219-262.
62. Takahashi Y, Moriwaki S, Sugiyama Y, et al. Decreased gene expression responsible for post-ultraviolet DNA repair synthesis in aging: a possible mechanism of age. related reduction in DNA repair capacity. J Invest Dermatol. 2005;124:435-442.
63. Yamada M, Udono MU, Hori M, et al. Aged human skin removes UVB-induced pyrimidine dimers from the epidermis more slowly than younger adult skin in vivo. Arch Dermatol. 2006;297:294-302.
64. Yaar M, Gilchrest BA. Photoaging: mechanism, prevention and therapy. Br Dermatol. 2007;157:874-887.
65. Sander CS, Chang H, Salzmann, S, et al. Photoaging is associated with protein oxidation in human skin in vivo. J Invest Dermatol. 2002;118:618-625.
66. Schweikert K, Gafner F, Dell’Acqua G. Uniprotect PT-3: bioactive complex for protection of skin proteins from UV-induced oxidation. Int Cosmet Sci. 2010; 32:29-34.
67. Wulff BC, Schick JS, Thomas Ahner JM, et al. Topical treatment with OGG1 enzyme affects UVB-induced skin carcinogenesis. Photochem Photobiol. 2008;84:317-321.
68. Ceccoli J, Rosales N, Tsimis J, et al. Encapsulation of the UV-DNA repair enzyme T4 endonuclease V in liposomes and delivery to human cells. J Invest Dermatol. 1989:93:190-194.
69. Berardesca E, Bertona M, Altabas K. et al. Reduced ultraviolet-induced DNA dam age and apoptosis in human skin with topical application of a photolyase con taining DNA repair enzyme cream: clues to skin cancer prevention. Mol Med Rep. 2012;5:570-574
70. Kiripolsky MG, Sundaram H, Bucay VW. A multi-center, open-label study to evalu ate the effects of topically applied DNA repair enzymes and substrates on photo aged skin. 2012. White paper.
71. Schweikert K, McGregor W. Klein C, et al. Amino acids to increase DNA repair after UVB irradiation of reconstituted human skin. SÖFW J. 2006;132:22-26.
72. Milligan JR, Aguilera JA, Ly A, et al. Repair of oxidative DNA damage by amino acids. Nucleic Acids Res. 2003;31:6258-6263.
73. Bender K, Blattner C, Knebel A, et al. UV-induced signal transduction. J Photochem Photobiol B. 1997;37:1-17.
74. Petit-Frere C, Clingen PH, Grewe M, et al. Induction of interleukin-6 production by ultraviolet radiation in normal human epidermal keratinocytes and in a human ker nocyte cell line is mediated by DNA damage. J Invest Dermatol. 1998:111:354-359.
75. Wolf P. Maier H, Mullegger RR, et al. Topical treatment with liposomes containing T4 endonuclease V protects human skin in vivo from ultraviolet-induced upregulation of interleukin-10 and tumor necrosis factor. J Invest Dermatol. 2000;114:149-156.
76. Stege H, Roza L. Vink AA, et al. Enzyme plus light therapy to repair DNA damage in ultraviolet-B-irradiated human skin. Proc Natl Acad Sci US A. 2000;97:1790-1795.
77. Schul W. Jans J, Rijksen YMA, et al. Enhanced repair of cyclobutane pyrimi dine dimers and improved UV resistance in photolyase transgenic mice. EMBO). 2002:21:4719-4729.
78. Berg RJW, Ruven HJT, Sands AT, et al. Defective global genome repair in XPC mice is associated to skin cancer susceptibility but not with sensitivity to UVB induced erythema and edema. J Invest Dermatol. 1998;110:405-409.
79. Dell’Acqua G, Schweikert K. A DNA repair complex to decrease erythema and UV-induced CPD formation. Cosmetics Toiletries. 2008;123:1-8.
80. Draelos ZD: Cosmeceutical botanicals: part 1. In: Draelos ZD, Dover JS, Alam M, eds. Procedures in Cosmetic Dermatology: Cosmeceuticals. Philadelphia: Saunders/ Elsevier; 2005:75-77.
81. Katiyar SK, Elmets CA, Agarwal R, et al. Protection against ultraviolet-B radia tion-induced local and systemic suppression of contact hypersensitivity and edema responses in C3H/HeN mice by green tea polyphenols. Photochem Photobiol. 1995;62:855-861.
82. Babu M, Wells A. Dermal-epidermal communication in wound healing. Wounds. 2001;13:183-189.
83. Bertaux B. Horneback W, Eisen AZ, et al. Growth stimulation of human keratino cytes by tissue inhibitor of metalloproteinases. J Invest Dermatol. 1991:97:679-85.
84. Finch PW, Rubin JS, Miki T, et al. Human KGF is FGF related with properties of a paracrine effector of epithelial cell growth. Science. 1989;245:752-55.
85. Eming SA, Krieg T, Davidson JM. Inflammation in wound repair: molecular and cellular mechanisms. J Invest Dermatol. 2001;127:514-525.
86. Schwartz E, Cruickshank FA, Christensen CC, et al. Collagen alterations in chroni cally sun-damaged human skin. Photochem Photobiol. 1993;58:841-844.
87. Bonin-Debs AL Boche I, Gille H, et al. Development of secreted proteins as bio therapeutic agents. Exp Opin Biol Ther. 2004;4:551-558.
88. Mehta RC, Smith SR, Grove GL, et al. Reduction in facial photodamage by a topical growth factor product. J Drugs Dermatol. 2008;7:864-871.
89. Sundaram H, Mehta R. Norine J, et al. Role of physiologically balanced growth fac tors in skin rejuvenation. J Drugs Dermatol. 2009;8(5 Suppl):1-13.
90. Demidova Rice TN, Hamblin MR, Herman IM. Acute and impaired wound healing pathophysiology and current methods for drug delivery. Part 2. Role of growth face tors in normal and pathological wound healing: therapeutic potential and methods of delivery. Adv Skin Wound Care. 2012:25:349-370.
91. Liu B, Earl HM, Baban D, et al. Melanoma cell lines express VEGF receptor KDR and respond to exogenously added VEGF Biochem Biophys Res Commun. 1995;217:721-727.
92. Lazar-Molnar E, Hegyesi H, Toth S, et al. Autocrine and paracrine regulation by cytokines and growth factors in melanoma. Cytokine. 2000;12:547-554.
93. Draelos ZD. Exploring the pitfalls in clinical cosmeceutical research. Cosmet Dermatol. 2007;20:556-558.
94. Tribo-Boixareu MJ, Parrado-Romero C, Rais B, et al. Clinical and histological effi cacy of a secretion of the mollusk Cryptomphalus aspersa in the treatment of cutaneous photoaging. Cosmet Dermatol. 2009:22:247-252
95. Wang X. A theory for the mechanism of action of the alpha hydroxy acids applied to the skin. Med Hypothes. 1999;53:380-382.
96. DiNardo JC, Grove GL, Moy LS. Clinical and histological effects of glycolic acid at different concentrations and pH levels. Dermatol Surg. 1996;22:421-424.
97. Draelos ZD. Dermatologic considerations of AHAs. Cosmet Dermatol. 1997;10:14-18
98. Daniello NJ. Glycolic acid controversies. Int J Aesthetic Restor Surg. 1996;4:113-116.
99. Murad H, Shaman AT, Premo PS. The use of glycolic acid as a peeling agent. Dermatol Clin. 1995;13:285-307.
100. Moy LS, Murad H, Moy RL. Glycolic acid peels for the treatment of wrinkles and photoaging. J Dermatol Surg Oncol. 1993;19:243-246.
101. Piacquadio D, Dobry M, Hunt S, et al. Short contact glycolic acid peels as a treatment for photodamaged skin: a pilot study. Dermatol Surg. 1996;22:449-452.
102. Coleman WP, Futrell JM. The glycolic acid tricholoroacetic acid peel. ) Derniatol Surg Oncol. 1994;20:76-80.
103. Newman NN, Newman A, Moy LS, et al. Clinical improvement of photoaged skin with 50% glycolic acid. Dermatol Surg. 1996;22:455-460.
104. Moy LS, Howe K, Moy RL. Glycolic acid modulation of collagen production in human skin fibroblast culture in vitro. Dermatol Surg. 1996;22:439-441.
105. Lim JT. Treatment of melasma using kojic acid in a gel containing hydroquinone and glycolic acid. Dermatol Surg. 1999;25:282-284.
106. Bontemps H. Mallaret M, Besson G, et al. Confusion after topical use of resorcinol. Arch Dermatol. 1995;131:112.
107. Baumbach JL, Sheth PB. Topical and intralesional antiviral agents. In: Wolverton SE, ed. Comprehensive Dermatologic Drug Therapy. Philadelphia: Saunders; 2001:532-533.
108. Stanley, MA. Imiquimod and the imidazoquinolones: mechanism of action and therapeutic potential. Clin Exp Dermatol. 2002;27(7):571-577.
109. Navi D, Huntley A. Imiquimod 5 percent cream and the treatment of cutaneous malignancy. Dermatol Online J. 2004;10:4.
110. Skinner RB Jr. Imiquimod. Dermatol Clin. 2003;21:291-300.
111. Cove JH, Holland KT. The effect of benzoyl peroxide on cutaneous micro-organisms in vitro. J Applied Bacteriol. 1983;54:379-382.
112. Oh CW, Myung KB. Retention hyperkeratosis of experimentally induced comedones in rabbits: the effects of three comedolytics. J Dermatol. 1996;23:169-180.
113. Hsu S. Quan LT. Topical antibacterial agents. In Wolverton SE, ed. Comprehensive Dermatologic Drug Therapy. Philadelphia: Saunders: 2001:480-481.
114. Mycek MJ, Gertner SB, Perper MM. Lippincott’s Illustrated Review: Pharmacology, New York: JB Lippincott; 1992.
115. Puhvel SM. Effects of treatment with erythromycin 1.5 percent topical solution or clindamycin phosphate 1.0 percent topical solution on P. acnes counts and free fatty acid levels. Cutis. 1982;31:339-42.
116. Rappaport M, Puhvel SM, Reisner RM. Evaluation of topical erythromycin and oral tetracycline in acne vulgaris. Cutis. 1982;30:122-126, 130, 132-135.
117. Moreau D: Physician’s Drug Handbook. Springhouse, PA: Springhouse Corporation; 1995.
118. Schmadel LK, McEvoy GK. Topical metronidazole: a new therapy for rosacea. Clin Pharm. 1990;9:94-101.
119. Gamborg Nielson P. Metronidazole treatment in rosacea with 1% metronidazole cream: a double-blind study. Br J Dermatol. 1983;108:327-332.
120. Eriksson G, Nord CE. Impact of topical metronidazole on the skin and colon microflora in patients with rosacea. Infection. 1987;15:8-10.
121. Gamborg Nielsen P. Metronidazole treatment in rosacea. Int J Dermatol. 1988;27:1-5.
122. Ward A, Campoli-Richards DM. Mupirocin: a review of its antibacterial activity, pharmacokinetic properties and therapeutic use. Drugs. 1986;32:425-444.
123. Parenti MA, Hatfield SM, Leyden JJ. Mupirocin: a topical antibiotic with a unique structure and mechanism of action. Clin Pharm. 1987;6:761-70.
124. Miller MA, Dascal A, Portnoy J, et al. Development of mupirocin resistance among methicillin-resistant Staphylococcus aureus after widespread use of nasal mupirocin ointment. Infect Control Hosp Epidemiol. 1996;17:811-813.
125. Lechevalier HA. The 25 years of neomycin. CRC Crit Rev Microbiol. 1975;3:359-97.
126. Winkelman W. Gratton D. Topical antibacterials. Clin Dermatol. 1989:7:156-162.
127. Marks JG Jr, DeLeo VA. Contact and Occupational Dermatology. St Louis: Mosby Year Book; 1997
128. Marone P, Monzillo V, Perversi L, et al. Comparative in vitro activity of silver sul fadiazine, alone and in combination with cerium nitrate, against staphylococci and gram-negative bacteria. J Chemother. 1998:10:17-21.
129. Phillips RM, Rosen T. Topical antifungal agents. In: Wolverton SE, ed. Comprehensive Dermatologic Drug Therapy. Philadelphia: Saunders 2001:497-523.
130. Vanden Bossche H. Mode of action of pyridine, pyrimidine and azole antifungals. In: Berg G, Plempel M, eds. Sterol Biosynthesis Inhibitors, Chichester, UK: Ellis Horwood; 1988:9.
131. Vanden Bossche H, Marichal P. Mode of action of anti-Candida drugs: focus on terconazole and other ergosterol biosynthesis inhibitors. Am J Obstet Gynecol. 1991;165:1193-1199.
132. Vanden Bossche H. Cytochrome P450: target for itraconazole. Drug Dev Res. 1986;8:287-298.
133. Vanden Bossche H, Lauwers W. Willemsens G, et al. Molecular basis for the antimy.
cotic and antibacterial activity of N-substituted imidazoles and triazoles: the inhibi tion of isoprenoid biosynthesis. Pestic Sci. 1984;15:188-198.
134. Vanden Bossche H. Biochemical targets for antifungal azole derivatives: hypothesis
on the mode of action. In: Mcginnis MK, ed. Current Topics in Medical Mycology Vol. 1. New York: Springer-Verlag 1985.
135. Lester M. Ketoconazole 2% cream in the treatment of tinea pedis, tinea cruris, and tinea corporis. Cutis. 1995;55:181-183.
136. Taieb A, Legrain V, Palmier C, et al. Topical ketoconazole for infantile seborrhoeic der matitis. Dermatologica. 1990;181:26-32.
137. Carr MM, Pryce DM, Ive FA. Treatment of seborrheic dermatitis with ketoconazole. I. Response of seborrheic dermatitis of the scalp to topical ketoconazole. Br J Dermatol. 1987:116:213-216.
138. Peter RU, Richarz-Barthauer U. Successful treatment and prophylaxis of scalp sebor
rhoeic dermatitis and dandruff with 2% ketoconazole shampoo: results of a multi center, double-blind, placebo-controlled trial. Br J Dermatol. 1995;132:441-445.
139. Farr P. Shuster S. Treatment of seborrheic dermatitis with topical ketoconazole. Lancet. 1984;2:1271-1272.
140. McGrath J, Murphy GM. The control of seborrhoeic dermatitis and dandruff by antipi tyrosporal drugs. Drugs. 1991;41:178-184.
141. Stratigos JD, Antoniou C, Katsambas A, et al. Ketoconazole 2% cream versus hydro cortisone 1% cream in the treatment of seborrheic dermatitis: a double-blind com parative study. J Am Acad Dermatol. 1988;19:850-853.
142. Ive FA. An overview of experience with ketoconazole shampoo. Br J Clin Pract. 1991;45:279-284.
143. Green CA, Farr PM, Shuster S. Treatment of seborrhoeic dermatitis with ketocon azole. II. Response of seborrhoeic dermatitis of the face, scalp and trunk to topical ketoconazole. Br J Dermatol. 1987;116:217-221.
144. Katsambas A, Antoniou C, Frangouli E, et al. A double-blind trial of treatment of seborrhoeic dermatitis with 2% ketoconazole cream compared with 1% hydrocortisone cream. Br J Dermatol. 1989;121:353-357.
145. Cauwenbergh G, De Doncker P. Schrooten P, et al. Treatment of dandruff with a 2% ketoconazole scalp gel. A double-blind placebo-controlled study. Int J Dermatol. 1986;25:541.
146. Danby FW, Maddin WS, Margesson LJ, et al. A randomized, double-blind, pla cebo-controlled trial of ketoconazole 2% shampoo versus selenium sulfide 2.5% shampoo in the treatment of moderate to severe dandruff. J Am Acad Dermatol 1993:29:1008-1012.
147. Rekacewicz I, Guillaume JC, Benkhraba F, et al. A double-blind placebo-controlled study of a 2 percent foaming lotion of ketoconazole in a single application in the treatment of pityriasis versicolor. Ann Dermatol Venereol. 1990;117:709-711.
148, el Euch D, Riahi I, Mokni M, et al. Ketoconazole 2% foaming gel in tinea versicolor: report of 60 cases. Tunis Med. 1999:77:38-40.
149. Caterall MD. Ketoconazole therapy for pityriasis versicolor (letter). Clin Exp Dermatol. 1982;7:679.
150. Savin RC, Horwitz SN. Double-blind comparison of 2% ketoconazole cream and placebo in the treatment of tinea versicolor. J Am Acad Dermatol. 1986;15:500-503.
151, Greer D, Jolly H. Topical ketoconazole treatment of cutaneous candidiasis. J Am Acad Dermatol. 1988;18:748-749.
152. Holt RJ, Newman RL. Laboratory assessment of the antimycotic drug clotrimazole. J Clin Pathol. 1972:25:1089-1097.
153. Gupta AK, Einarson TR, Summerbell RC, et al. An overview of topical antifungal therapy in dermatomycoses: a North American perspective. Drugs. 1998;55:645-674.
154. Clayton YM, Connor BL. Clinical trial of clotrimazole in the treatment of superficial fungal infections. Postgrad Med J. 1974;50(Suppl 1):66-69,
155. Gip L. The topical therapy of pityriasis versicolor with clotrimazole. Postgrad Med J. 1974;50(Suppl 1):59-60.
156. Oberste-Lehn H. Ideal properties of a modern antifungal agent: the therapy of myco ses with clotrimazole. Postgrad Med J. 1974;50(Suppl 1):51-53.
157. Fredriksson T. Topical treatment of superficial mycoses with clotrimazole. Postgrad Med J. 1974;50(Suppl 1):62-64.
158. Polemann G. Clinical experience in the local treatment of dermatomycoses with clotrimazole. Postgrad Med J. 1974;50(Suppl 1):54.56.
159. Zaias N, Battistini F. Superficial mycoses. Treatment with a new, broad-spectrum antifungal agent: 1% clotrimazole solution. Arch Dermatol. 1977,113:307-308.
160. Plempel M, Buchel KH, Bartmann K, et al. Antimycotic properties of clotrimazole. Postgrad Med J. 1974;50(Suppl 1):11-12.
161. Van Cutsem JM, Thienpont D. Miconazole, a broad-spectrum antimycotic agent with antibacterial activity. Chemotherapy. 1972;17:392-404.
162. Odds FC, Abbott AB, Pye G, et al. Improved method for estimation of azole anti fungal inhibitory concentrations against Candida species, based on azole/antibiotic interactions. J Med Vet Mycol. 1986;24:305-311.
163. Botter AA. Topical treatment of nail and skin infections with miconazole, a new broad spectrum antimycotic. Mykosen. 1971;14:187-191.
164. Brugmans J. Van Cutsem J. Thienpont D. Treatment of long term tinea pedis with miconazole. Arch Dermatol. 1970;102:428-432.
165. Fulton JE Jr. Miconazole therapy for endemic fungal disease. Arch Dermatol. 1975;111:596-598.
166. Mandy SJ, Garrott TC. Miconazole treatment for severe dermatophytoses. J Am Med Assoc. 1974;230:72-75.
167. Ongley RC. Efficacy of topical miconazole treatment of tinea pedis. Can Med Assoc J. 1978;119:353-354.
168. Heel RC, Brogden RN, Speight TM, et al. Econazole: a review of its antifungal activity and therapeutic efficacy. Drugs. 1978;16:177-201.
169. Schaefer H, Stuttgen G. Absolute concentrations of an antimycotic agent, econazole, in the human skin after local application. Arzneimittelforschung. 1976;26:432-435
170. Brenner M. Efficacy of twice-daily dosing of econazole nitrate 1% cream for tinea pedis. J Am Podiatr Med Assoc. 1990;80:583-587.
171. Cullen S, Millikan L. Mullen R. Treatment of tinea pedis with econazole nitrate cream. Cutis. 1986;7:388-389.
172. Cullen S, Rex I, Thorne E. A comparison of a new antifungal agent, 1% econazole nitrate (Spectazole) cream versus 1% clotrimazole cream in the treatment of inter triginous candidiasis. Curr Ther Res. 1984;35:606-609.
173. Vicik G, Mendiones M, Qinones C, et al. A new treatment for tinea versicolor using econazole nitrate 1.0 percent cream once a day. Cutis. 1984;33:570-571.
174. Fredriksson T. Treatment of dermatomycoses with topical econazole and clotrima zole. Curr Ther Res. 1979;25:590-594.
175. Daily A, Kramer S, Rex I, et al. Econazole nitrate (Spectazole) cream, 1 percent: a topical agent for the treatment of tinea pedis. Cutis. 1985;35:278 279.
176. Medoff G, Kobayashi G. The polyenes. In: Speller DCE, ed. Antifungal chemotherapy. London: John Wiley & Sons; 1980.
177. Hazen EL, Brown R. Nystatin. Ann N Y Acad Sci. 1960;89:258-266.
178. Fitzpatrick J. Topical antifungal agents. In: Freederg I, Eisen A, Wolff K, eds. Dermatology in General Medicine. New York: McGraw-Hill; 1999:2737-2741.
179. Bennett JE. Antimicrobial agents: antifungal agents. In: Gilman AG, Rall TW, Nies AS, eds. The Pharmacological Basis of Therapeutics. New York: McGraw-Hill 1993:1165-1181.
180. Ryder N. Mode of action of allylamines. In: Berg D, Plempel M, eds. Sterol Biosynthesis Inhibitors. Chichester, UK: Ellis Horwood; 1988.
181. Ryder N, Dupont M. Inhibition of squalene epoxidase by allylamine antimycotic compounds: a comparative study of the fungal and mammalian enzymes. Biochem). 1985;230:765-770
182. Ryder N. The mechanism of action of terbinafine. Clin Exp Dermatol. 1989;14: 98-100
183. Georgopoulos A, Petranyi G, Mieth H, et al. In vitro activity of naftifine, a new anti fungal agent. Antimicrob Agents Chemother. 1981;19:386-389.
184. Petranyi G, Georgopoulos A, Mieth H. In vivo antimycotic activity of naftifine. Antimicrob Agents Chemother. 1981;19:390-392.
185. Schuster I, Schaude M, Schatz F, et al. Preclinical characteristics of allylamines. In: Berg D, Plempel M, eds. Sterol biosynthesis inhibitors. Chichester, UK: Ellis Horwood; 1988:449-470.
186. Grassberger M, Mieth M, Petranyi G, et al. Aspects of antimycotic research exempli fied by the allylamines. Triangle. 1986;25:711-784.
187. Jones TC. Treatment of dermatomycoses with topically applied allylamines: naftifine and terbinafine. J Dermatol Treat. 1990;1(Suppl 2):29-32.
188. Faruqi A, Khan K, Qazi A, et al. In vitro antifungal activity of naftifine (SN 105-843
GEL) against dermatophytes. J Pakistani Med Assoc. 1981;31:279-282.
189. Millikan LE, Galen WK, Gewirtzman GB, et al. Naftifine cream 1% versus econazole cream 1% in the treatment of tinea cruris and tinea corporis. J Am Acad Dermatol. 1988;18:52-56.
190. Kagawa S. Comparative clinical trial of naftifine and clotrimazole in tinea pedis, tinea cruris, and tinea corporis. Mykosen. 1987;30(Suppl 1):63-69.
191. Haas PJ, Tronnier H, Weidinger G. Naftifine in foot mycoses: double-blind therapeu tic comparison with clotrimazole. Mykosen. 1985;28:33-40.
192. Smith EB, Wiss K. Hanifin JM, et al. Comparison of once and twice-daily naftifine cream regimens with twice-daily clotrimazole in the treatment of tinea pedis. J Am Acad Dermatol. 1990;22:1116-1117.
193. Smith EB, Brenerman DL, Griffith RF, et al. Double-blind comparison of naftifine cream and clotrimazole/betamethasone dipropionate cream in the treatment of tinea pedis. J Am Acad Dermatol. 1992:26:125-127.
194. Zaun H, Luszpinski P. Multicenter double-blind contralateral comparison of naftifine and clotrimazole cream in patients with dermatophytosis and candidiasis. Z Hautkr. 1984:59:1209-1217.
195. Petranyi G, Meingassner JG, Mieth H. Antifungal activity of the allylamine deriva tive terbinafine in vitro. Antimicrob Agents Chemother. 1987;31:1365-1368.
196. Hill S, Thomas R. Smith SG, et al. An investigation of the pharmacokinetics of topi cal terbinafine (Lamisil) 1% cream. Br J Dermatol. 1992;127:396-400.
197. Stutz A. Allylamine derivatives: a new class of active substances in antifungal chemo therapy. Angew Chemie (International Edition: England), 1987;26:320-328.
198. Stutz A. Synthesis and structure activity correlations within allylamine antimycotics. Ann N Y Acad Sci. 1988;544:46-62.
199, Clayton YM. In vitro activity of terbinafine. Clin Exp Dermatol. 1989;14:101. 103.
200. Kagawa S. Clinical efficacy of terbinafine in 629 Japanese patients with dermatomyco sis. Clin Exp Dermatol. 1989;14:116-119.
201. Villars V. Jones TC. Clinical efficacy and tolerability of terbinafine (Lamisil): a new topi cal and systemic fungicidal drug for treatment of dermatomycoses. Clin Exp Dermatol. 1989;14:124-127.
202. Nussenbaumer P. Dorfsatter G, Grassberger M, et al. Synthesis and structure activity relationships of phenyl-substituted benzylamine antimycotics: a novel benzylamine antifungal agent for systemic treatment. J Med Chem. 1993;36:2115-2120
203. Maeda T, Takase M, Ishibashi A, et al. Synthesis and antifungal activity of butenafine hydrochloride (KP-363), a new benzylamine antifungal agent. Yakugaku Zasshi. 1991;111:126-137.
204. Arika T, Hase T, Yokoo M. Anti-Trichophyton mentagrophytes activity and percu. taneous permeation of butenafine in guinea pigs. Antimicrob Agents Chemother. 1993;37:363-365.
205. Arika T, Yokoo M, Hase T, et al. Effects of butenafine hydrochloride, a new ben zylamine derivative, on experimental dermatophytosis in guinea pigs. Antimicrob Agents Chemother. 1990;34:2250-2253.
206. Tschen E, Elewski B, Gorsulowsky DC, et al. Treatment of interdigital tinea pedis with a 4-week once-daily regimen of butenafine hydrochloride 1% cream. J Am Acad Dermatol. 1997;36:59-S14.
207. Greer D, Weiss J, Rodriguez D, et al. Treatment of tinea corporis with topical once daily butenafine HCI 1%: a double-blind, placebo controlled trial. Presentation at 55th Annual American Academy of Dermatology Meeting, 1997.
208. Lesher J, Babel D, Stewart D, et al. Butenafine HCl 1% cream in the treatment of tinea cruris: A multicenter, vehicle controlled, double-blind trial. Presentation at 55th Annual American Academy of Dermatology Meeting, 1997.
209. Lesher JL. Jr, Babel DE, Stewart DM, et al. Butenafine 1% cream in the treatment of tinea cruris: a multicenter, vehicle-controlled, double-blind trial. J Am Acad Dermatol. 1997,36:S20-S24.
210. Greer DL, Weiss J, Rodriguez DA, et al. A randomized trial to assess once-daily topical treatment of tinea corporis with butenafine, a new antifungal agent. J Am Acad Dermatol. 1997;37:231-225.
211. Savin R, De Villez RL, Elewski B, et al. One-week therapy with twice-daily butenafine 1% cream versus vehicle in the treatment of tinea pedis: a multicenter, double-blind trial. J Am Acad Dermatol. 1997;36:S15-S19.
212. Reyes BA, Beutner KR, Cukllen SI, et al. Butenafine, a fungicidal benzylamine deriv ative, used once daily for the treatment of interdigital tinea pedis. Int J Dermatol. 1998;37:450-453.
213. Savin R. Lucky A, Brennan B. One-week treatment of tinea pedis with butenafine HCl 1%: a multi-center, double-blind, randomized trial. Presentation at 55th Annual American Academy of Dermatology Meeting, 1997.
214. Biafine PDR drug information; as found on 1-8-12 on www.por.net/drugpages/ concisemonograph.
215. Coulomb B, Friteau L, Dubertret L. Biafine applied on human epidermal wounds is chemotactic for macrophages and increases the IL-1/IL-6 ratio. Skin Pharmacol. 1997;10:281-287.
216. Brown GL, Nanney LB, Griffen J, et al. Enhancement of wound healing by topical treatment with epidermal growth factor. N Engl J Med. 1989;321:76-79.
Xem thêm:
CHĂM SÓC VÀ ĐIỀU TRỊ DA NHẠY CẢM

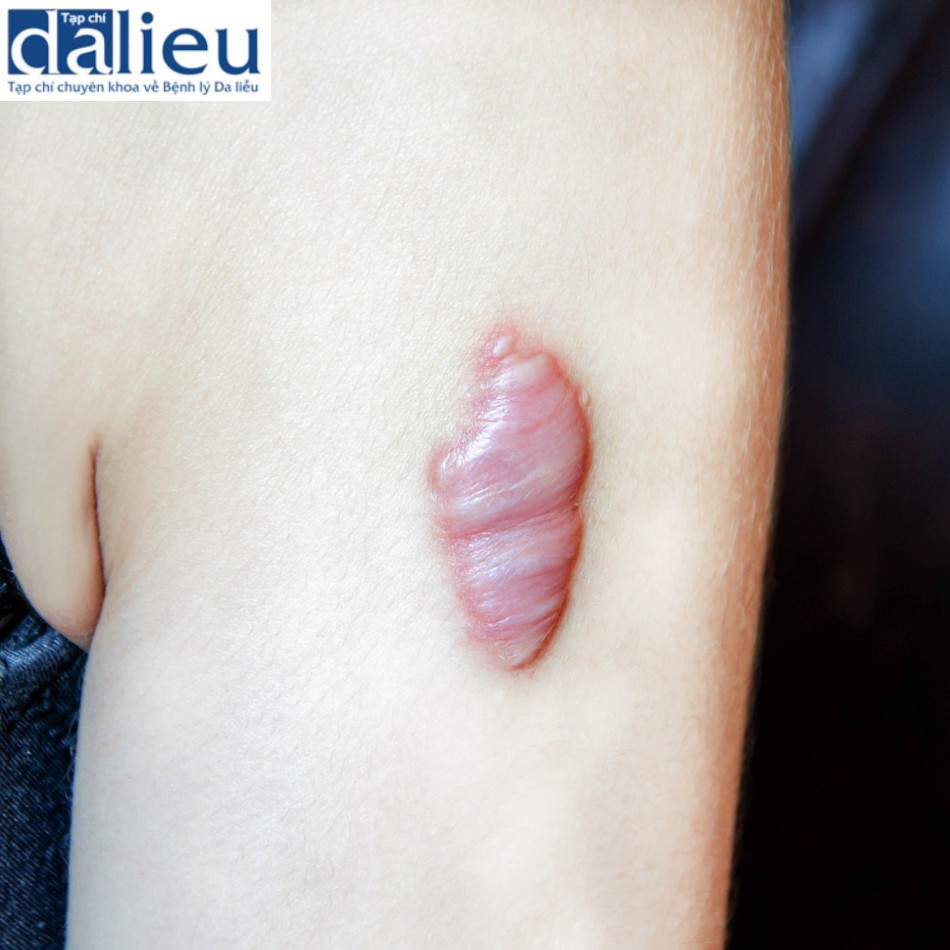
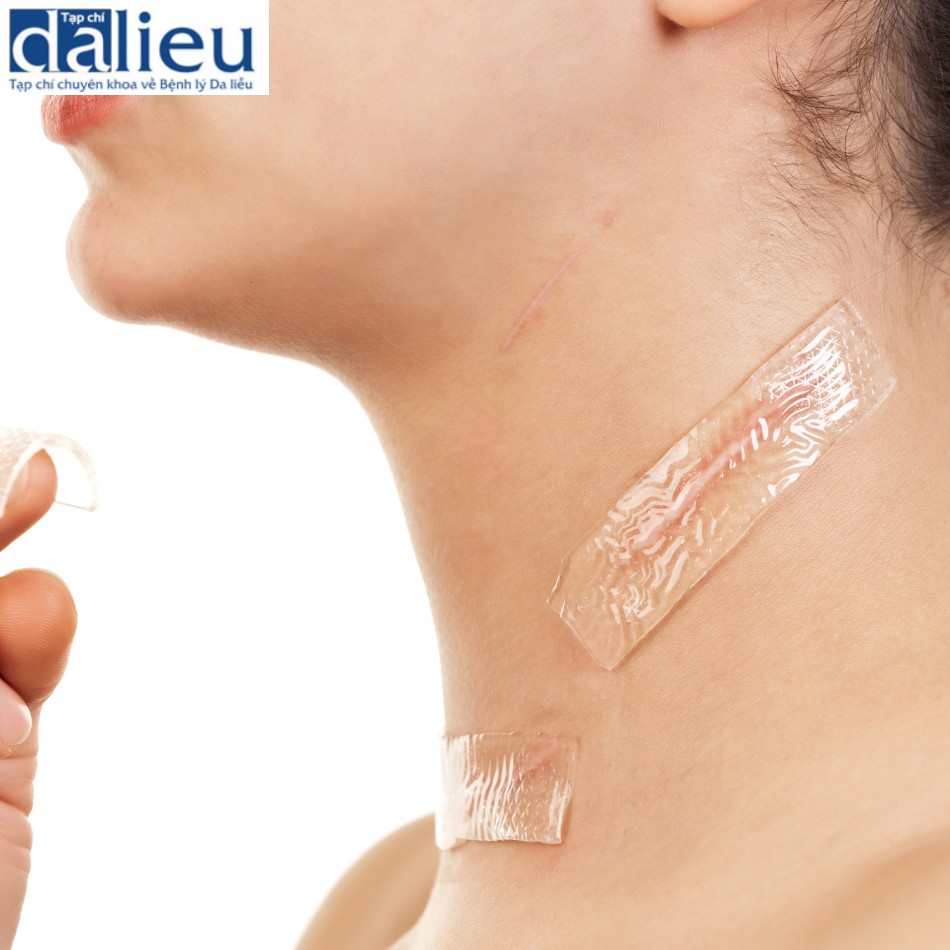
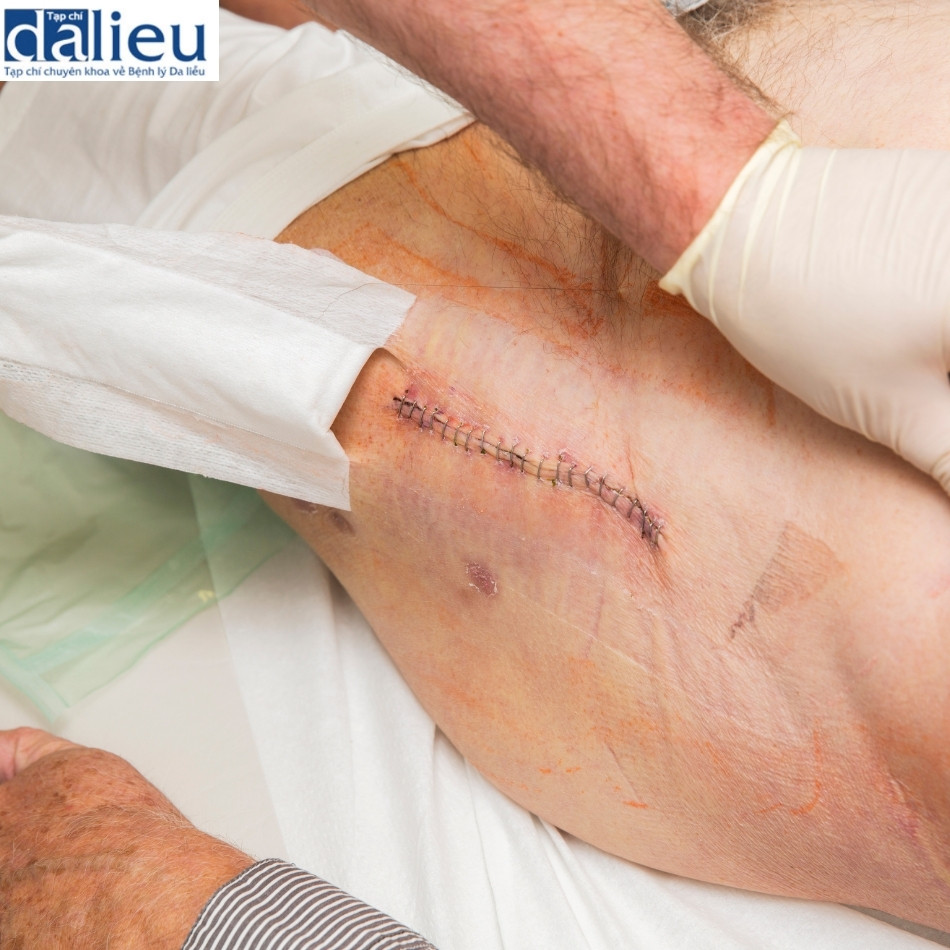
Tin tức hữu ích, cảm ơn nhà thuốc đã chia sẻ nhé