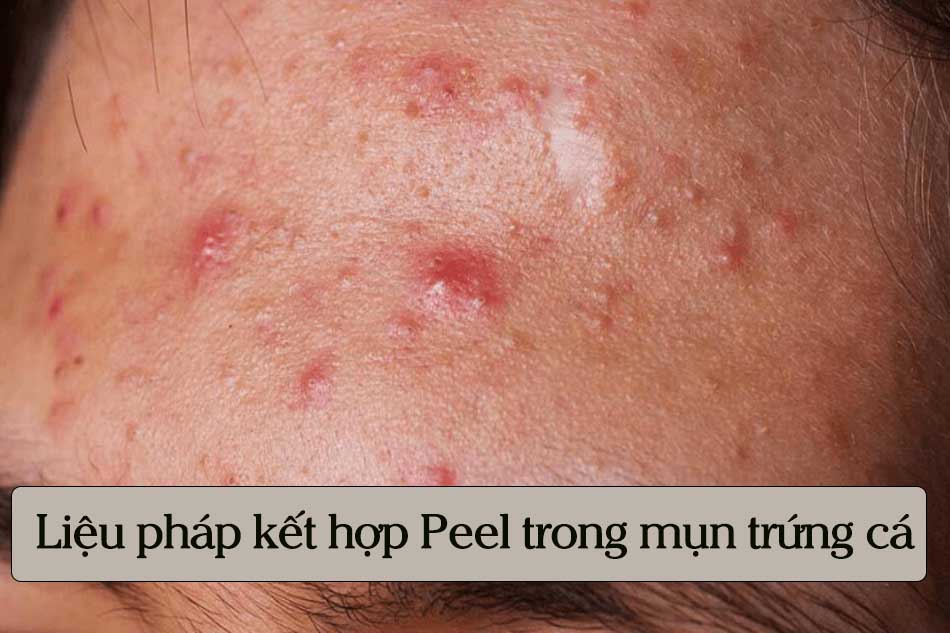
Tác giả: Ziyu Wei và Qiang Ju Dịch
Bs Dịch: Trương Tấn Minh Vũ
Chương 11: Mụn và các yếu tố môi trường
Xin gửi đến bạn đọc chủ đề Mụn và các yếu tố môi trường. Tải bản PDF tại đây
Giới thiệu
Da là cơ quan lớn nhất của cơ thể con người và một trong những chức năng chính của nó là bảo vệ cơ thể khỏi các chất gây hại, cho dù là bức xạ tia cực tím, hóa chất độc hại, hoặc tiếp xúc lâu/ liên tục với nước, có liên quan đến viêm da tiếp xúc, hóa chất. Giảm sắc tố da do hoá chất, bệnh mô liên kết, ung thư da và mụn trứng cá [1–5]. Về mặt lâm sàng, nguyên nhân của mụn trứng cá bao gồm cả yếu tố nội sinh như androgen và yếu tố ngoại sinh. Tiếp xúc với môi trường là yếu tố ngoại sinh quan trọng trong nguyên nhân của mụn trứng cá, dẫn đến một nhóm mụn trứng cá do yếu tố môi trường gây ra gồm chloracne do dioxin, mụn nhựa than, hút thuốc lá và bức xạ cực tím (UV) [6]. Đặc điểm lâm sàng và cơ chế của mụn trứng cá do yếu tố môi trường khác với mụn trứng cá nội sinh, vốn vẫn còn nhiều lầm tưởng cho đến nay. Chloracne do yếu tố môi trường, mụn do hút thuốc lá, mụn do nhựa than đá và mụn do tia cực tím gây ra được trình bày.
Chloracne
Chloracne thường là biểu hiện đầu tiên của nhiễm độc dioxin, gây ra bởi các hóa chất môi trường như phenol clo hóa, PCB và naphtalen clo hóa, có thời gian bán hủy dài trong cơ thể con người [7]. Hầu hết các trường hợp chloracne là do tiếp xúc nghề nghiệp và không do nghề nghiệp, như tai nạn Seveso ở Ý [8], trúng độc 2,3,7,8- tetrachlorodibenzo-p-dioxin (TCDD) trong tai nạn chất độc của Yushchenko, cựu tổng thống Ukraine [9], và thuốc diệt cỏ [10].
Chloracne khác với mụn trứng cá về đặc điểm lâm sàng, đặc trưng chủ yếu là các comedone giả không viêm, nốt sần và nang giống comedone. Các tổn thương lan rộng chủ yếu ảnh hưởng đến mặt, ngực và lưng, cũng như cổ, thân, tứ chi, bộ phận sinh dục, nách và các vùng da khác [7, 11]
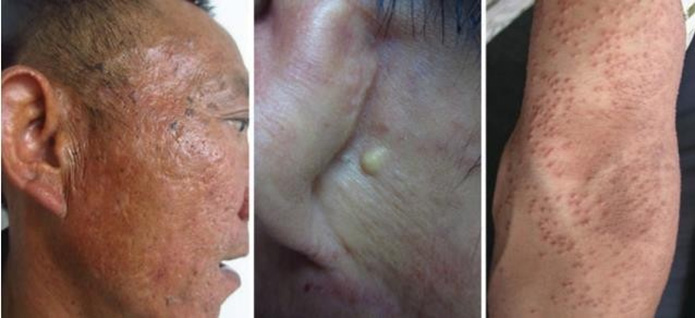
Ngoài ra, cũng có thể thấy ban đỏ cấp tính ở mặt, giảm tiết bã nhờn và da khô, sắc tố, bệnh lý chuyển hóa porphyrin, rậm lông, dày da, tăng tiết mồ hôi tay và tăng sừng lòng bàn tay. Về mặt mô bệnh học, chloracne chủ yếu được đặc trưng bởi sự tăng sản của biểu bì, giảm và không có tuyến bã nhờn, và hoàn toàn khác với mụn trứng cá [11, 12].
Mặc dù các tổn thương da được tóm tắt dưới thuật ngữ “chloracne”, chúng đại diện cho một quá trình hamartomatous (tăng sản lành tính) chức năng thích nghi đối với sự phơi nhiễm chất độc [13], được đặt tên là các tổn thương da do TCDD “hamartomas da do dioxin” [14]. Trên thực tế, các tổn thương giống chloracne được tìm thấy với các hóa chất khác như hút thuốc lá [15] và thuốc [12, 16], nhưng nếu chúng thuộc cùng một bệnh thì vẫn chưa rõ ràng, cần được nghiên cứu thêm trong tương lai.
Cơ chế phân tử chính xác của dioxin trên da người vẫn chưa rõ ràng. Sự biến đổi do chloracnegen của đơn vị nang lông tuyến bã được thúc đẩy bởi sự hoạt hóa và tăng tốc thoát ra của tế bào từ phần tế bào gốc cùng với sự chuyển đổi từ kiểu hình nang lông tuyến bã biệt hóa sang một dạng biểu bì, với nổi bật tăng sản và tăng sừng hóa biểu bì, và sự thu nhỏ tuyến bã và nang lông [17, 18]. Con đường truyền tín hiệu của thụ thể aryl hydrocarbon (AhR) đóng một vai trò trung gian quan trọng trong hoạt động của dioxin, đặc biệt là điều hoà giảm tế bào gốc đơn vị nang lông tuyến bã [19], bao gồm tăng tốc sự biệt hóa đầu cuối của tế bào sừng [20] và chuyển sự biệt hóa của tế bào tuyến bã thành các tế bào giống tế bào sừng [21, 22] cũng như giảm quá trình tạo lipid của các tuyến bã [23]. Các phân tử mục tiêu dưới dòng của AhR rất đa năng, bao gồm tác động của các enzym chuyển hóa xenobiotic (CYP), IL-1β, các yếu tố tăng trưởng khối u, c-Myc, thụ thể yếu tố tăng trưởng biểu bì và protein trưởng thành tế bào lympho B 1 (Blimp1) [21, 24].
Mặc dù một số tác nhân điều trị đã được sử dụng trong điều trị chloracne, nó khá kháng với liệu pháp thông thường. Ức chế tín hiệu AHR-CYP1A1 và kích hoạt trục chống oxy hóa NRF2 đã được thử nghiệm [25]. Retinoids thường được sử dụng trong điều trị các bệnh da dạng mụn trứng cá; tuy nhiên, nghiên cứu trong ống nghiệm cho thấy rằng retinoids không chỉ không hiệu quả trong điều trị các tổn thương da do TCDD ở chuột không có lông mà còn dẫn đến sự phát triển mạnh hơn [26]. Cách kiểm soát hiệu quả duy nhất là loại bỏ các yếu tố gây ra.
Hút thuốc lá và mụn
Một số nghiên cứu đã được tiến hành để làm sáng tỏ mối quan hệ giữa hút thuốc và mụn, và kết quả gây ra khá nhiều tranh cãi. Một số nghiên cứu cho thấy không có mối liên hệ nào giữa việc hút thuốc lá và mụn [27–29]. Một nghiên cứu cắt ngang cho thấy mối tương quan nghịch giữa hút thuốc và tỷ lệ bị mụn; trong khi đó, thuốc lá có thể biểu hiện đặc tính kháng viêm, dẫn đến ức chế mụn trứng cá dạng sẩn mụn mủ ở nữ giới [30, 31]. Tuy nhiên, các quan sát ngược lại cho thấy hút thuốc lá có thể dẫn đến tình trạng mụn trứng cá xấu đi cũng được báo cáo [6, 32].
Dường như mụn trứng cá sau tuổi dậy thì ở phụ nữ có thói quen hút thuốc nghiêng về mụn trứng cá không viêm, được đặc trưng bởi các comedone nhỏ và lớn, với ít tổn thương viêm [33, 34]. Đánh giá mô học cho thấy các comedone mở và đóng và các tuyến bã nhờn bình thường trong sinh thiết da của những người hút thuốc bị mụn trứng cá [34].
Khói thuốc lá chứa hơn 4000 hóa chất có thể được chia thành hai giai đoạn, đó là giai đoạn hạt bao gồm nicotine, hắc ín và benzopyrene và giai đoạn khí bao gồm CO, NO2 và hydrogen cyanide [35]. Nicotine gây ra quá trình tăng sừng hóa ở da thông qua việc kích hoạt các thụ thể nicotine acetylcholine (nACh-R) trong tế bào sừng ở người trong ống nghiệm [36]. Trong khi đó, tiếp xúc với nicotine lâu dài dẫn đến sự gia tăng bã nhờn hoặc thay đổi thành phần bã nhờn, được trung gian bởi nACh-R trong các tuyến bã nhờn của tổn thương mụn trứng cá [37]. Nicotine và các thành phần khác trong khói thuốc lá gây ra những thay đổi vi tuần hoàn với hậu quả là co mạch và giảm oxy máu [38, 39] và biểu hiện tác động ức chế hóa ứng động của bạch cầu trung tính và tế bào bạch cầu [40]. Nicotine cũng ức chế quá trình viêm thông qua tác động lên hệ thần kinh trung ương và ngoại vi [41]. Benzo (a) pyrene (BaP) là chất gây ô nhiễm môi trường có trong khói thuốc lá và là một trong những hydrocacbon thơm đa vòng (PAHs) [42]. Nghiên cứu gần đây cho thấy BaP có thể kích hoạt con đường tín hiệu AhR và thể hiện tác dụng tiền viêm và tác dụng ức chế sản xuất bã nhờn trong tế bào tuyến bã của người [43], do đó xác nhận dữ liệu trong một bài báo khác rằng BaP thể hiện tác động gây viêm và oxy hóa thông qua con đường tín hiệu AhR ở tế bào sừng người [44]. Một báo cáo gần đây cho thấy rằng tiếp xúc với khói thuốc lá cũng liên quan đến các comedone giống chloracne, trong đó BaP trong thuốc lá có thể liên quan [15]. Hơn nữa, hút thuốc có thể gây ra mụn trứng cá bằng cách tác động interleukin-1α (IL-1α) và làm trầm trọng thêm sự hình thành comedone cũng như những thay đổi về viêm ở các comedone, dẫn đến stress oxy hóa và sự tích tụ sau đó của lipid peroxide [6, 31, 34, 45]. Tiếp xúc với khói thuốc lá gây ra các điều chỉnh sau chuyển đổi thụ thể scavenger loại B 1 (protein SRB1) và sau đó là mất protein SRB1, gây ra sự thay đổi hàm lượng lipid trong tế bào tuyến bã của người [46].
Một loạt các PAH không tan trong nước trong khói thuốc lá có thể tạo ra các loại ôxy và kích hoạt con đường tín hiệu AhR, do đó tác động MMP-1 và CYP1B1, những chất đã bị loại bỏ bởi chất ức chế AhR [47, 48].
Mụn nhựa than (Coal Tar Acne)
Nhựa than đá là một trong những sản phẩm phụ của quá trình chưng cất than đá, là một sản phẩm dầu màu nâu sẫm, có hàm lượng PAH cao, như BaP, benzo [a] anthracene, và dibenz [a, h] anthracene [49]. Nhựa than đá đã được sử dụng trong điều trị bệnh ngoài da như bệnh vẩy nến, bệnh chàm và viêm da trong nhiều năm [50]. Gần đây, có báo cáo rằng nhựa than đá đã điều chỉnh thành phần vi khuẩn trên da và khôi phục hàng rào biểu bì bị tổn hại thông qua các peptide kháng khuẩn được tạo ra bởi tế bào sừng thông qua sự kích hoạt của AhR, điều này có thể giải thích các cơ chế tiềm ẩn hiệu quả của nhựa than trong điều trị bệnh viêm da cơ địa dị ứng [51]. Các tác dụng phụ ngắn hạn là viêm nang lông, kích ứng và dị ứng khi tiếp xúc [52]. Các nghiên cứu trên động vật [53–55] và các nghiên cứu trong môi trường nghề nghiệp [53, 56–58] cho thấy nguy cơ ung thư da không phải hắc tố sau khi tiếp xúc kéo dài với nhựa than đá tăng lên. Tuy nhiên, một nghiên cứu thuần tập lớn gồm 13.200 bệnh nhân bị vẩy nến và chàm cho thấy điều trị bằng nhựa than đá không liên quan đến việc tăng nguy cơ ung thư, điều này tạo cơ sở cho ứng dụng lâm sàng của nhựa than đá trong thực hành da liễu [59].
Mụn thường được quan sát thấy ở các công nhân trong ngành công nghiệp sau khi tiếp xúc lâu dài với một số phân tử hữu cơ, như nhựa than đá hoặc dầu thô, đặc trưng chính là comedone đen và hiếm khi sẩn trên vùng tiếp xúc [50, 60–63] (Hình 11.2).
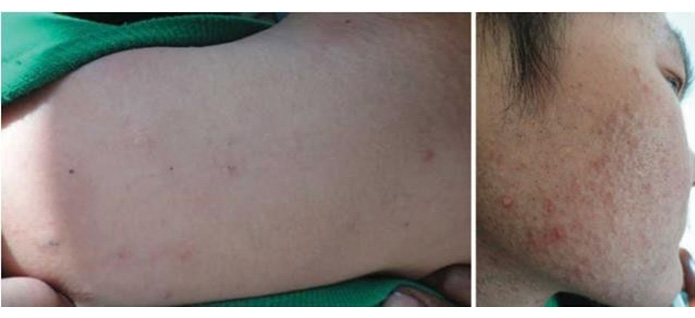
Có một cuộc khảo sát bệnh nhân quốc tế cho thấy rằng một số yếu tố nghề nghiệp như tiếp xúc với nhựa than đá được báo cáo thường xuyên hơn đáng kể đối với nhóm mụn trứng cá so với nhóm đối chứng khỏe mạnh [29]. Phơi nhiễm PAH trong nghề nghiệp thường đi kèm với thời gian rất dài ở mức nồng độ thấp, trong khi trong thực hành da liễu, phơi nhiễm cao và thời gian ngắn. Ngoài ra, con đường hấp thu cũng khá khác nhau: với sử dụng trong da liễu, sự hấp thu PAH chủ yếu xảy ra qua da, trong khi ở những cơ sở nghề nghiệp, con đường hấp thu cũng có thể bao gồm hệ thống hô hấp. Sự khác biệt trong kết quả các nghiên cứu về nguy cơ ung thư sau khi tiếp xúc với nhựa than đá có thể là do sự khác biệt về mức độ phơi nhiễm PAH và các con đường hấp thụ [52].
Có một số nghiên cứu liên quan đến sinh lý bệnh chính xác của mụn do nhựa than đá gây ra, và các PAH trong nhựa than đá có thể làm trung gian sinh bệnh thông qua việc kích hoạt đường truyền tín hiệu AhR
Xem thêm: Tổng quan về chẩn đoán điều trị mụn trứng cá dành cho phụ nữ
UV và mụn

Điều kiện khí hậu và sự thay đổi theo mùa thường đi kèm với sự kết hợp của nhiệt độ, độ ẩm và bức xạ tia cực tím mạnh có thể gây ra bùng phát mụn viêm, liên quan đến mụn nhiệt đới [64-67]. Một nghiên cứu gần đây cho thấy rằng mụn trứng cá xuất hiện thường xuyên hơn đáng kể ở các vùng nóng và ẩm [29]. Rõ ràng rằng tiếp xúc với tia UV có ảnh hưởng lớn đến làn da, như ung thư da do tia UV gây ra [68], chức năng hàng rào biểu bì [69] và lão hóa da [70]. Có một số nghiên cứu quan sát mối quan hệ giữa tiếp xúc ánh nắng mặt trời và mụn trứng cá; tuy nhiên, mối quan hệ giữa chúng vẫn còn gây tranh cãi. Một nghiên cứu cắt ngang trên mẫu đại diện gồm 2516 học sinh ở Serbia cho thấy sự thoái triển UVB trên tế bào tuyến bã nuôi cấy có thể trực tiếp gây ra sự biểu hiện của các cytokine gây viêm, đặc biệt là IL-1β và IL-8 [80]. Bên cạnh đó, mối quan hệ giữa tia UV và hệ vi sinh vật da đã được ghi nhận rằng việc sản xuất porphyrin của vi khuẩn P. acnes bị giảm khi tăng liều tia UV, điều này cho thấy vi khuẩn trên da mặt phản ứng với tia UV [81].
Bệnh Favre – Racouchot (FRD), còn được gọi là bệnh da đàn hồi dạng nốt với các nang và comedone còn được gọi là “comedone mặt trời” (Hình 11.3), là một bệnh về thẩm mỹ tương đối phổ biến ở người lớn tuổi trung niên. Gần 6% người lớn trên 50 tuổi bị ảnh hưởng, với tỷ lệ hiện mắc cao hơn ở nam giới da trắng [82]. Các yếu tố nguy cơ chính của FRD bao gồm tiếp xúc với tia UV kéo dài quá mức, hút thuốc lá và xạ trị. Về mặt lâm sàng, nó đặc trưng bởi sự hiện diện của nhiều comedone đóng và mở trong một vùng da bị tổn thương do ánh sáng, với vị trí ưu tiên ở các vùng quanh mắt và thái dương. Mụn mọc thường đối xứng và không có viêm, khác với mụn trứng cá. Về mặt mô học, FRD đặc trưng bởi bệnh sợi đàn hồi do ánh sáng và teo biểu bì xung quanh các tổn thương dạng nang. Các comedone tương tự như mụn trứng cá cũng có thể được thấy [83]. Hedelund và Wulf [84] đã thực hiện một thử nghiệm bằng cách sử dụng cả tia UV-A1 và UV-B. Thử nghiệm cho kết quả dương tính, vì chiếu tia UV (cả với UV-A1 và UV-B) dẫn đến các comedone, với mối liên hệ chặt chẽ hơn giữa mức độ nghiêm trọng của bệnh với tia UV-B hơn là với UV-A1.
Theo các nghiên cứu gần đây, vitamin D và magie ascorbyl phosphate (MAP) ức chế tác động gây viêm sau khi điều trị P. acnes và chiếu tia UVB trong tế bào tuyến bã được nuôi cấy. Do đó, chúng nên được coi là một liệu pháp bổ sung để điều chỉnh mụn viêm do tia UV gây ra [85, 86]. Hơn nữa, tiếp xúc với ánh sáng mặt trời đã được coi là một nguồn ánh sáng thay thế nhanh hơn và an toàn hơn cho liệu pháp quang động (PDT). Một nghiên cứu lâm sàng cho thấy DL-PDT dường như là một liệu pháp hiệu quả và dễ dung nạp để điều trị mụn viêm từ nhẹ đến nặng [87]. Ngoài ra, hiệu quả của liệu pháp tia UV, ánh sáng nhìn thấy hoặc ánh sáng hồng ngoại trong điều trị mụn trứng cá đã được chứng minh, do đó chúng có thể được sử dụng để nhắm mục tiêu P. acnes để điều trị mụn trứng cá, mà không làm tăng biểu hiện của chỉ dấu sinh học viêm và sản xuất bã nhờn [88]. Liệu pháp chiếu tia UV thông thường có thể có tác dụng có lợi cho mụn trứng cá bằng cách thay đổi hệ vi sinh vật trên da và giảm mật độ P. acnes [89].
Kết luận
Các yếu tố ngoại sinh đóng vai trò quan trọng trong căn nguyên của mụn, dẫn đến một nhóm mụn do yếu tố môi trường gây ra bao gồm chloracne do dioxin, mụn nhựa than, hút thuốc lá và bức xạ tia UV. Tuy nhiên, sinh lý bệnh của các yếu tố vật lý và hóa học này trên mụn vẫn chưa chắc chắn và gây tranh cãi, có thể có cơ chế khác với mụn trứng cá do yếu tố nội sinh gây ra. Hiểu rõ hơn về cách hoạt động của các yếu tố ngoại sinh này và cách chúng ảnh hưởng vào chức năng sinh lý của tế bào tuyến bã, tăng sừng hóa, điều hòa hệ vi sinh vật da, khởi đầu hệ miễn dịch bẩm sinh và quá trình viêm nhiễm, do đó dẫn đến sự xấu đi của mụn trứng cá, hy vọng sẽ cải thiện những hướng dẫn trong chẩn đoán và điều trị mụn trứng cá do yếu tố môi trường gây ra trong tương lai
Tài liệu tham khảo
- English JS, Dawe RS, Ferguson J. Environmental effects and skin Br Med Bull. 2003;68:129 42.
- Kotryna L, Marléne I, Laura Heavy metals and the skin: sensitization patterns in Lithuanian metalworkers. Contact Dermatitis. 2020;83(6):450–7.
- Wei B, Yu J, Kong C, Li H, Yang L, Xia Y, Wu A follow-up study of the development of skin lesions associated with arsenic exposure duration. Environ Geochem Health. 2018;40:2729–38.
- Passeron T, Krutmann J, Andersen ML, Katta R, Zouboulis CC. Clinical and biological impact of the exposome on the skin. J Eur Acad Dermatol 2020;34 Suppl 4:4–25.
- Ju Q, Zouboulis Endocrine-disrupting chemicals and skin manifestations. Rev Endocr Metab Disord. 2016;17:449–57.
- Yang YS, Lim HK, Hong KK, Shin MK, Lee JW, Lee SW, Kim Cigarette smoke-induced interleukin-1 alpha may be involved in the pathogenesis of adult acne. Ann Dermatol. 2014;26:11–6.
- Panteleyev AA, Bickers Dioxin-induced chloracne–reconstructing the cellular and molecular mechanisms of a classic environmental disease. Exp Dermatol. 2006;15:705–30.
- Pesatori AC, Consonni D, Bachetti S, Zocchetti C, Bonzini M, Baccarelli A, Bertazzi Short- and long-term morbidity and mortality in the population exposed to dioxin after the “Seveso accident”. Ind Health. 2003;41:127–38.
- Sorg O, Zennegg M, Schmid P, Fedosyuk R, Valikhnovskyi R, Gaide O, Kniazevych V, Saurat 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) poisoning in Victor Yushchenko: identifcation and measurement of TCDD metabolites. Lancet. 2009;374:1179–85.
- Kushwaha P, Kumar H, Kulkarni S, Ghorpade Chloracne in a farming family. Skinmed. 2017;15:485–8.
- Ju Q, Zouboulis CC, Xia L. Environmental pollution and acne: chloracne. Dermatoendocrinol. 2009;1:125–8.
- Kaya G, Saxer-Sekulic N, Kaya A, Sorg O, Boespfug A, Thomas L, Saurat JH. RASopathic comedone-like or cystic lesions induced by vemurafenib: a model of skin lesions similar but not identical to those induced by dioxins J Eur Acad Dermatol Venereol. 2018;32:1368–72.
- Saurat JH, Kaya G, Saxer-Sekulic N, Pardo B, Becker M, Fontao L, Mottu F, Carraux P, Pham XC, Barde C, et The cutaneous lesions of dioxin exposure: lessons from the poisoning of Victor Yushchenko. Toxicol Sci. 2012;125:310– 7.
- Saurat JH, Sorg O. Chloracne, a misnomer and its Dermatology. 2010;221:23–6.
- Patterson AT, Tian FT, Elston DM, Kaffenberger Occluded cigarette smoke exposure causing localized chloracne-like comedones. Dermatology. 2015;231:322–5.
- Cohen Sorafenib-associated facial acneiform eruption. Dermatol Ther (Heidelb). 2015;5:77– 86.
- Birnbaum Dioxin and the AH receptor: synergy of discovery. Curr Opin Toxicol. 2017;2:120–3.
- Forrester AR, Elias MS, Woodward EL, Graham M, Williams FM, Reynolds NJ. Induction of a chloracne phenotype in an epidermal equivalent model by 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) is dependent on aryl hydrocarbon receptor activation and is not reproduced by aryl hydrocarbon receptor knock down. J Dermatol 2014;73:10–22.
- Bock KW. 2,3,7,8-Tetrachlorodibenzo-p-dioxin (TCDD)-mediated deregulation of myeloid and sebaceous gland stem/progenitor cell Arch Toxicol. 2017;91:2295–301.
- Sutter CH, Bodreddigari S, Campion C, Wible RS, Sutter 2,3,7,8-Tetrachlorodibenzo-p- dioxin increases the expression of genes in the human epidermal differentiation complex and accelerates epidermal barrier formation. Toxicol Sci. 2011;124:128–37.
- Ju Q, Fimmel S, Hinz N, Stahlmann R, Xia L, Zouboulis CC. 2,3,7,8-Tetrachlorodibenzo-p- dioxin alters sebaceous gland cell differentiation in vitro. Exp Dermatol. 2011;20:320–5
- Furue M, Tsuji Chloracne and hyperpigmentation caused by exposure to hazardous aryl hydrocarbon receptor ligands. Int J Environ Res Public Health. 2019;16
- Muku GE, Blazanin N, Dong F, Smith PB Thiboutot D, Gowda K, Amin S, Murray IA, Perdew Selective ah receptor ligands mediate enhanced SREBP1 proteolysis to restrict lipogenesis in sebocytes. Toxicol Sci. 2019;
- Bock Toward elucidation of dioxin- mediated chloracne and Ah receptor functions. Biochem Pharmacol. 2016;112:1–5.
- Furue M, Fuyuno Y, Mitoma C, Uchi H, Tsuji Therapeutic agents with AHR inhibiting and NRF2 activating activity for managing chloracne. Antioxidants (Basel). 2018;7
- Rudyak SG, Usakin LA, Tverye EA, Orekhov AS, Belushkina NN, Paus R, Paltsev MA, Panteleyev Retinoic acid co-treatment aggravates severity of dioxin-induced skin lesions in hairless mice via induction of infammatory response. Biochem Biophys Res Commun. 2018;506:854–61.
- Jemec GB, Linneberg A, Nielsen NH, Frølund L, Madsen F, Jørgensen Have oral contraceptives reduced the prevalence of acne? A population- based study of acne vulgaris, tobacco smoking and oral contraceptives. Dermatology. 2002;204:179–84.
- Di Landro A, Cazzaniga S, Parazzini F, Ingordo V, Cusano F, Atzori L, Cutrì FT, Musumeci ML, Zinetti C, Pezzarossa E, et al. Family history, body mass index, selected dietary factors, menstrual history, and risk of moderate to severe acne in adolescents and young J Am Acad Dermatol. 2012;67:1129–35.
- Dreno B, Shourick J, Kerob D, Bouloc A, Taïeb The role of exposome in acne: results from an international patient survey. J Eur Acad Dermatol Venereol. 2020;34:1057–64.
- Rombouts S, Nijsten T, Lambert J. Cigarette smoking and acne in adolescents: results from a cross-sectional J Eur Acad Dermatol Venereol. 2007;21:326–33.
- Klaz I, Kochba I, Shohat T, Zarka S, Brenner S. Severe acne vulgaris and tobacco smoking in young men. J Invest Dermatol. 2006;
- Schäfer T, Nienhaus A, Vieluf D, Berger J, Ring Epidemiology of acne in the general population: the risk of smoking. Br J Dermatol. 2001;145:100–4.
- Capitanio B, Sinagra JL, Ottaviani M, Bordignon V, Amantea A, Picardo Smoker’s acne: a new clinical entity? Br J Dermatol. 2007;157:1070–1.
- Capitanio B, Sinagra JL, Ottaviani M, Bordignon V, Amantea A, Picardo M. Acne and smoking. 2009;1:129–35.
- Burns DM. Cigarettes and cigarette smoking. Clin Chest Med. 1991;12:631–42.
- Theilig C, Bernd A, Ramirez-Bosca A, Görmar FF, Bereiter-Hahn J, Keller-Stanislawski B, Sewell AC, Rietbrock N, Holzmann Reactions of human keratinocytes in vitro after application of nicotine. Skin Pharmacol. 1994;7:307–15.
- Kurzen H, Schallreuter KU. Novel aspects in cutaneous biology of acetylcholine synthesis and acetylcholine receptors. Exp Dermatol. 2004;13 Suppl 4:27–30.
- Di Carlo A, Ippolito F. Early effects of cigarette smoking in hypertensive and normotensive An ambulatory blood pressure and thermographic study. Minerva Cardioangiol. 2003;51:387–93.
- Monfrecola G, Riccio G, Savarese C, Posteraro G, Procaccini EM. The acute effect of smoking on cutaneous microcirculation blood fow in habitual smokers and nonsmokers. Dermatology. 1998;197:115–8.
- Sopori ML, Kozak W, Savage SM, Geng Y, Kluger MJ. Nicotine-induced modulation of T Cell function. Implications for infammation and Adv Exp Med Biol. 1998;437:279–89.
- Sopori ML, Kozak W, Savage SM, Geng Y, Soszynski D, Kluger MJ, Perryman EK, Snow Effect of nicotine on the immune system: possible regulation of immune responses by central and peripheral mechanisms. Psychoneuroendocrinology. 1998;23:189–204.
- Ortiz A, Grando Smoking and the skin. Int J Dermatol. 2012;51:250–62.
- Hu T, Pan Z, Yu Q, Mo X, Song N, Yan M, Zouboulis CC, Xia L, Ju Q. Benzo(a)pyrene induces interleukin (IL)-6 production and reduces lipid synthesis in human SZ95 sebocytes via the aryl hydrocarbon receptor signaling pathway. Environ Toxicol Pharmacol. 2016;43:54–60.
- Tsuji G, Takahara M, Uchi H, Takeuchi S, Mitoma C, Moroi Y, Furue An environmental contaminant, benzo(a)pyrene, induces oxidative stress-mediated interleukin-8 production in human keratinocytes via the aryl hydrocarbon receptor signaling pathway. J Dermatol Sci. 2011;62:42–9.
- Capitanio B, Sinagra JL, Bordignon V, Cordiali Fei P, Picardo M, Zouboulis Underestimated clinical features of postadolescent acne. J Am Acad Dermatol. 2010;63:782–8.
- Crivellari I, Sticozzi C, Belmonte G, Muresan XM, Cervellati F, Pecorelli A, Cavicchio C, Maioli E, Zouboulis CC, Benedusi M, et SRB1 as a new redox target of cigarette smoke in human sebocytes. Free Radic Biol Med. 2017.
- Ono Y, Torii K, Fritsche E, Shintani Y, Nishida E, Nakamura M, Shirakata Y, Haarmann- Stemmann T, Abel J, Krutmann J, et al. Role of the aryl hydrocarbon receptor in tobacco smoke extract-induced matrix metalloproteinase-1 Exp Dermatol. 2013;22:349–53.
- Fu PP, Xia Q, Sun X, Yu H. Phototoxicity and environmental transformation of polycyclic aromatic hydrocarbons (PAHs)-light-induced reactive oxygen species, lipid peroxidation, and DNA damage. J Environ Sci Health C Environ Carcinog Ecotoxicol 2012;30:1–41.
- Coal tars and coal-tar Rep Carcinog 2011, 12:111–3.
- Moustafa GA, Xanthopoulou E, Riza E, Linos Skin disease after occupational dermal exposure to coal tar: a review of the scientifc literature. Int J Dermatol. 2015;54:868–79.
- Smits JPH, Ederveen THA, Rikken G, van den Brink NJM, van Vlijmen-Willems I, Boekhorst J, Kamsteeg M, Schalkwijk J, van Hijum S, Zeeuwen P, et Targeting the cutaneous microbiota in atopic dermatitis by coal tar via AHR-dependent induction of antimicrobial peptides. J Invest Dermatol. 2020;140:415– 424.e410.
- Roelofzen JH, Aben KK, van der Valk PG, van Houtum JL, van de Kerkhof PC, Kiemeney LA. Coal tar in dermatology. J Dermatolog Treat. 2007;18:329–34