Để tải bài viết Liệu pháp đèn LED và LASER mức độ thấp: cơ chế hoạt động, chỉ định trong da liễu PDF mời các bạn click vào link ở đây.
(Light Emitting Diodes and Low Level Laser Light Therapy).
Tác giả: Caiwei Zheng, Ali Rajabi-Estarabadi, Melanie M. Hirsch, and Keyvan Nouri.
Dịch: Bác sĩ da liễu Trương Tấn Minh Vũ.
Cơ chế hoạt động
Liệu pháp laser mức độ thấp
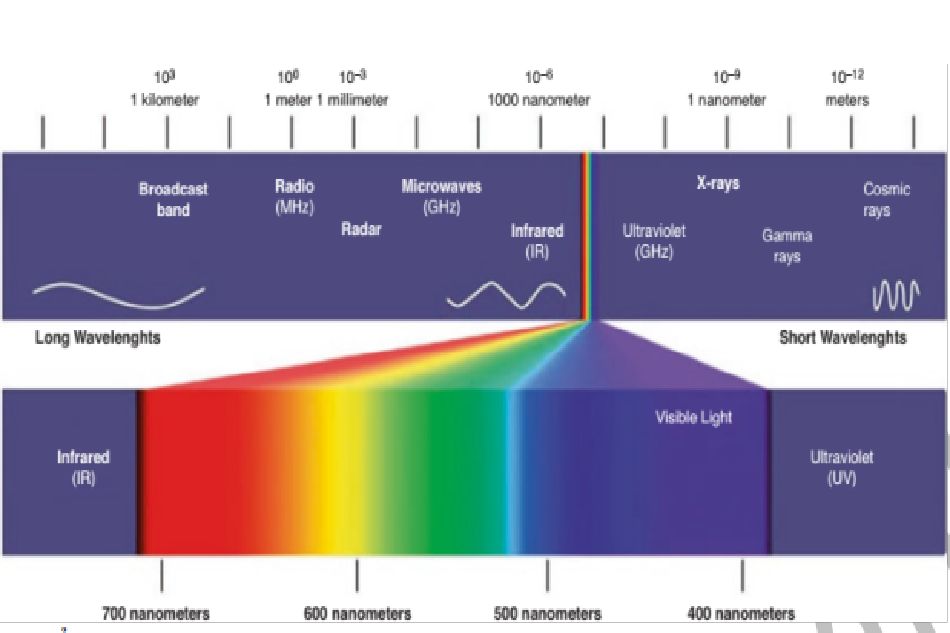
Các thuật ngữ liệu pháp laser mức độ thấp (low level laser therapy, LLLT), quang trị liệu (phototherapy) và quang điều biến (photobiomodulation) đôi khi được sử dụng thay thế cho nhau để chỉ việc sử dụng các photon trong bức xạ không sinh nhiệt để thay đổi hoạt động sinh học của tế bào [1]. LLLT thường sử dụng ánh sáng có bước sóng từ 390 nm đến 1100 nm (Hình 8.1a.). Nó được gọi là “mức thấp” vì sử dụng ánh sáng ở mật độ công suất thấp hơn (<100 mW/cm2) và mật độ năng lượng (0,04–50 J/cm2), không giống như laser được dùng để bóc tách, cắt hoặc đông đặc mô [1, 2]. LLLT có thể sử dụng nguồn sáng nhất quán (ví dụ: laser), nguồn sáng không nhất quán (ví dụ: đèn có màng lọc hoặc diode phát quang-LED) hoặc kết hợp cả hai [1]. Quang điều chế bằng LLLT có tác dụng rộng và các cơ chế hoạt động cụ thể vẫn chưa được hiểu rõ. Nói chung, quang điều chế ở công suất thấp hơn liên quan đến sự kích thích và ở mức cao hơn có liên quan đến việc ức chế chuyển hóa tế bào.
Laser phát ánh sáng đỏ và hồng ngoại gần có bước sóng tương ứng với phổ hấp thụ của các chromophore chủ yếu của ty thể, đặc biệt là cytochrome c oxidase của chuỗi hô hấp [3]. Năng lượng ánh sáng được hấp thụ có thể kích thích các electron trong chromophore nhảy từ quỹ đạo năng lượng thấp sang quỹ đạo năng lượng cao hơn, sau đó dẫn đến một loạt các hiệu ứng theo dòng ở cấp độ phân tử, tế bào và mô [1, 2]. Hiệu ứng theo dòng này được giả thuyết là đạt được thông qua sự phân ly quang học của oxit nitric ức chế từ cytochrome c oxidase, dẫn đến tăng cường hoạt động của enzym trong vận chuyển electron, hô hấp ty thể và sản xuất ATP [1, 4]. LLLT cũng thay đổi trạng thái oxy hóa khử của tế bào, gây ra sự kích hoạt của nhiều con đường tín hiệu nội bào thông qua việc kích hoạt các yếu tố phiên mã như: Yếu tố hạt nhân kappa B (Nuclear factor kappa B, NFkB), Yếu tố cảm ứng giảm oxy (Hypoxia inducible factor, HIF-1α) và ERK / FOXM1 (Hình 8.1b.) [2, 4].
![Hình 8.1 (a) Phổ hấp thụ đối với chromophore sinh học của máu (oxyhemoglobin và deoxyhemoglobin) [26] (b) Cơ chế hoạt động của liệu pháp laser mức thấp (LLLT) và diode phát quang (LED). LLLT- Liệu pháp laser mức độ thấp, LEDT- Liệu pháp LED, ROS-các loại oxy phản ứng, NO- Nitric oxide, ATP- Adenosine triphosphate](https://tapchidalieu.com/wp-content/uploads/2022/01/hinh_8.jpg)
LED
Quang trị liệu bằng diode phát sáng là một phương thức được giới thiệu gần đây thuộc phạm trù của LLLT. Trong công nghệ LED, các chip bán dẫn hiệu suất cao nằm trên bề mặt phản chiếu tạo ra ánh sáng không nhất quán, không chuẩn trực khi dòng điện đi qua [5, 6]. Các electron tái kết hợp với các lỗ trống electron trong thiết bị để giải phóng năng lượng dưới dạng photon [1]. Tùy thuộc vào khoảng trống năng lượng của chất bán dẫn, các bước sóng ánh sáng khác nhau được tạo ra trong dải khoảng 255–1300 nm, tương ứng với các dải cực tím, khả kiến và hồng ngoại gần của quang phổ điện từ [5, 6]. Ánh sáng LED cũng ảnh hưởng đến quá trình trao đổi chất của tế bào bằng cách tác động lên ty thể để kích thích các phản ứng quang hóa nội bào [5, 6]. Các thuộc tính của ánh sáng phát ra và cách cung cấp quyết định tác động lên các tế bào. Các đèn LED có sẵn trên thị trường có thể được thiết lập để cung cấp liên tục hoặc theo kiểu quang điều chế, với các xung và thời lượng cụ thể [6]. Các bước sóng cũng có thể được thiết lập để cho ra ánh sáng đỏ, vàng, xanh lam và hồng ngoại gần [6].
Ánh sáng LED đỏ kích thích các đồng/heme sắt trung tâm của cytochrome C oxidase trong chuỗi vận chuyển electron, làm tăng các loại oxy phản ứng (ROS) và sản xuất ATP [7]. Sự thay đổi nồng độ ROS có ảnh hưởng đến việc giải phóng TGF-beta 1 và TGF-beta 3, tiếp tục tác động trên diễn tiến tạo mô sợi, làm giảm sự tăng sinh nguyên bào sợi và sinh tổng hợp collagen [7]. Nồng độ ROS cũng tác động lên các yếu tố phiên mã nhạy cảm với oxy hóa khử (ví dụ: AP-1, NF-kB, p53, v.v.) có tác động quá trình phiên mã, tăng sinh tế bào và tốc độ di chuyển, cũng như sản xuất chất nền ngoại bào [7]. Ánh sáng LED vàng được phát hiện có khả năng điều chỉnh gen collagen loại 1 (COL- I) dẫn đến tăng sản xuất collagen và sản xuất ATP thông qua sự gia tăng các cytochromes [8]. Ánh sáng vàng cũng được biết là làm giảm mức MMP-1, một mục tiêu quan trọng trong quá trình trẻ hóa da [8]. Cơ chế của ánh sáng LED xanh lam vẫn chưa được xác định rõ, nhưng người ta giả thuyết rằng nó phát huy tác dụng bằng cách trực tiếp tạo ra ROS hoặc bằng cách kích thích quang nhóm flavin trên phức hợp I của chuỗi vận chuyển điện tử ty thể [9]. Theo đó, ánh sáng xanh làm thay đổi khả năng tăng sinh nguyên bào sợi và khả năng chống oxy hóa, tín hiệu TGF-beta và biệt hóa nguyên bào sợi. Ánh sáng xanh cũng được biết đến với tác dụng lên nồng độ cytokine và chất trung gian gây viêm (Hình 8.1) [9]. Ánh sáng hồng ngoại gần hiện được biết là gây ra sự giải phóng guanylate cyclase và nitrous oxide, giúp kích thích tuần hoàn. Điều này làm thúc đẩy sự giãn mạch và sản xuất yếu tố tăng trưởng, cuối cùng khuyến khích sự hình thành mạch, một yếu tố có lợi trong việc chữa lành vết thương [6].
Chỉ định trong Da liễu
LLLT đã được nghiên cứu để sử dụng cho nhiều bệnh lý da liễu trong nhiều thập kỷ, nhưng vẫn còn đối mặt với sự hoài nghi do cơ chế hoạt động của nó còn chưa ổn định và sự tiêu chuẩn hóa các thông số liều lượng còn hạn chế [1]. Hiện tại, LLLT được biết đến với ứng dụng trong một số tình trạng như chữa lành vết thương, mọc tóc, trẻ hóa da, mụn trứng cá, bệnh vẩy nến, bệnh bạch biến, sẹo phì đại, có tiềm năng lớn để phát triển như một ứng dụng đa năng trong da liễu trong tương lai gần.
LLLT trong chữa lành vết thương
Chữa lành vết thương là một trong những ứng dụng sớm nhất của LLLT. Hiện nay, LLLT đã được công nhận là có khả năng thúc đẩy quá trình sửa chữa mô thông qua việc giải phóng các chất như histamine, serotonin và bradykinin, các chất này kích thích sản xuất ATP và ức chế sản xuất các prostaglandin gây viêm và đau [10]. Những hiệu ứng này được tăng cường hơn nữa nhờ hiệu ứng điện sinh học của tia laser dẫn đến cải thiện chức năng của bơm natri-kali (Na + / K + -ATPase), và do đó cải thiện việc duy trì điện thế màng tế bào [10]. Các ATP kết quả sau đó có thể được sử dụng để bình thường hóa các chức năng của tế bào và mô, do đó thúc đẩy quá trình sửa chữa mô nhất quán hơn [11, 12]. Về mặt lâm sàng, những thay đổi này mang lại những hiệu quả đầy hứa hẹn đối với việc chữa lành da, bao gồm: tăng tốc sửa chữa mô, tăng hình thành mô hạt, co vết thương, điều chỉnh viêm và giảm đau [11, 12].
Trelles và cộng sự đã đánh giá tác dụng của LED đối với việc chữa lành vết thương trong một nghiên cứu trên bệnh nhân nữ trải qua quá trình tái tạo bề mặt da bằng laser. 28 bệnh nhân nữ tái tạo bề mặt bằng laser Er: YAG / CO2 được điều trị bằng LLLT ngay sau khi tái tạo bề mặt và sau 72 giờ — cả hai lần với ánh sáng hồng ngoại 830 nm (55 J/cm2 ) trong 20 phút, tiếp theo là ánh sáng đỏ 633 nm (98 J/cm2 ) trong 20 phút [13]. Tất cả các bệnh nhân chỉ được điều trị ở một bên của khuôn mặt, bên còn lại được che bằng mặt nạ làm đối chứng. Ba lần điều trị bổ sung được thực hiện trong vòng ba tuần tiếp theo sau thủ thuật tái tạo bề mặt: hai trong số đó được thực hiện cách nhau 3 ngày trong tuần đầu tiên và lần cuối cùng trong tuần thứ ba [13]. Nghiên cứu báo cáo rằng nửa khuôn mặt được điều trị bằng đèn LED thấy giảm nhanh hơn 50% các vấn đề tiết dịch, đóng vảy, đau và phù nề [13]. Ngoài ra, mặc dù không có sự khác biệt đáng kể về biểu hiện của nếp nhăn, phần da được điều trị trông trẻ hơn khi được đánh giá sau 6 tháng [13]. Một số nghiên cứu tiếp theo cũng đã báo cáo kết quả nhất quán.
Chaves và cộng sự đã đánh giá việc sử dụng đèn chiếu LED-nIR trong việc chữa lành vết thương núm vú ở phụ nữ đang cho con bú. Trong nghiên cứu thử nghiệm ngẫu nhiên, có đối chứng với giả dược (N = 16), nhóm thực nghiệm (N = 8) đã được tham gia một buổi đào tạo về chăm sóc núm vú và các kỹ thuật cho con bú cùng với đèn LED hoạt động [14]. Để so sánh, nhóm đối chứng (N = 8) được thực hiện cùng một buổi đào tạo nhưng với liệu pháp quang trị liệu giả dược. Đèn LED hoạt động có các thông số sau: bước sóng 860 nm, tần số 100 Hz, công suất trung bình 50 mW, mật độ công suất 50 mW/cm2 , tổng diện tích chiếu xạ 1 cm2 , chế độ phát xung với chu kỳ làm việc 50%, và mật độ năng lượng 4 J/cm2 [14]. Thời gian áp dụng điều trị là 79 giây. Liệu pháp đèn chiếu được thực hiện hai lần một tuần trong thời gian 4 tuần, tổng cộng là 8 buổi. Khu vực tổn thương sau đó được đánh giá qua chụp ảnh kỹ thuật số và hình ảnh được phân tích bằng phần mềm Quantikov, phần mềm này tính toán diện tích tổn thương dựa trên định nghĩa của người dùng về ranh giới tổn thương [14]. Nghiên cứu báo cáo rằng nhóm thử nghiệm cho thấy sự chữa lành nhanh hơn đáng kể so với nhóm đối chứng, với việc lành hoàn toàn tổn thương đạt được trong phiên thứ tư so với phiên thứ tám đối với nhóm đối chứng. Nhóm thực nghiệm cũng cho thấy mức độ giảm đau có ý nghĩa thống kê so với nhóm chứng, được đo bằng thang đánh giá cường độ đau 11 điểm (PI-NRS).
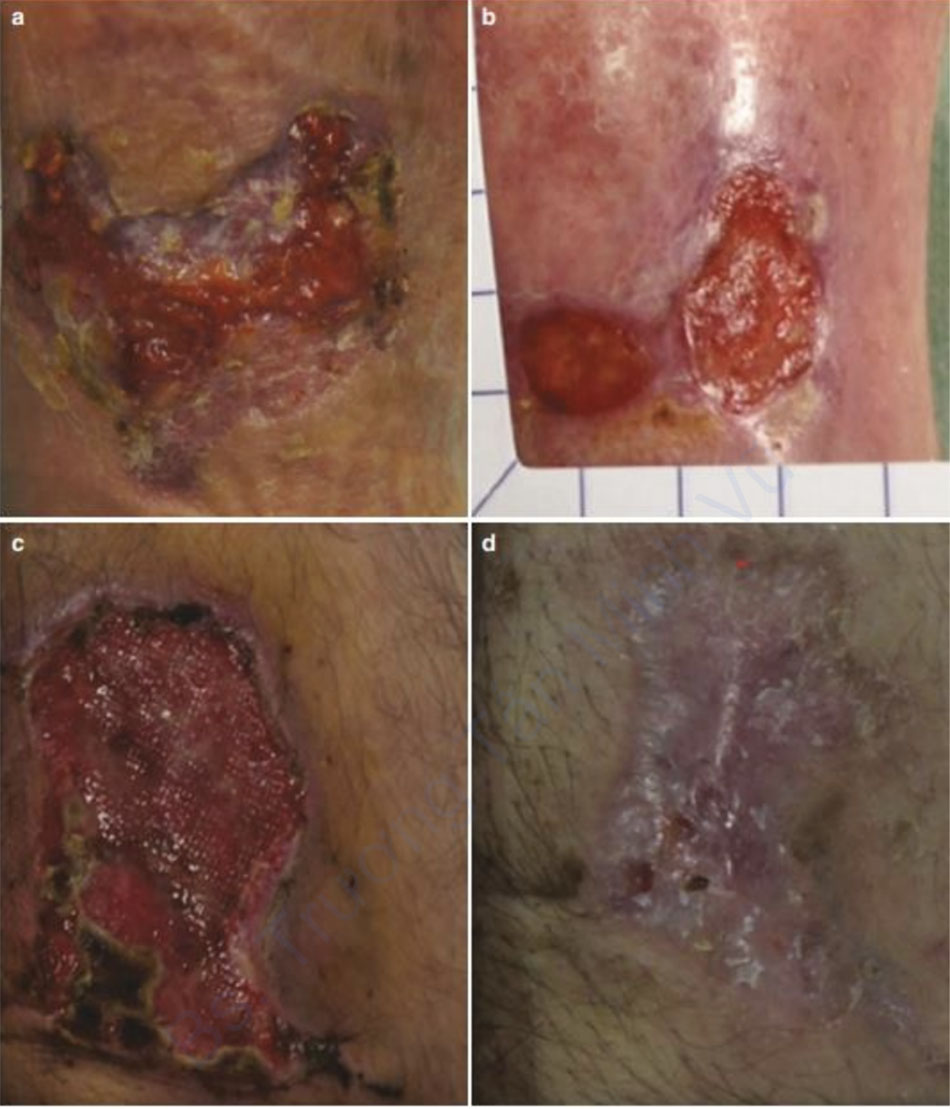
Tác dụng của đèn LED trong việc chữa lành vết bỏng gần đây cũng đã được nghiên cứu trong một nghiên cứu mù đôi. Một loạt các trường hợp bỏng độ 2 và độ 3 ở 5 bệnh nhân được điều trị bằng liệu pháp LED cường độ thấp trong phổ ánh sáng đỏ 658 nm ở 7 J/cm2 , công suất 40 mW, mật độ công suất 0,31 W/cm2 [15]. Các khu vực được điều trị được đánh giá về mặt lâm sàng và thông qua phân tích mô bệnh học trước và sau khi điều trị. Kết quả mô bệnh học cho thấy các khu vực được chiếu xạ có biểu hiện biểu mô hóa lớn hơn, với nhiều tế bào sừng hơn và tăng sinh nguyên bào sợi cũng như tăng tổng hợp collagen (Hình 8.2) [15].
Tác dụng của LLLT đối với các vết thương mãn tính, chẳng hạn như loét tĩnh mạch cũng đã được nghiên cứu. Trong số các nghiên cứu có sẵn, một nghiên cứu đã điều trị tổng cộng 68 bệnh nhân bị loét chân Meggitt-Wagner độ I mãn tính (hơn 4 tuần) do bệnh đái tháo đường loại 2. Những người tham gia được chia ngẫu nhiên thành hai nhóm 34 người [16]. Nhóm điều trị được điều trị bằng LLLT 660 và 850 nm ở 2–4 J/cm2 (tùy thuộc vào kích thước vết loét) hàng ngày trong 15 ngày, trong khi nhóm chứng được điều trị bằng liệu pháp thông thường. Nghiên cứu báo cáo diện tích vết loét giảm đáng kể sau phác đồ điều trị 15 ngày [16]. Điều đáng chú ý là nghiên cứu này, cùng với những nghiên cứu khác đưa ra kết quả tích cực tương tự, bị giới hạn ở kích thước mẫu nhỏ và thiếu sàng lọc để loại trừ những người nhanh lành thương [11]. Do đó, các thử nghiệm lâm sàng lớn hơn với sự sàng lọc thích hợp là cần thiết để nghiên cứu thêm về hiệu quả. Cho đến nay, không có tác dụng phụ đáng kể nào được báo cáo đối với bất kỳ phương pháp điều trị vết thương bằng LLLT.
LLLT trong mọc tóc
Việc sử dụng LLLT để kích thích tóc mọc lại được hỗ trợ mạnh mẽ hơn, đặc biệt là trong điều trị chứng rụng tóc androgen (androgenic alopecia, AGA) và rụng tóc từng mảng (alopecia areata, AA). Sự phát triển của tóc được chia thành ba giai đoạn: anagen, giai đoạn tăng trưởng tích cực; catagen, giai đoạn chuyển tiếp; và telogen, giai đoạn nghỉ. Người ta đã phát hiện ra rằng biện pháp quang điều chế dùng cho da đầu có thể khuyến khích các nang tóc chuyển từ giai đoạn telogen sang giai đoạn anagen và tăng thời gian của giai đoạn anagen để tăng cường sự phát triển của tóc, mang lại mái tóc dày và nhiều sắc tố hơn [2, 4]. Cơ chế chính xác vẫn chưa được thiết lập đầy đủ, nhưng gần đây, các cơ chế mới đã được đề xuất. Các nghiên cứu báo cáo rằng sự kích hoạt con đường tín hiệu Wnt10b / β-catenin có thể chịu trách nhiệm tạo ra giai đoạn anagen của nang lông, vì sự biểu hiện của Wnt10b và β-catenin cao hơn đáng kể đã được quan sát thấy khi điều trị LLLT trên mô hình chuột [17, 18]. Con đường Wnt10b và β-catenin và sự kích hoạt con đường ERK có thể giải thích cho việc chiếu xạ gây ra sự tăng sinh tế bào nang tóc bên ngoài và ức chế quá trình chết tự nhiên của nó, có thể là cơ chế về khả năng tác động của LLLT đối với sự phát triển của tóc [18].
Một đánh giá có hệ thống và phân tích tổng hợp đã được thực hiện trên các thử nghiệm lâm sàng ngẫu nhiên nghiên cứu tác dụng kích thích của LLLT đối với sự phát triển của tóc và kết luận rằng LLLT là một phương pháp điều trị hiệu quả cho chứng rụng tóc ở nam giới [19]. Nghiên cứu đáng chú ý nhất để điều trị AGA là thử nghiệm lâm sàng đối với HairMax LaserComb®, được thử nghiệm bởi Leavitt và cộng sự trong một thử nghiệm ngẫu nhiên mù đôi, có kiểm soát với thiết bị giả trên 110 bệnh nhân AGA nam [20]. Thiết bị này là một thiết bị LLLT cầm tay phát 9 chùm tia ở bước sóng 655 nm (+/− 5%) tới da đầu của người dùng trong khi chia tóc bằng lược đi kèm [20]. Bệnh nhân được hướng dẫn sử dụng thiết bị ba lần mỗi tuần trong các phiên 15 phút trong 26 tuần [20]. Kết quả cho thấy các đối tượng trong nhóm HairMax LaserComb® có sự gia tăng có ý nghĩa thống kê về mật độ trung bình tóc đầu cuối so với nhóm đối chứng, chứng tỏ thiết bị này có hiệu quả và dung nạp tốt [20]. Tác dụng của HairMax LaserComb® đối với sự phát triển và độ bền kéo của tóc đã được thử nghiệm thêm trong một nghiên cứu của Satino và cộng sự trên 28 bệnh nhân AGA nam và 7 nữ. Bệnh nhân được hướng dẫn sử dụng LLLT tại nhà trong 6 tháng với các buổi 5–10 phút cách ngày. Kết quả được đánh giá bởi bác sĩ phẫu thuật cấy tóc có kinh nghiệm và sử dụng phần mềm đếm tóc có hỗ trợ của máy tính. Mặc dù nghiên cứu cho thấy thiết bị hoạt động mang lại kết quả tốt hơn ở nam giới, nhưng cả nam và nữ đều có sự cải thiện đáng kể về cả số lượng tóc và độ bền kéo [21]. HairMax LaserComb hiện đã được FDA chấp thuận là phương pháp điều trị an toàn cho AGA nam và nữ (Hình 8.3b) [1].
Để đánh giá điều trị chứng rụng tóc từng mảng, một nghiên cứu đã được thực hiện với 15 bệnh nhân (6 nam, 9 nữ) sử dụng Super Lizer TM, phát ra ánh sáng xung tuyến tính phân cực (600–1600 nm) ở 1,8 W [22]. Bệnh nhân được chiếu xạ điều trị trên da đầu trong 3 phút mỗi tuần một lần hoặc cách tuần một lần cho đến khi quan sát thấy tóc mọc lại ở ít nhất một nửa khu vực được chiếu xạ và carpronium chloride 5% được bôi tại chỗ hai lần mỗi ngày cho tất cả các vị trí tổn thương [22] . Kết quả nghiên cứu đã quan sát thấy tóc mọc ở vùng được chiếu xạ sớm hơn 1,6 tháng so với vùng không được chiếu ở 47% bệnh nhân [22].
![Hình 8.3 (a) Sự cải thiện mức độ trung bình sự phát triển của tóc ở những bệnh nhân được điều trị bằng mũ laser lúc ban đầu và sau 24 tuần [23]. (b) Các thiết bị ánh sáng thường được sử dụng để chữa rụng tóc](https://tapchidalieu.com/wp-content/uploads/2022/01/hinh_8.3.jpg)
LLLT trong trẻ hóa da
Đèn LED cũng có các ứng dụng thẩm mỹ, chủ yếu trong trẻ hóa da không sinh nhiệt, không bóc tách. Các bước sóng màu vàng (570–590 nm), đỏ (630–700 nm) và hồng ngoại gần (800–1200 nm) đã được sử dụng cho các hiệu ứng quang điều biến trên ty thể, kích thích tăng sinh nguyên bào sợi, tổng hợp collagen, các yếu tố tăng trưởng và sản xuất chất nền ngoại bào [24].
Cụ thể, tăng mức mRNA của interleukin-1 beta (IL-1ß), yếu tố hoại tử khối u alpha (TNF-α), phân tử kết dính gian bào 1 (ICAM-1), và liên kết 43 (Cx43) cùng với giảm IL-6 đã được được báo cáo sau khi điều trị bằng đèn LED với ánh sáng laser đỏ và hồng ngoại [25]. IL-1ß và TNF-α được cho là chịu trách nhiệm cho việc kích thích hoạt động MMP, góp phần loại bỏ các đoạn collagen bị tổn thương do ánh sáng và đến lượt nó, sinh tổng hợp collagen mới (Hình 8.4) [25]. Sự biểu hiện tăng cường của Cx43 có thể góp phần tăng cường giao tiếp tế bào giữa các nguyên bào sợi, dẫn đến sự đồng bộ cao hơn giữa các phản ứng tế bào [25]. Nói chung, những thay đổi này được cho là làm nâng và săn chắc tình trạng da lỏng lẻo và giảm nếp nhăn [24]. Đặc biệt, ánh sáng đỏ và hồng ngoại gần cũng được ghi nhận là có tác dụng bổ sung trong việc thúc đẩy tái cấu trúc lớp bì do khả năng thâm nhập sâu hơn của chúng [1, 26].
Các thử nghiệm lâm sàng cho thấy việc sử dụng đèn LED trong việc trẻ hóa da cho kết quả phần lớn được sự đồng thuận. Một thử nghiệm lâm sàng đa trung tâm đã điều trị cho 90 bệnh nhân bằng đèn LED không sinh nhiệt 590 nm ở 0,1 J/cm2 trong 8 phiên trong 4 tuần và cho thấy sự cải thiện đáng kể về biểu hiện của da bị lão hoá do ánh sáng [27]. Theo báo cáo, 90% bệnh nhân đã cải thiện ít nhất một bậc da lão hoá ánh sáng theo Fitzpatrick, với 65% bệnh nhân ghi nhận sự cải thiện về kết cấu khuôn mặt, nếp nhăn, ban đỏ nền và sắc tố [27] Điều này được củng cố bởi một thử nghiệm lâm sàng lớn hơn của Weiss, trong đó 900 bệnh nhân được điều trị bằng liệu pháp LED: 300 bệnh nhân trong số đó chỉ sử dụng LED 590 nm ở 0,10 J/cm2 , và 600 bệnh nhân trong số đó được điều trị bằng cả liệu pháp LED và quy trình trẻ hóa quang học dựa trên nhiệt [28]. Những người được điều trị chỉ với đèn LED được báo cáo kết quả tương tự.
![Hình 8.4 Các mẫu sinh thiết của vị trí không được điều trị (a, c) và bên được điều trị bằng LED 830-nm (b, d) vào 2 tuần sau phiên điều trị LED cuối cùng. Cả hai mặt được điều trị đều cho thấy mật độ sợi collagen (a, b) và elastin (c, d) cao hơn đáng kể với sự liên kết tốt, đặc biệt là ở vùng grenz, lớp biểu bì dày hơn và nhiều tế bào hơn, và lớp sừng có tổ chức tốt hơn. ([a, b]: hematoxylin và eosin, độ phóng đại gốc 100; [c, d]: elastica van Giessen, độ phóng đại ban đầu 200) [25]](https://tapchidalieu.com/wp-content/uploads/2022/01/mau_sinh_triet.jpg)
Những kết quả đầy hứa hẹn này đã được hỗ trợ thêm bởi một nghiên cứu lớn hơn, ngẫu nhiên, mù đôi, có đối chứng, được thiết kế để xác nhận thêm hiệu quả của đèn LED 830 nm và 633 nm. 76 đối tượng có nếp nhăn trên mặt được phân ngẫu nhiên vào một trong 3 nhóm được điều trị ở một bên mặt, hoặc nhóm thứ tư được điều trị giả ở cùng một bên mặt [25]. Trong số ba nhóm đầu tiên, các đối tượng được điều trị bằng cách sử dụng riêng đèn LED 830 nm (126 J/cm2 ), riêng đèn LED 633 nm (66 J/cm2 ), hoặc đèn LED 830 nm, 633 nm lần lượt tương ứng [25]. Một sự khác biệt đáng kể đã được báo cáo giữa các nhóm thực nghiệm so với đối chứng: 95,2%, 72,3% và 95,5% đối tượng cho thấy sự cải thiện so với 13,3% đối tượng trong nhóm đối chứng (Hình 8,4) [25].
Barolet và cộng sự đã đánh giá tác động của điều trị bằng ánh sáng đối với làn da lão hóa/ lão hóa do ánh sáng. Nghiên cứu theo dõi 12 đối tượng được điều trị bằng ánh sáng LED 660 nm. Và tương tự, kết quả được báo cáo với 90% đối tượng cho thấy giảm độ sâu nếp nhăn và độ nhám bề mặt (dựa trên định lượng), và 87% đối tượng báo cáo giảm chỉ số nếp nhăn Fitzpatrick [31].
LLLT trong mụn trứng cá
Mụn trứng cá là tình trạng viêm của các đơn vị tuyến bã liên quan đến việc tăng sản xuất bã nhờn, tăng sừng hóa, tiết ra chất trung gian gây viêm và sự phát triển quá mức của vi khuẩn Propionibacterium acnes (P. acnes) [32]. LLLT ở bước sóng 415 nm (xanh lam) và 630 nm (đỏ) phù hợp với đỉnh hấp thụ của porphyrin do P. acnes tạo ra và được sử dụng để điều trị mụn trứng cá do khả năng hình thành ROS cũng như đặc tính chống viêm của nó [6 , 33].
Chiếu ánh sáng xanh đã được chứng minh là đặc biệt hiệu quả trong việc tiêu diệt P. acnes bằng cách quang hoạt các porphyrin nội sinh, dẫn đến hình thành các gốc tự do phá hủy màng tế bào vi khuẩn [34]. Ba mươi bệnh nhân, bị mụn trứng cá nhẹ đến trung bình, được điều trị bằng đèn LED ánh sáng xanh 415 nm trong một nghiên cứu của Morton và cộng sự. Các phương pháp điều trị được thực hiện dưới dạng các phiên 8 phút, 10 phút hoặc 20 phút trong khoảng thời gian bốn tuần, làm giảm số lượng tổn thương viêm 25%, 53% và 60%, ở 5, 8 và 12 tuần tương ứng [35]. Hiệu quả trên các tổn thương không viêm là rất ít. Một thử nghiệm lâm sàng khác được thực hiện bởi Tremblay đã nghiên cứu việc sử dụng đèn LED xanh dương (415 nm) trong 20 phút, hai lần mỗi tuần trong 4-8 tuần và báo cáo giảm 50% số lượng tổn thương với 9 bệnh nhân hoàn toàn hết tổn thương.
Liệu pháp ánh sáng đỏ ở liều thấp cũng đã được nghiên cứu để điều trị mụn trứng cá trong các nghiên cứu khác nhau. Một nghiên cứu mô hình in-vitro đã sử dụng axit oleic (OA) để gây ra phản ứng viêm trong mô tương đương biểu bì của con người, mô hình này bắt chước các tổn thương mụn trứng cá trên cơ thể người [32]. Kết quả cho thấy rằng ánh sáng đỏ ở 0,2–1,2 J/cm2 cho thấy tác dụng ức chế giải phóng IL-1α do OA gây ra, và giảm nhẹ axit béo không no gây ra sự dày lên và tăng sừng hóa của lớp sừng [32].
Liệu pháp ánh sáng đỏ cũng được chứng minh là làm giảm các khiếm khuyết hàng rào do OA gây ra, một yếu tố có lợi gợi ý ứng dụng tiềm năng của ánh sáng đỏ trong điều trị mụn trứng cá.
Liệu pháp quang động với ánh sáng xanh và đỏ
Các loại chất cảm quang khác nhau, chẳng hạn như axit 5-aminolevulinic (ALA) và metyl este aminolevulinate (MAL), có sẵn cho liệu pháp đèn LED và việc sử dụng các chất cảm quang này kết hợp với liệu pháp ánh sáng được gọi là liệu pháp quang động (PDT).
[36]. Việc sử dụng ánh sáng xanh trong liệu pháp quang động axit aminolevulinic (ALA- PDT) và sử dụng ánh sáng đỏ trong liệu pháp quang động methyl aminolevulinate (MALPDT) để điều trị mụn trứng cá cũng đã được khám phá. Kết quả của nó được so sánh với kết quả của liệu pháp LED đơn thuần. Trong một nghiên cứu so sánh liệu pháp ánh sáng xanh đơn thuần và với ALA-PDT, sự khác biệt về kết quả không có ý nghĩa thống kê [37]. Không có thay đổi đáng kể về bài tiết bã nhờn, ban đỏ hoặc chỉ số melanin được ghi nhận ở nhóm được điều trị bằng cả ALA-PDT và ánh sáng xanh. Tuy nhiên, các tác dụng phụ như đau, châm chích, bong tróc da, ngứa, chảy dịch và mụn mủ ở nhóm ALA-PDT nghiêm trọng hơn so với chỉ điều trị bằng ánh sáng xanh [37]. Các kết quả tương tự cũng được báo cáo trong một loạt các nghiên cứu so sánh MAL-PDT với liệu pháp ánh sáng đỏ và đèn LED ánh sáng đỏ đơn thuần. Phân tích tổng hợp các nghiên cứu cho thấy rằng bốn lần MAL từ 400 mg/g đến 160 mg/g kết hợp với ánh sáng đỏ, ít tác động đến sự thay đổi về số lượng tổn thương viêm so với giả dược kết hợp với ánh sáng đỏ khi được đánh giá ở tuần thứ 6 [38]. MAL-PDT kết hợp ánh sáng đỏ không liên quan đến tỷ lệ tác dụng phụ nghiêm trọng cao hơn so với giả dược hoặc không điều trị [38]. Một trong những thiết bị thường được sử dụng cho các liệu pháp ánh sáng xanh và đỏ (Hình 8.5).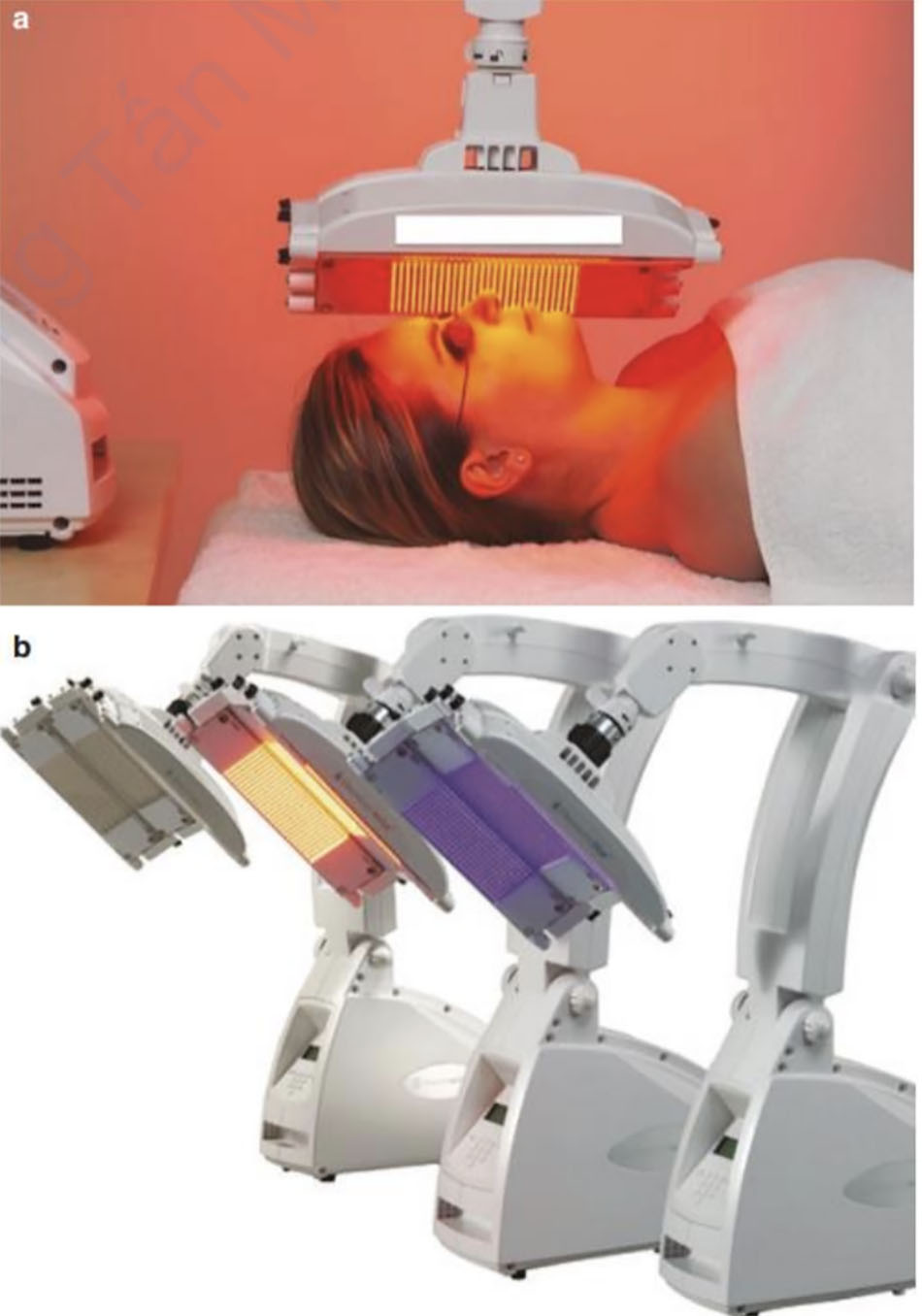
LLLT trong bệnh vẩy nến
Cơ chế bệnh sinh của bệnh vẩy nến được biết là có liên quan đến tương tác bất thường giữa các hệ miễn dịch tự nhiên, như tế bào T và tế bào sừng [39]. Trong bệnh vẩy nến, các tế bào miễn dịch này giải phóng dư thừa các yếu tố tiền viêm, dẫn đến việc kích hoạt không kiểm soát được phản ứng miễn dịch, bao gồm cả con đường tín hiệu của yếu tố hạt nhân-κB (NFkB) và sự biệt hóa của tế bào T trợ giúp (Th) đối với tế bào Th1 và/hoặc Th17 [39]. LLLT của một số bước sóng đã được chứng minh là có tác dụng hữu ích trong việc điều hoà quá trình này.
Ánh sáng xanh dương ở bước sóng 400–480 nm đã được chứng minh là làm giảm hoạt động tăng sinh của tế bào sừng, giảm phản ứng miễn dịch của tế bào T, và do đó cải thiện bệnh vẩy nến thể mảng nhẹ [40]. Trong một nghiên cứu của Weinstabl và cộng sự, 37 bệnh nhân bị vảy nến thể nhẹ đến trung bình (PV) được điều trị bằng đèn LED ánh sáng xanh ở bước sóng 420 nm hoặc ở bước sóng 453 nm một lần mỗi ngày trong 4 tuần [41]. Các mảng được đánh giá bằng chỉ số Local Psoriasis Severity Index (LPSI) và cả hai nhóm đều cho thấy sự cải thiện đáng kể [41].
Pfaff và cộng sự cũng tiến hành một nghiên cứu dài hạn ngẫu nhiên về điều trị ánh sáng xanh cho PV nhẹ với 47 bệnh nhân sử dụng cả điều trị cường độ cao (453 nm LED 200 mW/cm2 ) và điều trị cường độ thấp (453 nm LED 100 mW/cm2 ) [40]. Nghiên cứu cho thấy sự cải thiện có ý nghĩa thống kê trong cả 2 cách cài đặt đèn LED so với các mảng đối chứng, chứng minh sự an toàn khi điều trị và sự hài lòng của bệnh nhân khi điều trị bằng ánh sáng xanh [40].
Ánh sáng đỏ (620–770 nm) và ánh sáng hồng ngoại gần (800–1200 nm) ở bước sóng dài hơn, được biết là có thể xuyên sâu vào da, cho phép nó kích thích hoạt động của ty thể và điều chỉnh giải phóng cytokine để giảm viêm [42 ]. Một nghiên cứu pilot đã kiểm tra hiệu quả của liệu pháp LED trong điều trị bệnh vẩy nến kháng trị bằng cách sử dụng kết hợp bức xạ 830 nm (hồng ngoại gần) và 630 nm (ánh sáng đỏ). Những bệnh nhân bị bệnh vẩy nến mãn tính thể mảng (n = 8) và vẩy nến thể giọt (n = 1) trong thời gian lên đến 35 năm đã được ghi danh, hầu hết trong số họ bị bệnh vẩy nến kháng với liệu pháp điều trị thông thường. Những người tham gia được điều trị tuần tự bằng hồng ngoại gần và ánh sáng đỏ trong hai buổi 20 phút cách nhau 48 giờ trong 4–5 tuần [43]. Kết quả cho thấy mức độ sạch bệnh vẩy nến dao động từ 60 đến 100% với sự hài lòng của bệnh nhân cao và không có tác dụng phụ bất lợi [43]. Kết luận, những báo cáo tích cực này cho thấy nhiều hứa hẹn trong việc áp dụng LLLT trong điều trị bệnh vẩy nến. Ưu điểm của nó là không xâm lấn với ít tác dụng phụ đáng được khám phá thêm trong điều trị bệnh vẩy nến.
LLLT trong bệnh bạch biến
Bạch biến là một bệnh rối loạn sắc tố mắc phải mà cơ chế tiềm ẩn của việc thiếu tế bào hắc tố chức năng vẫn đang được nghiên cứu. Một số tiến bộ đã cho thấy sự tham gia của các tế bào sừng, nguyên bào sợi, nguyên bào hắc tố và tế bào hắc tố, và do đó kích thích các tế bào biểu bì và bì này được cho là một lựa chọn điều trị khả thi [1].
Việc sử dụng LLLT như một liệu pháp thay thế cho bệnh bạch biến có từ năm 1997, khi Mandel đã báo cáo tình trạng phục hồi sắc tố đáng chú ý sau khi điều trị 18 bệnh nhân bạch biến bằng liệu pháp laser HeliumNeon (He-Ne) năng lượng thấp (632 nm, 25 mW/cm2 ) [44]. Sau đó, sử dụng laser He-Ne đã được đề xuất cho bệnh bạch biến loại phân đoạn, một biến thể được biết là có khả năng kháng cao hơn các liệu pháp thông thường [45]. Trong nghiên cứu của Yu và cộng sự, tế bào sừng và nguyên bào sợi được nuôi cấy được điều trị bằng laser He-Ne ở 0,5– 1,5 J/cm2 [45]. Việc chiếu xạ dẫn đến sự tăng đáng kể giải phóng bFGF ở cả tế bào sừng và nguyên bào sợi cũng như tăng giải phóng NGF từ tế bào sừng [45]. Được áp dụng trên lâm sàng, kết quả duy trì lâu dài: 30 bệnh nhân được điều trị bằng laser HeNe (632,8 nm) được sử dụng cục bộ ở 3 J/cm2 , 1,0 mW với kích thích điểm 1-2 lần mỗi tuần, và tái tạo sắc tố quanh tổn thương và quanh nang rõ rệt (> 50%) được quan sát thấy ở 60% bệnh nhân [45]. Nghiên cứu của Lan và cộng sự đã giúp làm rõ cơ sở lý thuyết cho các kết quả tích cực trong điều trị bệnh bạch biến. Nghiên cứu chỉ ra rằng laser He-Ne (632,8 nm, 1 J/cm2 và 10 mW) kích thích sự tăng sinh tế bào hắc tố thông qua tăng cường biểu hiện α2β1 và biểu hiện protein liên kết yếu tố phản ứng chu kỳ-AMP (CREB), một chất điều chỉnh chính của sự phát triển tế bào hắc tố [46 ].
Gần đây, ảnh hưởng của LLLT lên siêu cấu trúc và số lượng melanosome trong tế bào hắc tố của người bình thường được nuôi cấy đã được nghiên cứu. Trong một nghiên cứu của Khalid và cộng sự, các tế bào hắc tố được chiếu xạ bằng liệu pháp ánh sáng ở mức năng lượng 2,0 J/cm2 , sử dụng tia laser xanh lam (457 nm), đỏ (635 nm) hoặc tia cực tím (UV) (355 nm) và so với nhóm đối chứng được điều trị giả [47]. Các giai đoạn phát triển của melanosome được quan sát và đếm số lượng của chúng. Số lượng melanosomes giai đoạn I cao hơn đáng kể được báo cáo trong các tế bào được điều trị bằng LLLT so với đối chứng [47]. Điều trị bằng ánh sáng laser đỏ mang lại một lượng lớn hơn so với các phương pháp khác, cho thấy sự kích thích hình thành hắc tố hiệu quả hơn [47]. Nhóm nghiên cứu tương tự cũng đã thử nghiệm tác động của LLLT khác nhau đối với sự di chuyển của tế bào hắc tố ở người trong ống nghiệm. Nghiên cứu báo cáo rằng LLLT ở mật độ năng lượng thấp có những tác động đầy hứa hẹn trong việc tăng khả năng tồn tại, tăng sinh và di chuyển của tế bào hắc tố, trong khi LLLT ở mật độ năng lượng cao hơn mang lại kết quả không kích thích [48]. Với những tiến bộ này, ứng dụng lâm sàng của LLLT trong bệnh bạch biến sẽ được hưởng lợi từ các thử nghiệm lâm sàng lớn hơn.
LLLT trong sẹo: sẹo phì đại và sẹo lồi
Sẹo phì đại và sẹo lồi từ phẫu thuật, chấn thương hoặc mụn trứng cá từ lâu đã trở thành một thách thức trong da liễu mặc dù có rất nhiều lựa chọn điều trị. Cơ chế bệnh sinh của những tình trạng này được cho là liên quan đến sự mất cân bằng giữa tốc độ sinh tổng hợp và suy thoái collagen dẫn đến tăng sinh nguyên bào sợi và lắng đọng collagen dư thừa [1]. Các nghiên cứu gần đây đã đề xuất rằng việc điều hòa không đầy đủ các con đường tín hiệu interleukin (IL) -6 và sự biểu hiện của yếu tố tăng trưởng biến đổi beta-I (TGF-βI) có vai trò quan trọng trong quá trình này, làm ức chế con đường IL-6 và / hoặc TGF- βI là một mục tiêu điều trị tiềm năng [49–53]. Vì một số bước sóng trong phổ LED-RL (633 nm) và phổ hồng ngoại (830 nm) đã được chứng minh là dẫn đến sự giảm IL-6 (mặc dù gia tăng IL- 1ß và TNFa), LLLT đã được đề xuất là dự phòng để tránh hoặc làm giảm sự hình thành sẹo phì đại hoặc sẹo lồi [25].
Trong một nghiên cứu case study, hiệu quả của LLLT được khảo sát trên ba bệnh nhân có các loại sẹo khác nhau. Mỗi người, một bên sẹo trong sẹo hai bên được điều trị hàng ngày tại nhà với NIR — LED 805 nm ở 30 mW/cm2 và 27 J/cm2 [54]. Trong trường hợp đầu tiên, điều trị bằng đèn LED được áp dụng cho sẹo lồi tuyến tính trước tai do thủ thuật căng da mặt, đã được điều trị bằng phẫu thuật để chỉnh sửa sẹo [54]. Trường hợp thứ hai được thực hiện trên một bệnh nhân có sẹo phì đại trên ngực do mụn trứng cá, sử dụng laser CO2 để tái tạo bề mặt [54]. Trường hợp thứ ba được điều trị cho một bệnh nhân có sẹo phì đại ở lưng sau khi cắt bỏ, cũng được điều trị bằng laser CO2 để tái tạo bề mặt [54]. Kết quả cho thấy sự cải thiện đáng kể trên vết sẹo được điều trị bằng đèn LED nIR so với bên sẹo đối chứng [54]. Không có tác dụng phụ đáng kể nào liên quan đến điều trị được báo cáo [54].
Hiệu quả của LLLT trong điều trị sẹo phì đại sau bỏng ở trẻ em đã được khám phá gần đây. Trong một thử nghiệm ngẫu nhiên có đối chứng gồm 15 trẻ em từ 2 đến 10 tuổi đã được tiến hành và kết quả được đánh giá bằng Thang điểm sẹo Vancouver (VSS). Mỗi vết sẹo trong nghiên cứu này được chia đôi. Một bên của vết sẹo được xử lý bằng laser Helium -Neon (bước sóng 632,8 nm, mật độ công suất 119 mW/cm2 và mật độ năng lượng 16 J/cm2 ) trong 25 phút. Cải thiện đáng kể sau khi điều trị đã được báo cáo, với điểm VSS trung bình trước khi điều trị là 9 (toàn bộ sẹo) so với 6 (toàn bộ sẹo) sau khi điều trị (Hình 8.6) [55].

LLLT trong Photoprotection
Việc áp dụng LLLT trong photoprotection (quang bảo vệ) vẫn đang ở giai đoạn đầu và vẫn đang tranh cãi. Các nghiên cứu gần đây đã đề xuất rằng việc tiếp xúc với ánh sáng hồng ngoại ở một số thông số nhất định có thể có tác dụng bảo vệ da bằng cách kích hoạt các phản ứng bảo vệ/sửa chữa đối với tia UV (Bảng 8.1) [1]. Tuy nhiên, hiệu quả mang tính tham số cao và các quan điểm mâu thuẫn cũng tồn tại [2]. Sự khác biệt này có thể được giải thích bởi thực tế là chỉ một phạm vi cụ thể của sự kết hợp tối ưu giữa chiếu xạ và thời gian kích thích mới mang lại kết quả mong muốn: liều dưới tối ưu dẫn đến thiếu phản ứng, liều cao hơn tối ưu dẫn đến ức chế phản ứng – hiện tượng được gọi là liều đáp ứng hai pha [2]. Mặc dù có một số bất đồng về cơ chế tự nhiên của da để chuẩn bị cho tác hại của tia UV, một số nghiên cứu đã chỉ ra rằng bức xạ hồng ngoại gần không kết hợp (NIR) (700- 2000 nm) chuẩn bị cho tế bào chống lại tổn thương do tia UVB gây ra bằng cách ức chế quá trình tự chết do tia UVB gây ra [56–58 ]. Trong việc ngăn chặn sự hoạt hóa của caspase-9 và -3, làm giảm protein proapoptotic (tức là Bax) và tăng protein antiapoptotic (tức là, Bcl-2 hoặc Bcl-xL), IR được báo cáo là có tác dụng điều chỉnh cân bằng Bcl2 / Bax, được cho là kéo dài và tích lũy [56–58].
Bảng 8.1 Các chỉ định của LLLT
| Chỉ định | Laser | Cơ chế | Nghiên cứu | |||
| Lành thương | Ánh sáng hồng ngoại 830 nm (55 J/cm2), tiếp theo là ánh sáng đỏ 633 nm | Kích thích sản xuất ATP và ức chế sản xuất prostaglandin thông qua giải phóng histamine, serotonin và bradykinin. | Trelles và cộng sự | |||
| LED-nIR 860 nm | Chaves và cộng sự. | |||||
| Mọc tóc | HairMax 655 nm | LaserComb® | Con đường Wnt10b và β-catenin và kích hoạt con đường ERK | Leavitt và cộng sự. | ||
| Trẻ hoá da | LED 590 nm không sinh nhiệt | Tăng mức mRNA của interleukin-1 beta (IL-1ß), yếu tố hoại tử khối u alpha (TNF-α), phân tử kết dính gian bào 1 (ICAM-1), và liên kết 43
(Cx43) cùng với IL-6 giảm |
McDaniel và cộng sự.
Weiss và cộng sự |
|||
| LED 633 nm và 830 nm | Bahat và cộng sự. Lee và cộng sự. | |||||
| Mụn | Ánh sáng xanh lam 415 nm | Hình thành các gốc tự do phá hủy màng tế bào vi khuẩn P. acnes | Morton và cộng sự. | |||
| Ánh sáng đỏ 630 nm | Tác dụng ức chế giải phóng IL-1α do OA gây ra, và làm dày và tăng sừng hóa lớp sừng | Li và cộng sự. | ||||
| Vảy nến | Ánh sáng xanh lam (400– 480 nm) | Điều chỉnh con đường truyền tín hiệu của yếu tố nhân-κB (NF-kB) và sự biệt hóa của tế bào trợ giúp T (Th) | Weinstabl và cộng sự. | |||
| Ánh sáng đỏ (620-770 nm) và ánh sáng hồng
ngoại gần (800–1200 nm) |
Kích thích hoạt động của ty thể và điều chỉnh giải phóng cytokine để
giảm viêm |
Ablon và cộng sự. | ||||
| Bạch biến | Laser Heli-neon (he-ne) 632 nm | Kích thích tế bào hắc tố và tế bào sừng | Mandel và cộng sự. Yu và cộng sự. | |||
| Laser xanh lam (457 nm), đỏ (635 nm) hoặc cực tím (UV 355 nm) | Khalid và cộng sự. | |||||
| Sẹo phì Sẹo lồi | đại/ | NIR — LED 805 nm | Giảm IL-6 | Barolet và cộng sự. | ||
| Laser heli-neon 632,8 nm | Alsharnoubi cộng sự. | và | ||||
| Quang bảo vệ | NIR 700–2000 nm | Ức chế quá trình apoptosis do tia UVB gây ra | Menezes và cộng sự.
Frank và cộng sự. Applegate và cộng sự. |
|||
| Phơi sáng LED (660 nm | Tăng tiết procollagen nguyên bào sợi ở da và giảm sản xuất metalloproteinase (MMP) hoặc collagenase | Barolet và cộng sự. | ||||
Một loạt các nghiên cứu của Barolet và Boucher đã đánh giá tác dụng lâm sàng của những phát hiện như vậy. Mười ba đối tượng khỏe mạnh và hai đối tượng bị phát ban đa dạng do ánh sáng (polymorphous light eruption, PLE) đã được điều trị bằng đèn LED để kiểm tra tác dụng bảo vệ của việc xử lý bằng đèn LED (660 nm) khi được sử dụng trước khi tiếp xúc với tia cực tím [59]. Kết quả cho thấy rằng chiếu xạ LED 660 nm theo liều có hiệu quả trong việc giảm > 50% ban đỏ do tia UVB gây ra trong ít nhất một lần ở 85% đối tượng, bao gồm cả những người bị PLE [59]. Một nghiên cứu trong phòng thí nghiệm sau đó đã được thực hiện vào năm 2009, báo cáo rằng tiếp xúc với đèn LED màu đỏ đậm không kết hợp không sinh nhiệt (660 nm, chế độ phát xung tuần tự) dẫn đến sự gia tăng tiết procollagen nguyên bào sợi ở da, làm giảm metalloproteinase (MMP) hoặc sản xuất collagenase [54]. Những phát hiện này có mối tương quan với sự cải thiện đáng kể về mặt lâm sàng đối với các nếp nhăn in vivo [54].
Các biện pháp ngăn ngừa và chuẩn bị trước khi điều trị
Ứng dụng của LLLT trong da liễu vẫn đang ở giai đoạn đầu và do đó nó chủ yếu được sử dụng như một liệu pháp bổ trợ cho các lựa chọn điều trị đã được thiết lập. Trong số những mối quan tâm trong việc sử dụng nó, đáng chú ý nhất là những vấn đề liên quan đến tính an toàn và hiệu quả của nó. Các chỉ định sử dụng tương đối rõ ràng hơn như rụng tóc, và như một biện pháp dự phòng chống lại sự hình thành sẹo [60]. Các chỉ định khác bao gồm chữa lành vết thương, trẻ hóa da bị tổn thương do ánh sáng, mụn trứng cá và xơ hóa. Đo liều lượng là một yếu tố quan trọng quyết định phần lớn đến hiệu quả. Việc lựa chọn giữa một số lượng lớn các thông số chiếu sáng như bước sóng, mật độ năng lượng, mật độ công suất, dạng xung và thời gian điều trị là một nhiệm vụ phức tạp và là một yếu tố giải thích tiềm năng cho một loạt các kết quả khác nhau đã được báo cáo [2]. LLLT thường là một lựa chọn điều trị an toàn, dung nạp tốt, nhưng một số chống chỉ định đã được đề xuất (Bảng 8.2). Do tác dụng kích thích sinh học của tia laser, bệnh lý ác tính và chiếu xạ trực tiếp lên tuyến giáp là những chống chỉ định được ghi nhận rõ ràng [61–65]. Chiếu xạ trực tiếp lên thai nhi trong thai kỳ thường được coi là chống chỉ định, mặc dù các mô hình động vật đã báo cáo không có tác dụng gây quái thai [65]. LLLT gây kích ứng mắt, do đó nên tránh chiếu xạ trực tiếp lên võng mạc cũng như sử dụng cho những người mắc chứng sợ ánh sáng hoặc da nhạy cảm với ánh sáng [65]. Các chống chỉ định khác vẫn đang được xem xét bao gồm: bệnh truyền nhiễm và sốt do tác dụng kích thích sinh học của laser đối với các tác nhân lây nhiễm, và tác dụng kìm khuẩn tiềm năng của laser đối với hệ vi sinh [65]. Về việc sử dụng LLLT ở trẻ em, cho đến nay, chưa có tài liệu nào báo cáo về bất kỳ tác dụng phụ nào từ việc sử dụng LLLT trên các đĩa tăng trưởng. Tuy nhiên, đôi khi được liệt kê là chống chỉ định trong sách hướng dẫn vận hành thiết bị cũng như tài liệu, nên tốt nhất là tránh chiếu xạ trực tiếp lên các đĩa tăng trưởng như một biện pháp phòng ngừa. LLLT không chống chỉ định ở trẻ em. Da có hình xăm và da có sắc tố sẫm màu hơn có thể hấp thụ năng lượng ánh sáng hiệu quả hơn và dự đoán nguy cơ gia tăng các tác dụng phụ; một patch test được khuyến cáo thực hiện trước khi điều trị. Liều lượng thấp hơn – giảm xuống còn 50–75% liều lượng đề nghị cũng được khuyến nghị.
Kỹ thuật điều trị
Trước khi điều trị, vùng da mục tiêu nên được làm sạch bằng cồn và nên loại bỏ lông thừa trên cơ thể. Điều quan trọng cần lưu ý là không dùng các sản phẩm như kem dưỡng da, gel hoặc thuốc mỡ trên da của bệnh nhân trong quá trình chiếu LLLT. Kỹ thuật tĩnh nên được sử dụng để cho phép truyền năng lượng hiệu quả nhất. Để đảm bảo độ sâu thâm nhập, bác sĩ nên chỉnh thiết bị chiếu trực tiếp, chắc chắn với vùng da của bệnh nhân trong suốt quy trình. Cả người sử dụng và người được điều trị bằng laser mức độ thấp phải đeo kính bảo vệ do nhà sản xuất cung cấp trước khi bắt đầu sử dụng ánh sáng.
Tư vấn và Kế hoạch chăm sóc sau Điều trị
Không có hướng dẫn cụ thể cho việc theo dõi điều trị LLLT. Cũng như nhiều phương pháp điều trị bằng laser khác, bệnh nhân cần được thăm khám và theo dõi chặt chẽ xem có tác dụng phụ sau điều trị hay không và được hướng dẫn cách chăm sóc da đúng cách. Nên tuân thủ các đề xuất chung về chăm sóc da sau khi phẫu thuật laser. Lưu ý rằng khu vực được điều trị có thể có hồng hoặc đỏ trong 4–8 giờ đầu tiên sau khi điều trị với cảm giác châm chích / ngứa ran có thể xảy ra. Bệnh nhân nên được hướng dẫn không chà xát, gãi hoặc đè lên vùng điều trị cho đến khi hết ban đỏ hoặc sạch vảy. Nên tránh trang điểm hoặc dùng lotion cho đến khi các dấu hiệu mẩn đỏ và châm chích đã biến mất. Nên sử dụng kem dưỡng ẩm thích hợp trong suốt thời gian điều trị và ít nhất ba tháng sau lần điều trị cuối cùng. Được phép rửa vùng điều trị nếu thực hiện nhẹ nhàng bằng nước, nhưng thường không nên đi bơi cho đến sau 2-4 tuần tùy thuộc vào quy trình được thực hiện. Chườm đá hoặc chườm lạnh có thể được áp dụng để giảm bớt ban đỏ, phù nề và ngứa. Nói chung, nên tránh kích ứng vùng điều trị bằng cách sử dụng các chất làm sạch nhẹ hơn. Cần tránh tiếp xúc trực tiếp với ánh nắng mặt trời và thoa kem chống nắng thích hợp nếu cần.
Các biến chứng
LLLT nói chung là một phương thức điều trị an toàn, ít rủi ro, được dung nạp tốt với các tác dụng phụ và biến chứng tối thiểu. Hiện tại, các tác dụng phụ được báo cáo một cách đáng tin cậy bởi các nghiên cứu bao gồm: ban đỏ sau điều trị, tăng sắc tố, phù nề, khô da và cảm giác bỏng rát ở các vùng điều trị [5]. Tuy nhiên, khi được sử dụng bởi các bác sĩ lâm sàng được đào tạo bài bản về chỉ định, chống chỉ định, liều lượng và cách dùng LLLT, sẽ có rất ít thời gian downtime và hiếm khi xảy ra các tác dụng ngoại ý. Trong y văn, rất ít tác dụng phụ được báo cáo, ngay cả khi thử nghiệm ở liều cao hơn liều tối ưu. Ngay cả trong trường hợp có tác dụng phụ bất lợi, các triệu chứng thường thoáng qua. Trên thực tế, trong một đánh giá có hệ thống năm 2018 về 31 thử nghiệm có đối chứng về điều trị bằng đèn LED trên tất cả các chỉ định nói trên (tức là mụn trứng cá, trẻ hóa da, chữa lành vết thương, v.v.), chỉ có 8 báo cáo tác dụng phụ.
Tài liệu tham khảo
1. Avci P, Sadasivam AGM, Vecchio D, Pam Z, Pam N, Hamblin MR. Low-level laser (light) therapy (LLLT) in skin: stimulating, healing, restoring. Semin Cutan Med Surg. 2013;32(1):41–52. 2. Chung H, et al. The nuts and bolts of low-level laser (light) therapy. Ann Biomed Eng. 2012;40(2): 516– 33. 3. Ketty Peris TM, Piccolo D, Concetta M. Dermoscopic features of actinic keratosis. J German Soc Dermatol. 2007;5(11):970–5. 4. de Freitas LF, Hamblin MR. Proposed mechanisms of photobiomodulation or low-level light therapy. IEEE J Selected Top Quantum Electron. 2016;22(3):7000417. 5. Jagdeo J, et al. Light-emitting diodes in dermatology: a systematic review of randomized controlled trials. Lasers Surg Med. 2018;50(6):613–8. 6. Opel DR, Hagstrom E, Pace AK, Sisto K, HiranoAli SA, Desai S, Swan J. Light-emitting diodes: a brief review and clinical experience. J Clin Aesthet Dermatol. 2015;8(6):36–44. 7. Andrew Mamalis DS, Jagdeo J. Visible red light emitting diode photobiomodulation for skin fibrosis: key molecular pathways. Curr Dermatol Rep. 2016;5(1):121–8. 8. Kim SK, You HR, Kim SH, Yun SJ, Lee SC, Lee JB. Skin photorejuvenation effects of light-emitting diodes (LEDs): acomparative study of yellow and red LEDs in vitro and in vivo. Clin Exp Dermatol. 2016;41(7):798–805. 9. Andrew Mamalis MG, Jagdeo J. Light emitting diode-generated blue light modulates fibrosis characteristics: fibroblast proliferation, migration speed, and reactive oxygen species generation. Lasers Surg Med. 2015;47(2):210–5. 10. Taline Bavaresc AP, Moraes VM, Osmarin VM, Silveira DT, de Fátima Lucena A. Low-level laser therapy for treatment of venous ulcers evaluated with the nursing outcome classification: study protocol for a randomized controlled trial. Trials. 2018;19:372. 11. Tchanque-Fossuo CN, Ho D, Dahle SE, Koo E, Li CS, Isseroff RR, Jagdeo JA. A systematic review of low-level light therapy for treatment of diabetic foot ulcer. Wound Repair Regen. 2016;24(2):418–26. 12. Andrade F, de Oliveira Clark RM, Ferreira ML. Effects of low-level laser therapy on wound healing. Rev Col Bras Cir. 2014;41(2):129–33. 13. Trelles MA, Allones I, Mayo E. Combined visible light and infrared light-emitting diode (LED) therapy enhances wound healing after laser ablative resurfacing of photodamaged facial skin. Med Laser Appl. 2006;21:165–75.
14. Emı’lia de Abreu Chaves M, Araujo AR, Santos SF, Pinotti M, Oliveira LS. LED phototherapy improves healing of nipple trauma: a pilot study. Photomed Laser Surg. 2012;30(3):172–8. 15. de Oliveira RA, et al. Low-intensity LED therapy (658 nm) on burn healing: a series of cases. Lasers Med Sci. 2018;33(4):729–35. 16. Kajagar BM, Godhi AS, Pandit A, Khatri S. Efficacy of low level laser therapy on wound healing in patients with chronic diabetic foot ulcers—a randomised control trial. Indian J Surg. 2012;74(5):359– 63. 17. Tiran Zhang LL, Fan J, Tian J, Gan C, Yang Z, Jiao H, Han B, Liu Z. Low-level laser treatment stimulates hair growth via upregulating Wnt10b and β-catenin expression in C3H/HeJ mice. Lasers Med Sci. 2017;32(5):1189–95. 18. Kim JE, Woo YJ, Sohn KM, Jeong KH, Kang H. Wnt/β-catenin and ERK pathway activation: a possible mechanism of photobiomodulation therapy with light-emitting diodes that regulate the proliferation of human outer root sheath cells. Laser Surg Med. 2017;49(10):940–7. 19. Adil A, Godwin M. The effectiveness of treatments for androgenetic alopecia: a systematic review and metaanalysis. J Am Acad Dermatol. 2017;77(1):136–41. 20. Leavitt M, Charles G, Heyman E, Michaels D. HairMax LaserComb laser phototherapy device in the treatment of male androgenetic alopecia: a randomized, double-blind, sham device-controlled, multicentre trial. Clin Drug Investig. 2009;29(5):283–92. 21. Satino JL, Markou M. Hair regrowth and increased hair tensile strength using the HairMax LaserComb for low-level laser therapy. Int J Cosmet Surg Aesthet Dermatol. 2003;5:113–7. 22. Yamazaki M, Miura Y, Tsuboi R, Ogawa H. Linear polarized infrared irradiation using super Lizer is an effective treatment for multiple-type alopecia areata. Int J Dermatol. 2003;42(9):738–40. 23. Suchonwanit P, Chalermroj N, Khunkhet S. Lowlevel laser therapy for the treatment of androgenetic alopecia in Thai men and women: a 24-week, randomized, double-blind, sham device-controlled trial. Lasers Med Sci. 2019;34(6):1107–14. 24. Ablon G. Phototherapy with light emitting diodes: treating a broad range of medical and aesthetic conditions in dermatology the journal of clinical and aesthetic. Dermatology. 2018;11(2):21–7. 25. Lee SY, Ki-Ho P, Jung-Woo C, Jung-Kyun K, Rak LD, Sun SM, Sung LJ, Eui YC, Youn PM. prospective, randomized, placebo-controlled, double-blinded, and split-face clinical study on LED phototherapy for skin rejuvenation: clinical, profilometric, histologic, ultrastructural, and biochemical evaluations and comparison of three different treatment settings. J Photochem Photobiol: Biol. 2007;88(1):51–67. 26. Glen Calderhead R, Vasily DB. Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg. 2016;43(3):541–50. 27. McDaniel DH, Newman J, Geronemus RG, Weiss MA. Non-ablative non-thermal LED photomodulation—a multicenter clinical photoaging trial. Laser Surg Med. 2003;25:22. 28. Weiss RA, McDaniel D, Geronemus RG, et al. Clinical experience with light-emitting diode (LED) photomodulation. Dermatol Surg. 2005;31(9 Pt 2):1199–205.
29. Bhat J, Birch J, Whitehurst C. A single-blinded randomised controlled study to determine the efficacy of Omnilux revive facial treatment in skin rejuvenation. Lasers Med Sci. 2005;20(6):6–10. 30. Russell BA, Kellett N, Reilly LR. A study to determine the efficacy of combination LED light therapy (633nm and 830nm) in facial skin rejuvenation. J Cosmet Laser Therap. 2005;7:196–200. 31. Barolet D, Roberge C, Auger FA, Boucher A, Germain L. Regulation of skin collagen metabolism in vitro using a pulsed 660 nm LED light source: clinC. Zheng et al.217 ical correlation with a single- blinded study. J Investig Dermatol. 2009;12:2751–9. 32. Li W-H, Fassih A, Binner C, Parsa R, Southall MD. Low-level red LED light inhibits hyperkeratinization and inflammation induced by unsaturated fatty acid in an in vitro model mimicking acne. Laser Surg Med. 2018;50(2):158–65. 33. Gold MH, Goldberg DJ, Nestor MS. Current treatments of acne: medications, lights, lasers, and a novel 650-μs 1064-nm Nd: YAG laser. J Cosmet Dermatol. 2017;16(3):303–18. 34. Ashkenazi H, Malik Z, Harth Y. Eradication of Propionibacterium acnes by its endogenic porphyrins after illumination with high intensity blue light. FEMS Immunol Med Microbiol. 2003;35(1):17–24. 35. Morton CA, Scholefield R, Whitehurst C, Birch J. An open study to determine the efficacy of blue light in the treatment of mild to moderate acne. J Dermatol Treat. 2005;16:219–23. 36. Sorbellini E, Rucco M, Rinaldi F. Photodynamic and photobiological effects of light-emitting diode (LED) therapy in dermatological disease: an update. Lasers Med Sci. 2018;33(7):1431–9. 37. Akaraphanth R, Kanjanawanitchkul W, Gritiyarangsan P. Efficacy of ALA-PDT vs blue light in the treatment of acne. Photodermatol Photoimmunol Photomed. 2007;23:186–90. 38. Pawel Posadzki JC. Light therapies for acne. JAMA Dermatol. 2018;154(5):597–8. 39. Greb JE, Golminz AM, Elder JT, Lebwohl MG, Gladman DD, Wu JJ, Mehta NN, Finlay AY, Gottlieb AB. Psoriasis. Nat Rev Dis Primers. 2016; 24:2. 40. Pfaff S, Liebmann J, Born M, Merk HF, von Felbert V. Prospective randomized long-term study on the efficacy and safety of UV-free blue light for treating mild psoriasis vulgaris. Dermatology. 2015;231(1):24–34. 41. Weinstabl A, Hoff-Lesch S, Merk HF, von Felbert V. Prospective randomized study on the efficacy of blue light in the treatment of psoriasis vulgaris. Dermatology. 2011;223(3):251–9. 42. Niu T, Tian Y, Ren Q, Wei L, Li X, Cai Q. Red light interferes in UVA-induced photoaging of human skin fibroblast cells. Photochem Photobiol. 2014;90(6):1349–58. 43. Ablon G. Combination 830-nm and 633-nm lightemitting diode phototherapy shows promise in the treatment of recalcitrant psoriasis: preliminary findings. Photomed Laser Surg. 2010;28(1):141–6. 44. Mandel AS, Haberman HF, Pawlowski D, Goldstein E. Non PUVA nonsurgical therapies for vitiligo. Clin Dermatol. 1997;15(6):907–19. 45. Yu HS, Wu C, Yu CL, Kao YH, Chiou MH. Heliumneon laser irradiation stimulates migration and proliferation in melanocytes and induces repigmentation in segmental-type vitiligo. J Investig Dermatol. 2003;120(1):56–64.
46. Lan CC, Wu C, Chiou MH, Chiang TY, Yu HS. Lowenergy helium-neon laser induces melanocyte proliferation via interaction with type IV collagen: visible light as a therapeutic option for vitiligo. Br J Dermatol. 2009;161(2):273–80. 47. Alghamdi KM, Kumar A, Al-ghamdi A, Al-rikabi AC, Mubarek M. Ultra-structural effects of different low-level lasers on normal cultured human melanocytes: an in vitro comparative study. Lasers Med Sci. 2016;31(9):1819–25. 48. AlGhamdi KM, Kumar A, Ashour AE, AlGhamdi AA. A comparative study of the effects of different low-level lasers on the proliferation, viability, and migration of human melanocytes in vitro. Lasers Med Sci. 2015;30(5):1541–51. 49. Wolfram D, Tzankov A, Pulzl P, Piza-Katzer H. Hypertrophic scars and keloids—a review of their pathophysiology, risk factors, and therapeutic management. Dermatol Surg. 2009;35(2):171–81. 50. Bouzari N, Davis S, Nouri K. Laser treatment of keloids and hypertrophic scars. Int J Dermatol. 2007;46(1):80–8. 51. Uitto J. IL-6 signaling pathway in keloids: a target for pharmacologic intervention? J Investig Dermatol. 2007;127(1):6–8. 52. Ghazizadeh M, Tosa M, Shimizu H, Hyakusoku H, Kawanami O. Functional implications of the IL-6 signaling pathway in keloid pathogenesis. J Investig Dermatol. 2007;127(1):98–105. 53. Liu W, Wang D, Cao YL. TGF-beta: a fibrotic factor in wound scarring and a potential target for antiscarring gene therapy. Curr Gene Ther. 2004;4(1): 123–6. 54. Barolet D, Boucher A. Prophylactic low-level light therapy for the treatment of hypertrophic scars and keloids: a case series. Laser Surg Med. 2010;42(6):597–601. 55. Alsharnoubi J, Shoukry KE-S, Fawzy MW, Mohamed O. Evaluation of scars in children after treatment with low-level laser. Lasers Med Sci. 2018;33:1991. 56. Menezes S, Coulomb B, Lebreton C, Dubertret L. Non-coherent near infrared radiation protects normal human dermal fibroblasts from solar ultraviolet toxicity. J Investig Dermatol. 1998;111(4): 629–33. 57. Frank S, Oliver L, Coster CL-D. Infrared radiation affects the mitochondrial pathway of apoptosis in human fibroblasts. J Investig Dermatol. 2004;123(5):823–31. 58. Applegate LA, Scaletta C, Panizzon R, Frenk E, Hohlfeld P, Schwarzkopf S. Induction of the putative protective protein ferritin by infrared radiation: implications in skin repair. Int J Mol Med. 2000;5(3):247–51. 59. Barolet D, Boucher A. LED photoprevention: reduced MED response following multiple LED exposures. Laser Surg Med. 2008;40(2):106–12. 8 Light Emitting Diodes and Low Level Laser Light Therapy218 60. Won-Serk Kim RGC. Is light-emitting diode phototherapy (LED-LLLT) really effective? Laser Therapy. 2011;20(3):205–15. 61. Baxter D. Electrotherapy: evidence-based practice. 11th ed. London: WB Saunders; 2003.
62. Belanger AY. Evidence-based guide to therapeutic physical agents. Philadelphia, PA: LippincottWilliams & Wilkins; 2002. 63. Ann Reed JL. Electrotherapy explained: principles and practice. 3rd ed. London: Elsevier HealthSciences; 1999. 64. Jan Tuner LH. Laser therapy clinical practice & scientific background. Grangesberg: Prima Books; 2014. 65. Leos Navratil JK. Contraindications in noninvasive laser therapy: truth and fiction. J Clin Laser Med Surg. 2002;20(6):341–3.